Лобно-височная деменция — нейродегенеративное заболевание, сопровождающееся прогрессирующими поведенческими и личностными расстройствами. Со временем, особенно без правильно подобранного лечения, человек полностью утрачивает способность к полноценному продуктивному контакту с окружающими (тотальное слабоумие). Патология развивается на фоне дегенеративных изменений лобных и передних отделов височных долей головного мозга. На сегодняшний день не существует лечебных протоколов и препаратов, с помощью которых можно вылечить человека, страдающего от лобно-височной деменции (ЛВД), однако доктора центра психического здоровья «Лето» индивидуально подберут медикаментозную терапию, способную затормозить прогрессирование тяжелых симптомов.
Классификация
В соответствии с современными стандартами психотерапии выделяют несколько форм лобной деменции:
- поведенческая с преобладанием личностных нарушений (встречается чаще всего);
- аграмматическая (семантическая);
- логопенический (однако по мнению некоторых специалистов, подобный вариант является скорее одной из атипичных разновидностей болезни Альцгеймера).
Атрофия может поражать височную, лобную или лобно-височную область мозга. Расположение очага — ещё один критерий определения формы болезни.
Клиническая картина
Недуг начинается между 45 и 70 годами, случаев лобно-височной деменции у подростков нет (при наличии схожей симптоматики у более молодых людей требуется более тщательная диагностика, так как вероятны или наследственные психические заболевания, или нарушения на фоне органического поражения головного мозга). Симптомы развиваются постепенно.
На ранних этапах преобладают личностные изменения, выраженность которых зависит от точной локализации нейродегенеративного процесса. При деменции лобного типа постепенно развиваются:
- бездеятельность;
- вялость;
- отсутствие внешних эмоциональных проявлений;
- безразличие ко всему происходящему вокруг;
- снижение и упрощение психической активности,
- замедление, искажение речи (вплоть до потери возможности говорить),
- скудность движений, лежачий образ жизни.
При локализации патологического процесса в орбитальной коре в клинической картине превалируют:
- утрата чувства такта, дистанции;
- потеря нравственных установок и принципов;
- импульсивность поступков;
- грубые нарушения когнитивного спектра (теряется способность к абстрактному мышлению, планированию, выполнению многоступенчатых действий), но в то же время сохраняется память, ориентировка в пространстве и окружающем.
Атрофия височных долей сопровождается стереотипиями — бессмысленными, нелогичными повторениями фраз или отдельных слов, движений, например, топанье, хлопанье в ладоши, растирание кожи, почесывание, сжатие губ, причмокивание и т.д. Иногда появляется навязчивый счет: пациент постоянно считает количество пройденных шагов, ступеней и т.д.
Кроме того, отмечают явно патологическую склонность к чистоте, которая иногда принимает форму фобии. Еще одна форма стереотипий — строжайшее соблюдение установленного распорядка дня, изменение которого вызывает у человека настоящую панику.
Кроме того, ЛВД сопровождается:
- астенической симптоматикой (слабостью, быстрой утомляемостью, головными болями, бессонницей);
- двигательными расстройствами, ригидностью мускулатуры;
- формированием бредовых идей;
- расстройствами речи (причем у 60% пациентов их отмечают на начальном этапе патологии).
Одним из ключевых симптомов является ранняя утрата способности понимать чужие эмоции и сопереживать им. Человека перестают интересовать чувства и переживания окружающих (в том числе и близких людей), он равнодушен к чужому горю, из-за чего больной обычно попадает в социальную изоляцию.
Характерны также и изменения пищевого поведения. Для лобно-височной деменции типично пристрастие к сладостям, или же к продуктам строго определенного цвета, формы, или же с каким-либо специфическим запахом. Утрачивается чувство насыщения. На более поздних этапах ЛВД больной может стремиться попробовать на вкус любые предметы, в том числе и явно несъедобные.
Можно ли вылечить
Прогноз при лобной деменции зависит от скорости развития дегенеративных изменений. На ранних стадиях заболевания у пациентов отсутствуют серьезные нарушения и расстройства, поэтому при их лечении эффективной является комплексная терапия.
При полной деградации личности появляются проблемы с ориентацией в пространстве, выражением мыслей, уходом за собой, поэтому больному необходима помощь опытных врачей-неврологов и близких людей. На поздних стадиях мышцы атрофируются, поэтому больной вынужден вести малоподвижный, лежачий образ жизни. Деменция лобной доли на последней стадии может вызвать вторичные заболевания.
Продолжительность больных с тяжелым слабоумием может достигать 15 лет при адекватной терапии. При обнаружении симптомов заболевания важно обратиться к врачу-неврологу. Специалисты Юсуповской больницы подбирают для пациентов современные методы терапии, позволяющие поддерживать интеллектуальную и физическую активность больных, улучшать качество их жизни.
Диагностика
Некоторые симптомы лобно-височной деменции (бредовые идеи, сексуальная расторможенность и т.д.) типичны и для других психических недугов, в частности для шизофрении, болезни Альцгеймера. Поэтому доктора клиники «Лето» придерживаются принципов поэтапной диагностики с исключением всех вероятных диагнозов.
Обследование включает такие этапы:
- Сбор семейного анамнеза (при необходимости мы изучаем амбулаторные карты родственников пациента, у которых были выявлены отклонения психики);
- Тщательное изучение клинической картины. Врач подробнейшим образом расспрашивает близких о том, как началась болезнь, какие признаки появились в первую очередь, как именно ведет себя больной, каким образом проявляются психические и поведенческие нарушения.
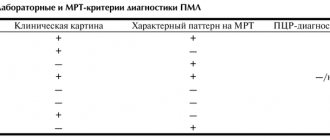
- Инструментальные исследования. Обязательно назначают томографию головного мозга. На КТ, МРТ и ПЭТ-КТ (считается наиболее информативной) отчетливо видны признаки избирательной атрофии.
Причины
Лобно-височная деменция – это постепенно развивающийся, неуклонно прогрессирующий дегенеративно-дистрофический патологический процесс в ткани головного мозга, приводящий к деградации с распадом речи, в основном произносимой вслух. Средний возраст больных – 53 – 60 лет, но болезнь может начинаться раньше или позже, мужчины заболевают чаще женщин.
Считается, что в основе заболевания лежит наследственная мутация генов в области 17 хромосомы. В некоторых случаях была выявлена вовлеченность 9, 14 и 3 хромосом. Встречались многочисленные случаи семейных случаев заболеваемости. Известны семьи, в которых наблюдались и другие формы наследственно-дегенеративных заболеваний.
Важно. Внешние воздействия (травмы, болезни) имеют провоцирующую роль и утяжеляют течение лобно-височной деменции, особенно актуально это для детей и подростков. Если ребенок отстает в развитии, не справляется со школьной программой, имеет особенности в поведении,стоит обратиться к детскому неврологу, психиатру.
Височно-лобная деменция у подростков и у детей совсем не редкость. Причиной заболевания является отягощенная наследственность, а пусковыми факторами – черепно-мозговые травмы, нейроинфекции и др.
Стоимость услуг
| КОНСУЛЬТАЦИИ СПЕЦИАЛИСТОВ | |
| Первичная консультация врача психиатра (60 мин.) | 6 000 руб. |
| Повторная консультация | 5 000 руб. |
| Консультация психиатра-нарколога (60 мин.) | 5 000 руб. |
| Консультация психолога | 3 500 руб. |
| Консультация Громовой Е.В. (50 минут) | 12 000 руб. |
| ПСИХОТЕРАПИЯ | |
| Психотерапия (сеанс) | 7 000 руб. |
| Психотерапия (5 сеансов) | 30 000 руб. |
| Психотерапия (10 сеансов) | 60 000 руб. |
| Групповая психотерапия (3-7 человек) | 3 500 руб. |
| Сеанс психотерапии у Громовой Е.В. (50 минут) | 12 000 руб. |
| ЛЕЧЕНИЕ В СТАЦИОНАРЕ | |
| Палата 4-х местное размещение | 10 000 руб./сутки |
| Палата 3-х местное размещение | 13 000 руб./сутки |
| Палата 1 местное размещение VIP | 23 000 руб./сутки |
| Индивидуальный пост | 5 000 руб. |
| ПИТ | 15 000 руб./сутки |
В данном перечне представлены не все цены на услуги, которые предоставляет наша клиника. С полным прайсом можно ознакомиться на странице «Цены», либо по телефону: 8(969)060-93-93. Первичная консультация БЕСПЛАТНА!
Лечение лобно-височной деменции в мед
Терапия преимущественно сводится к назначению общеукрпеляющих препаратов. Это поливитаминные комплексы, ноотропы, средства для нормализации метаболизма, кардио- и нейропротекторы. Однако перечисленные лекарства способны лишь поддержать функционирование внутренних органов и систем, и по большому счету, никак не влияют на симптоматику ЛВД.
Особенности клинической картины недуга и риск быстрого развития тотального слабоумия заставляет врачей использовать все медикаментозные ресурсы современной психиатрии и неврологии. Так, по данным исследований, при лобно-височной деменции хороший результат оказывают препараты, применяемые для лечения болезни Альцгеймера (ингибиторы холинэстеразы и NDMA-антагонисты).
Для коррекции поведенческих нарушений назначают:
- антидепрессанты (предпочтение отдают препаратам из группы селективных ингибиторов обратного захвата серотонина): показаны при тревожности, депрессии, обсессивных расстройствах;
- нейролиптики и вальпроаты: применяют при агрессивности, психомоторном возбуждении.
Так как больные быстро теряют способность к самообслуживанию и выполнению элементарных повседневных обязанностей, мы предлагаем проводить лечение в стационаре, где пациентам обеспечен круглосуточный уход и наблюдение квалифицированного медицинского персонала.
Для записи на прием и дополнительной консультации звоните нам по телефону 8(969)060-93-93.
Введение
Термин «лобно-височные деменции» (ЛВД) в настоящее время используется в качестве общего названия для группы нейродегенеративных заболеваний, состоящей из трех основных клинических типов: поведенческого варианта ЛВД (П-ЛВД) и первично прогрессирующей афазии (ППА), которая включает два афатических варианта ЛВД: семантический (С-ППА) (семантическая деменция) и ППА со снижением беглости речи (аграмматический вариант ППА — А-ППА).
Клинические проявления, характерные для ЛВД, часто проявляются и при трех других нейродегенеративных заболеваниях с тяжелыми двигательными расстройствами: кортикобазальной дегенерации (КБД), прогрессирующем надъядерном параличе (ПНП) и боковом амиотрофическом склерозе (БАС) [1]. Несмотря на широкий спектр клинических проявлений, вышеуказанные заболевания обычно обозначаются общим термином «лобно-височная долевая дегенерация» (ЛВДД), поскольку их клинические типы часто имеют общие нейроморфологические субстраты.
Клиническая картина ЛВД определяется прогрессирующими поведенческими нарушениями, расстройствами исполнительных функций и выраженным речевым дефицитом. ЛВД является распространенным типом деменции, особенно у пациентов пресенильного возраста. Появление первых симптомов заболевания обычно происходит до 60 лет, а средние сроки выживаемости от момента установления диагноза варьируют от 3 до 10 лет. Распространенность ЛВД составляет 15 на 100 000 населения в возрасте от 45 до 65 лет, что аналогично распространенности болезни Альцгеймера (БА) в этой возрастной группе [2]. ЛВД могут имитировать различные психические расстройства (например, большое депрессивное расстройство, биполярное аффективное расстройство, шизофрения, обсессивно-компульсивное расстройство, пограничные расстройства личности и др.) вследствие наличия выраженных поведенческих нарушений и раннего возраста начала заболевания, что нередко приводит к неправильной постановке диагноза и, как следствие, неправильной терапевтической тактике.
Лежащие в основе ЛВД нейроморфологические особенности определяют клинический фенотип, который характеризуется селективной нейродегенерацией лобной и височной коры головного мозга. В зависимости от первичной локализации атрофии, в клинических проявлениях преобладают либо поведенческие, либо речевые нарушения. Генетическая предрасположенность является важным фактором риска ЛВД. Общей особенностью ЛВД является накопление определенных нейрональных белков. Из них наиболее важными являются τ-протеин, ассоциированный с микротрубочками (Microtubule-associated protein tau — МАРТ), трансактивный ДНК-связывающий белок (Transactiveresponse DNA-binding protein 43 kDa — TDP-43), РНК-связывающий белок (Tumor associated protein fused in sarcoma —FUS). Наличие случаев деменции в семейном анамнезе отмечается в 40% случаев ЛВД, хотя явный аутосомно-доминантный тип наследования обнаружен лишь в 10% случаев [3]. Показано, что мутации в генах C9orf72
,
MAPT
и
GRN
составляют около 60% всех случаев наследственной ЛВД [4]. Проведение генетического исследования считают необходимым при наличии наследственной отягощенности у больных деменцией, в первую очередь при аутосомно-доминантных неврологических заболеваниях, таких как ЛВД, БА, паркинсонизм, БАС, миопатии и психозы позднего возраста [4, 5].
Последние достижения в области клинической практики, нейровизуализационных исследований и молекулярно-генетических открытий, значительно повысив точность диагностики ЛВД, позволяют дифференцировать клинические варианты заболевания и отграничивать их от других психических расстройств. По мере того, как улучшается понимание молекулярно-генетических основ ЛВД, появляются и новые рациональные методы лечения [6].
В настоящем обзоре рассматриваются применяющиеся в настоящее время методы лечения ЛВД, обсуждаются последние достижения в области ЛВД, позволяющие совершенствовать и развивать терапевтические методики, а также анализируются результаты недавно завершенных и выполняющихся в настоящее время клинических испытаний. Рассматривается целесообразность применения нефармакологических методов ЛВД.
Терапевтические аспекты изучения ЛВД
Фармакологические стратегии
Исследований, направленных на поиск терапевтических средств для лечения ЛВД, было проведено значительно меньше, чем при Б.А. Согласно данным интернет-ресурса www.clinicaltrials.gov, предоставленным Американской национальной библиотекой медицины, при оценке 293 985 клинических исследований (данные на январь 2021 г.), проведенных в 207 странах мира и в 50 американских штатах, выявили, что было проведено или проводится в настоящее время 150 фармакологических и нефармакологических испытаний при ЛВД, в то время как при БА — 2021.
До сих пор Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (Food and Drug Administration — FDA, USFDA) не утвердило ни одного лекарственного препарата, показанного для применения при ЛВД [7]. В настоящее время предлагается лишь несколько фармакологических подходов (официально неподтвержденных и не рекомендованных для лечения ЛВД), в частности симптоматическое использование антидепрессантов, нейролептиков, ингибиторов холинэстераз и мемантина.
Систематический поиск в 4 основных базах данных (PubMed, Medline, Psych INFO и Cochrane) показал, что за последнее годы было проведено лишь 9 рандомизированных контролируемых двойных слепых клинических исследований, в которых рассматривалась эффективность разных препаратов при лечении больных ЛВД. Среди них 2 исследования были направлены на изучение эффективности пароксетина — антидепрессанта из группы селективных ингибиторов обратного захвата серотонина (СИОЗС); 1 — антидепрессанта тразодона, 2 — стимуляторов: метилфенидата и декстроамфетамина. Только 1 исследование было посвящено применению ингибитора ацетилхолинэстеразы (АХЭ) галантамина. В 2 работах выявляли эффективность антагониста N-метил-D-аспартата мемантина. Была также предпринята попытка назначения пациентам с ЛВД нейропептидного препарата окситоцина. Анализ полученных результатов показал, что СИОЗС, тразодон и амфетамины могут быть эффективными в уменьшении выраженности некоторых поведенческих симптомов, однако ни одно из этих лекарственных средств не влияет на когнитивное функционирование больных [8].
S. Lopez-Pousa и соавт. [9] провели обсервационное исследование, в которое были включены 1092 пациентов с БА и 64 больных ЛВД. Анализ проводимой терапии показал, что 43,8% пациентов с ЛВД лечились противодементными препаратами, 31,3% — нейролептиками, 1,6% — противопаркинсоническими препаратами и 53,1% пациентов принимали антидепрессанты. Исследователи пришли к выводу о несоответствии клинической практики и терапевтических рекомендаций, основанных на клинических данных. Однако, по мнению авторов, это не означает, что эти виды терапии являются малоэффективными. Подтверждено [10—14], что прием антидепрессантов и антипсихотиков улучшает, главным образом, поведенческие симптомы ЛВД, такие как раздражительность, возбуждение, симптомы депрессии и нарушения пищевого поведения.
Ингибиторы
АХЭ
Ингибиторы АХЭ успешно применяющиеся при лечении БА, достаточно широко изучались и для терапии когнитивных нарушений у пациентов с ЛВД, однако все они оказались неэффективными. В частности, препарат донепезил, который в 6-месячном открытом исследовании [15] принимали 24 пациента с ЛВД, вызвал ухудшение симптомов ЛВД, а у 4 больных — усиление поведенческих симптомов. Прекращение приема препарата привело к снижению поведенческих расстройств.
Изучение эффективности ривастигмина проводилось в 12-месячном открытом исследовании с участием пациентов с ЛВД. Результаты исследования продемонстрировали, что прием препарата способствовал небольшому улучшению выраженности поведенческих нарушений, которые оценивались по нейропсихиатрическому опроснику NPI, и, в частности, снижению нагрузки на ухаживающих за больными. Однако применение ривастигмина не предотвращало нарастание расстройств когнитивных функций [16].
Терапию третьим, наиболее часто используемым ингибитором АХЭ, галантамином, применяли у 36 пациентов с П-ЛВД и ППА в ходе 8-недельного плацебо контролируемого и последующего 18-недельного открытого исследования [17]. По результатам исследования, у пациентов с ППА на фоне лечения речевые функции оставались стабильными, что было расценено как тенденция к эффективности. Однако авторы предположили, что, возможно, у этих пациентов была логопедическая форма ППА, которая очень близка к Б.А. Терапевтический эффект в отношении поведенческих расстройств при приеме галантамина не был установлен.
По мнению ряда авторов [16—18], применение ингибиторов АХЭ у больных ЛВД может усилить поведенческие расстройства и нарушение двигательных функций, из-за чего использование препаратов этой группы при ЛВД не рекомендуется.
С учетом полученных ранее данных о положительных терапевтических эффектах препарата мемантин, имеющего терапевтические показания для лечения умеренной и тяжелой стадии БА, в отношении когнитивных способностей и общего функционирования было проведено несколько исследований для определения терапевтической эффективности мемантина у больных ЛВД.
В открытом исследовании М. Swanberg [19] у части пациентов с ЛВД, получавших мемантин, было отмечено улучшение общего показателя оценки некогнитивных расстройств (по опроснику NPI), в основном за счет уменьшения апатии, ажитации и тревоги. В том же наблюдении у пациентов c ЛВД наблюдалась хорошая переносимость терапии мемантином. Однако результаты мультицентрового рандомизированного двойного слепого плацебо-контролируемого исследования [20], в котором пациенты с ЛВД принимали мемантин в суточной дозе 20 мг или плацебо в течение 26 нед, не подтвердили эффективность препарата при ЛВД. Тем не менее было показано улучшение ряда показателей по опроснику NPI и по шкале общего клинического впечатления CGI-C, не достигающее уровня статистической значимости [20].
В открытом пилотном исследовании [21] терапевтических эффектов мемантина у 17 пациентов с ЛВД оценивались метаболическая активность лобной и височной доли головного мозга при проведении позитронно-эмиссионной томографии (ПЭТ) с 18FФДГ (18F-фтордезоксиглюкоза), а также поведенческие расстройства с использованием специальных шкал. Через 6 мес терапии мемантином было установлено повышение метаболической активности в левой орбитофронтальной области коры у 5 пациентов с С-ППА. Кроме того, было отмечено отсроченное повышение метаболизма левой и правой доли островка, левой передней поясной извилины. В правой передней поясной извилине метаболическая активность повысилась в начале терапии, ее показатели продолжили улучшаться в дальнейшем к 6-му месяцу терапии. Однако показатели поведенческих нарушений, оцениваемые по опроснику лобных поведенческих симптомов FBI, ухудшились на 43,3%. Повышение кортикальной метаболической активности у пациентов с С-ППА сохранялось в течение 6 мес. Авторы пришли к заключению о необходимости проведения соответствующего двойного слепого плацебо-контролируемого исследования.
Метаанализ научных публикаций [22], посвященных использованию мемантина у пациентов с ЛВД в рамках двух плацебо-контролируемых исследований, показал, что состояние 130 пациентов с ЛВД, получавших препарат, при оценке по ряду тестов и шкал, например краткой шкале оценки психического статуса MMSE, NPI, опроснику бремени Зарита ZBI, улучшалось по сравнению с пациентами, получавшими плацебо, однако различия не достигали степени статистической достоверности. Авторы считают, что мемантин может быть полезен при лечении пациентов с ЛВД, однако подчеркивают наличие ограничений при экстраполяции результатов, полученных при терапии больных БА, на лечение пациентов с ЛВД и признают необходимым проведение дальнейших рандомизированных двойных слепых плацебо-контролируемых исследований с привлечением большего числа пациентов.
Среди антидепрессантов для лечения ЛВД в основном применялись СИОЗС. В 2004 г. М. Ikeda и соавт. [23] сообщали о результатах открытого 12-недельного исследования, в ходе которого проводилось лечение 60 пациентов с П-ЛВД и С-ППА флувоксамином. Изменение поведенческих и других психопатологических симптомов оценивалось по опроснику NPI [24]. По полученным данным, флувоксамин значительно уменьшал поведенческие симптомы у больных ЛВД, особенно стереотипии в поведении, однако оценки когнитивных функций по шкале MMSE [25] не изменились.
Препарат тразодон, антагонист обратного захвата серотонина, производное тиазолопиридина, применялся в рандомизированном двойном слепом плацебо-контролируемом перекрестном исследовании [26] у 31 пациента с поведенческими симптомами при ЛВД, оценка которых проводилась по опроснику NPI. На фоне терапии тразодоном поведенческие расстройства, особенно нарушения пищевого поведения, а также ажитация, раздражительность, симптомы депрессии и дисфории значительно уменьшились. В период после отмены препарата была отмечена стабильность улучшения (от легкого до умеренного) в клинических проявлениях заболевания, однако оценки когнитивных функций по шкале MMSE не изменились.
В двух клинических исследованиях [27, 28] оценивали эффективность пароксетина — селективного ингибитора обратного захвата 5-гидрокситриптамина (5-HT) и серотонина серотонинергическими нейронами — у пациентов с ЛВД. Первое исследование [27], в которое были включены 16 пациентов с ЛВД, было открытым рандомизированным неконтролируемым и не перекрестным. В 1-ю группу вошли 8 пациентов, которым был назначен пароксетин 20 мг/сут, 8 пациентов 2-й группы получали пирацетам 1200 мг/сут. После 14 мес терапии у пациентов 1-й группы (пароксетин) было отмечено значительное уменьшение проявлений поведенческих расстройств. Кроме того, была констатирована редукция стресса у ухаживающих за больными. В другом рандомизированном двойном слепом плацебо-контролируемом перекрестном исследовании [28] принимали участие 10 пациентов с ЛВД, которые в течение 12 нед получали пароксетин с постепенным (на 10 мг в неделю) повышением дозировки препарата до 40 мг/сут. Авторы не обнаружили значительного улучшения состояния больных по поведенческим шкалам, только по некоторым психологическим показателям (например, в обучающей модели распознавания образов) была отмечена положительная динамика. Наблюдались нежелательные побочные явления при приеме пароксетина в дозе 40 мг/сут, при которых состояние пациентов выглядело, как триптофановое истощение. Расхождения в результатах этих двух клинических исследований, скорее всего, связаны с отличающимися процедурами и дизайном исследований, а также с различиями в дозировке применявшегося препарата. Доза пароксетина 40 мг/сут была признана слишком высокой для пациентов с ЛВД. Оптимальная доза препарата, поддерживающая баланс между терапевтическим эффектом и отсутствием побочных явлений, составляла 20 мг/сут.
В группе антипсихотических средств наибольшее внимание исследователей привлекали атипичные нейролептики. По мнению ряда авторов [12, 29], нейролептики, такие как арипипразол и оланзапин, могут улучшить клинические состояние больных с ЛВД, оказывая влияние на поведенческие расстройства и раздражительность. Назначение кветиапина в ряде случаев показало снижение ажитации у пациентов с П-ЛВД [30], однако в двойном слепом перекрестном исследовании [31] у 8 пациентов положительные изменения (по опроснику NPI) не были отмечены. Подчеркивается, что эти препараты также могут вызывать побочные эффекты, такие как сонливость, увеличение массы тела, симптомы паркинсонизма. Кроме того, они повышают вероятность экстрапирамидных побочных эффектов, что ограничивает их терапевтическое применение.
Крайне неубедительны сведения о целесообразности использования у пациентов с ЛВД для купирования поведенческих и аффективных нарушений противоэпилептических препаратов с нормотимическими эффектами, таких как дериваты вальпроевой кислоты, топирамат, карбамазепин, тем более что сообщения об их терапевтических эффектах ограничиваются единичными случаями [30, 32].
В работе S. Jesso и соавт. [33] у 20 пациентов с П-ЛВД в двойном слепом плацебо-контролируемом рандомизированном исследовании с перекрестным дизайном был использован нейропептидный препарат окситоцин в дозе 24 МЕ.
Цель исследования — оценка влияния разовой дозы интраназального окситоцина на поведенческие и эмоциональные нарушения. Через 8 ч и через 1 нед после введения препарата у пациентов, получавших окситоцин, проводили обследование по опроснику NPI. Отмечалось значительное улучшение показателей по NPI как в сравнении с группой плацебо, так и с исходными показателями. Предполагается, что окситоцин является потенциально перспективным кандидатом для симптоматического лечения пациентов с П-ЛВД. Обоснована необходимость дальнейшего изучения этого нейропептида при лечении ЛВД.
Одно из последних клинических исследований, проведенных у пациентов с ЛВД [34], касалось определения безопасности и переносимости 3 дозировок интраназального окситоцина (24, 48, 72 МЕ) в параллельных группах больных (23 пациента с П-ЛВД, 3 — С-ППА) с использованием схемы повышения дозы препарата, вводимого 2 раза в день в течение 1 нед. Результаты исследования показали, что прием окситоцина в 3 дозировках был безопасен и хорошо переносился пациентами. Однако авторы считают, что для определения терапевтической эффективности долгосрочного приема интраназального окситоцина при ЛВД требуется более длительное многоцентровое исследование [34].
Целью 8 клинических исследований было изучение влияния психостимуляторов на симптомы апатии при деменции. Больным ЛВД назначались метилфенидат и декстроамфетамин. Была отмечена потенциальная польза терапии апатических нарушений психостимуляторами, однако подчеркивалась необходимость тщательной оценки физического состояния каждого пациента в связи с возможностью развития побочных соматических реакций в виде повышения артериального давления и развития тахикардии. Не меньшее значение придавалось риску появления раздражительности, развития ажитации и психозов [35].
Недавние научные достижения в понимании патобиологических процессов ЛВД позволили выявить некоторые новые потенциальные терапевтические цели и мишени для развития и создания новых эффективных болезнь-модифицирующих препаратов. Так, открытие факта распространения патологического τ-протеина транссинаптически прионоподобным образом в другие регионы головного мозга по корковым ассоциативным путям вызвало повышенный интерес к возможности использования антител для предотвращения транснейронального распространения патологических белков. Авторы этой идеи надеются в будущем таким образом найти способ предотвращения заболевания [36—38]. Другие возможные терапевтические подходы, связанные с тау-патиями, базируются на проверке эффективности ингибиторов τ-агрегации с производными метиленового синего и с микротубулярными стабилизаторами в качестве лекарственных средств (например, TPI 287), а также с разработкой τ-вакцин с использованием моноклональных τ-антител (МТА). [39].
Поскольку нейродегенерация у носителей мутаций програнулина связана с гаплонедостаточностью програнулина и снижением концентрации сывороточного програнулина, современными исследователями предпринимаются попытки сдерживать развитие нейродегенерации в переносчиках мутаций програнулина с помощью таких молекул, как ингибитор гистон деацетилазы субероиланилид гидроксамовой кислоты, который усиливает или увеличивает транскрипцию програнулина. Внимание исследователей привлечено к тому, что алкализиновые соединения, такие как хлорохин, бепридил и амиодарон, стимулируют выработку програнулина, а ингибиторы вакуолярной АТФазы увеличивают внутриклеточную и секретируемую концентрацию програнулина [40, 41]. Эти открытия являются основанием для разработки новых направлений исследований в области терапии ЛВД.
В 2015 г. появилась информация о проведении клинического исследования эффективности нимодипина (NCT01835665) [42], однако результаты этого исследования еще не опубликованы.
Новые потенциальные терапевтические цели и мишени для развития и создания новых эффективных болезнь-модифицированных препаратов, клинические исследования которых в настоящее время проводятся или подготовлены к исследованиям согласно данным интернет-ресурса www.clinicaltrials.gov, представлены в таблице.
Новые потенциальные терапевтические цели и мишени для создания эффективных болезнь-модифицированных препаратов для лечения ЛВД
Анализ исследований в области терапии ЛВД позволяет констатировать незначительную эффективность отдельных препаратов, таких как мемантин в отношении проявлений деменции и СИОЗС в отношении поведенческих симптомов заболевания. Однако достижения нейронаук создают перспективы для разработки генных технологий для терапии ЛВД и, возможно, для предупреждения развития этой тяжелой формы нейродегенеративной патологии у родственников.
В отечественных публикациях последних лет работ, посвященных терапии пациентов с ЛВД, очень мало. В одной из последних работ, опубликованной в 2021 г. [43], приводится анализ собственного опыта авторов по применению антидепрессантов СИОЗС и атипичных антипсихотиков у больных ЛВД с некогнитивными психическими расстройствами. Автором отмечено, что 8-недельный курс терапии циталопрамом и кветиапином у больных ЛВД уменьшает агрессию, раздражительность, аберрантное моторное поведение и эйфорию, а также улучшает ночной сон. При этом подчеркивается, что оба препарата мало влияли на тревожно-депрессивные симптомы и апатию. Кроме того, на фоне терапии кветиапином пациенты становились менее расторможенными, при приеме циталопрама уменьшилась выраженность нарушений пищевого поведения [43].
Нефармакологические терапевтические стратегии
Нефармакологические подходы к лечению ЛВД в последние годы приобретают особую значимость как наиболее предпочтительное вмешательство, предваряющее фармакологическую терапию, которая может усугубить сопутствующие соматические заболевания у пожилых пациентов с ЛВД. Основная цель нефармакологических вмешательств заключается в предотвращении асоциального и аддиктивного поведения, в облегчении симптомов болезни и уменьшении страданий людей, ухаживающих за такими пациентами. Поведенческие и когнитивные расстройства у пациентов с ЛВД часто приводят к возникновению тяжелого стресса как у родственников пациентов, так и у медицинских работников в связи с тем, что такие больные могут быть опасны и для себя, и для окружающих. Нефармакологические стратегии основываются на вовлечении пациентов в экологические, поведенческие и физкультурные мероприятия [44].
S. Cheng и соавт. [45] было показано, что физические упражнения у пациентов с деменцией способствовали улучшению когнитивного функционирования, повышению настроения и общего физического здоровья и должны быть рекомендованы всем пациентам, способным их выполнять.
Экологические подходы в ведении пациентов с ЛВД направлены на снижение раздражительности, агрессивности и беспокойства, поступающих из массива ежедневных стимулов, которые возникают из-за сложности обработки пациентами информации. Эти методики включают в себя снижение уровня шума, ограничение стимуляционных мероприятий, упрощение социальных влияний путем ограничения взаимодействия с небольшими группами и облегчение в устранении сложных повседневных действий, которые могут запутать и, следовательно, возбудить больных. Особое внимание следует уделять применению слуховых аппаратов и оптимизации сенсорной стимуляции для ограничения дискомфорта у пациентов. Полагают, что использование игровых методик или прежних увлечений может уменьшить расторможенность и неуместное поведение. М. Ikeda и соавт. [46] отметили, что включение в жизнь пациентов прежних (доболезненных) увлечений (хобби) и любимых ранее игр уменьшало асоциальное поведение и расторможенность у пациентов с ЛВД.
По мнению ряда авторов (www.theaftd.org), для облегчения бремени ухода за пациентами с ЛВД целесообразно проводить просветительскую работу среди родственников больных. Уход за пациентами с ЛВД, и особенно с поведенческими нарушениями, может потребовать более тщательного наблюдения для предотвращения злоупотребления алкоголем, чрезмерного увеличения массы тела вследствие нарушений пищевого поведения, а также возможных соматических осложнений из-за опасного размещения во рту несъедобных предметов и веществ. Неправильная оценка ситуации и импульсивность пациентов с ЛВД приводит к необходимости ограничивать их доступ к банковским счетам, чтобы предотвратить финансовое мошенничество или совершение неосторожных покупок. Такие поведенческие нарушения у пациентов с ЛВД, как отсутствие эмпатии и межличностного общения, могут быть особенно сложными для осуществляющих уход, поскольку эти симптомы могут усилить чувство изоляции. Социальная поддержка родственников и других ухаживающих очень важна. Ассоциация для пациентов с ЛВД (www.theaftd.org) и их родственников, созданная в 2005 г., предлагает помощь всем нуждающимся в получении информации о заболевании ЛВД, продвигает и финансирует исследования в области диагностики, лечения и ухода, а также занимается оказанием различных видов помощи: юридической, социальной, просветительской и образовательной. И хотя сайт ассоциации ориентирован на англоязычное население, ознакомление с его деятельностью, возможно, будет полезно и в нашей стране.