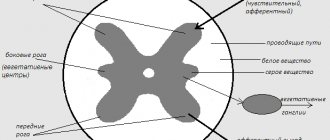
Диагностика
Для определения рассеянного склероза врачи используют методы опроса и неврологического осмотра, а затем подтверждают диагноз МРТ-исследованием и анализами. На МРТ изучают головной и спинной мозг на наличие старых и новых очагов поражения. Для лучшей визуализации свежих бляшек применяют контраст. Диагноз ставится, если у пациента обнаружили 4 и более очага демиелинизации размером не меньше 3 мм, либо 3 очага рядом с боковыми желудочками, в стволе мозга, мозжечке или спинном мозге.
Кроме МРТ при рассеянном склерозе могут назначать:
- регулярные анализы крови для определения уровня иммуноглобулинов в ликворе;
- люмбальные пункции для изучения состава жидкости спинного мозга.
Как остановить рассеянный склероз: лечение разных форм заболевания
К сожалению, несмотря на прогресс в терапии РС, окончательно победить болезнь пока не представляется возможным. Тем не менее, если у человека рассеянный склероз, лечение может помочь уменьшить проявление симптомов и снизить число рецидивов. Терапия назначается в зависимости от тяжести болезни.
При прогрессирующих формах РС лечение может помочь снизить тяжесть заболевания. Специалисты могут назначать:
- плазмоферез — очистку крови пациента;
- иммуносупрессоры — препараты искусственного угнетения иммунитета;
- иммуномодуляторы — лекарства, регулирующие иммунный ответ организма.
Для предотвращения рецидивов могут использоваться В-интерфероны, а для снижения интенсивности симптоматики применяют:
- комплексы витаминов Е и В;
- ноотропы, улучшающие мозговую деятельность;
- антихолинэстеразные препараты, тормозящие активность нервной системы;
- миорелаксанты, способствующие снижению тонуса мускулатуры;
- энтеросорбенты, помогающие вывести токсины.
Реабилитация при рассеянном склерозе
- Лечебная физкультура.
ЛФК помогает улучшить состояние человека при нарушении двигательной активности. Работа на тренажерах помогает восстановить координацию движений. При верно подобранных нагрузках метод продемонстрировал отличную эффективность. - Физиотерапия.
Для пациентов с РС рекомендованы электрофорез, миостимуляция, ультразвуковое воздействие, магнитотерапия. Эти методики способствуют активизировать обменные процессы организма и снизить воспаление. - Массаж.
При рассеянном склерозе этот метод реабилитации может использоваться для снятия болевых симптомов и спазмов. Также массаж помогает улучшить тонус мышц при его снижении.
Также реабилитация при рассеянном склерозе включает психотерапию, которая поможет пациенту справиться с негативными мыслями, а также консультации диетолога.
Прогноз заболевания
Рассеянный склероз не относят к смертельным заболеваниям, неприятные симптомы РС можно достаточно успешно купировать. Ученые выяснили, что благодаря современному лечению, продолжительность жизни пациентов сегодня значительно выросла по сравнению с теми, кто заболел даже несколько десятилетий назад.
В целом люди с рассеянным склерозом живут в среднем на 7 лет меньше, чем в общей популяции. Часто снижение продолжительности жизни связано с осложнением других патологий: онкологических и сердечно-сосудистых заболеваний. У многих пациентов благодаря качественному лечению удается предотвратить снижение качества жизни и продуктивности. По данным Национального общества рассеянного склероза ⅔ людей с РС обходятся без инвалидного кресла даже спустя 20 лет после диагностирования болезни.
Инвалидность при рассеянном склерозе
| Если рассеянный склероз стал причиной нетрудоспособности на 5 месяцев и более в течение года, то пациент может обратиться для оформления инвалидности. |
После рассмотрения документов комиссия вынесет решение о нетрудоспособности, что дает право на получение пенсии и льготных условий труда. На установление группы инвалидности влияют:
- срок, на который была утрачена трудоспособность;
- срок, когда пациент был поставлен на учет с данным заболеванием;
- частота, продолжительность и тяжесть обострений;
- результаты терапии;
- изменения в течении заболевания, скорость развитие симптомов.
Инвалидность назначается на год, после чего необходимо пройти комиссию снова. Инвалидность I и II групп при РС дает право на сокращенный рабочий день — 35 часов в неделю. При этом заработная плата выплачивается в полном объеме.
Постинсультная депрессия
Современная медицина в снижении смертности и инвалидизации от инсульта видит важную роль в первичной, вторичной профилактике и также в эффективной реабилитации после инсульта, где участие самого пациента трудно переоценить. Комплекс мероприятий, направленных на уменьшение степени инвалидизации перенесших инсульт пациентов, предполагает и борьбу с депрессией (постинсультная депрессия, ПД), возникающей в постинсультном периоде.
А она возникает практически у каждого третьего пациента (в 33% случаев), выжившего после острого нарушения мозгового кровообращения, через 3‒6 месяцев.2 И о ее негативном влиянии на процесс реабилитации, здоровье пациентов, качество их жизни врач не должен забывать. Тем более есть данные, что ПД провоцирует манифестации сопутствующих психических заболеваний (в том числе тревожные расстройства), значительно ухудшает прогноз выживаемости. У пациентов с симптомами ПД смертность в течение 15 месяцев после инсульта в 8 раз выше, чем у больных без ее признаков, и в 3,5 – в течение 10 лет после события.3,4
Клинические проявления
У пациентов, перенесших инсульт, наблюдается, как правило, депрессия легкой степени выраженности – 77%, реже (20%) – средней степени тяжести («малая депрессия»), «большая депрессия» (тяжелая форма) отмечается не чаще чем в 3% случаев.5 ПД у около половины больных длится более полугода, при этом ее длительность зависит от локализации инсульта (полгода – симптоматика сохраняется у подавляющего большинства пациентов с инсультом в бассейне средней мозговой артерии, гораздо меньше – с очагом в вертебробазилярном бассейне).5
При легкой (или умеренной) степени депрессивных расстройств жалобы пациента нередко слабо представлены или скрыты за мотивационными (нарушения сна и/или аппетита), соматическими (хроническая боль) и вегетативными проявлениями, не воспринимаемыми больным как депрессивные, что серьезно затрудняет диагностику.
При более тяжелой степени расстройств пациенты чаще всего страдают от колебаний настроения, усталости, нарушений сна, раздражительности, страха или апатии. В то же время такие проявления, как ангедония, пессимизм, суицидальные мысли или дефицит внимания, как правило, встречаются при большом депрессивном расстройстве и не характерны для ПД.
Важно: у пациента, перенесшего инсульт, трудно определить, являются ли симптомы астении и апатии следствием депрессии или постинсультного неврологического дефицита. Но игнорировать ПД нельзя, т. к. она значительно снижает физическую активность и качество жизни пациента,6 а также существенно увеличивает риск самоубийства.7 Это состояние негативно влияет на мотивацию пациента принимать лечение, снижает его приверженность лечению, приводит к увеличению физической нетрудоспособности, плохому функциональному результату, что в итоге повышает вероятность повторного инсульта и определяет более высокую смертность. Являясь плохим прогностическим признаком, ПД требует своевременной диагностики и лечения, имеющих жизненно важное значение для восстановления и прогнозирования у выживших после инсульта.
Диагностика
Диагностировать депрессивные расстройства после инсульта достаточно сложно: контакт с больным затруднен из-за афазии; печаль на его лице – из-за слабости лицевой мускулатуры; плач – может быть связан с псевдобульбарным параличом; апатия – вызвана поражением правого полушария и пр.
Диагностические критерии ПД:8
Три (или более) из следующих симптомов присутствовали в течение недели и представляют собой изменение по сравнению с предыдущим функционированием:
- Пациент не общается (например, избегает говорить) большую часть дня, каждый день или большую часть недели.
- Усталость каждый день или большую часть недели.
- Подавленное настроение, сохраняющееся большую часть дня, каждый день или большую часть недели, на что указывают либо жалобы пациента, либо наблюдения других людей (например, он чувствует печаль, легко плачет).
- Инсомния, раннее пробуждение или гиперсомния каждый день или большую часть недели.
- Чувство беспомощности, бесполезности большую часть дня, каждый день или большую часть недели.
- Периодические мысли о смерти (а не просто страх смерти), периодические мысли о самоубийстве без определенного плана, попытка самоубийства или конкретный план его совершения.
- Чувство безнадежности или отчаяния (особенно в связи с инсультом) большую часть дня, каждый день или большую часть недели.
- Необоснованная раздражительность каждый день или большую часть недели.
Симптомы вызывают клинически значимые расстройства или нарушения в социальном взаимодействии, роде занятий или других важных областях функционирования. Возникновение, развитие и продолжительность этих симптомов тесно связаны с цереброваскулярным заболеванием. Возникновение тяжелого депрессивного эпизода не может быть проявлением расстройства адаптации с депрессивным настроением, шизоаффективным расстройством, шизофренией, бредовым расстройством или другими уточненными или неуточненными спектрами шизофрении или другими психическими расстройствами. Нет маниакального или гипоманиакального эпизода.
Важно провести скрининг депрессивных симптомов в острой фазе инсульта (в течение 1-го месяца) и по возможности записать время начала, характеристики, тяжесть и сопутствующие психологические и соматические симптомы депрессии. Принимая во внимание тесную взаимосвязь между постинсультной депрессией и инсультом, также важна общая оценка инсульта, включая его тип, местоположение, размер, тяжесть и функциональное состояние пациента.
В существующей МКБ-10 нет диагноза «постинсультная депрессия». В настоящее время у врача не психиатра нет возможности использования психиатрических кодов, поэтому этот диагноз всегда будет идти как осложнение перенесенного инсульта.
Факторы, увеличивающие риск ПД:
- старший возраст;9
- нетрудоспособность и изменение статуса в обществе и семье после перенесенного инсульта;10
- негативные жизненные события;11
- отсутствие социальной поддержки, низкий доход семьи;12
- личностные преморбидные невротические расстройства и тип поведения А («трудоголики», перфекционисты);13
- семейный наследственный анамнез по депрессии.14
Инсульты в анамнезе, а также депрессии и другие психические расстройства – все это важные предикторы ПД. Необходима также оценка факторов сердечно-сосудистого риска, так как гипертония и стенокардия являются независимыми предикторами ПД.15,16 Двигательная инвалидность – наиболее тяжелое последствие инсульта.
Для оценки неврологического дефицита рекомендуются:
- NIHSS;17
- модифицированная шкала Ранкина (mRS);18
- индекс Бартела (BI).19
Оценка депрессивных проявлений может производиться как с помощью самооценочных шкал, так и при врачебной оценке.
Среди самооценочных шкал в России наиболее популярны:
- Опросник депрессии Бека (BDI).20
- Госпитальная шкала тревоги и депрессии (HADS).20
- Шкала центра эпидемиологических исследований.21
Дифференциальная диагностика
Постинсультная апатия. Дифференциальная диагностика достаточно трудна, но можно опираться на клинические особенности эмоциональных проявлений и выражение лица. Апатия сопровождается снижением когнитивной функции и нарушениями поведения, в то время как ПД будет проявляться тревогой, возбуждением и раздражительностью. Пациенты с апатией равнодушны, имеют нейтральное настроение и обычно не испытывают суицидальные мысли.22,23 В то время как люди с ПД показывают явно негативное настроение. Что касается выражения лица, то у апатичных пациентов часто наблюдается плоский аффект и отсутствие зрительного контакта, а для большинства людей с депрессией характерно выражение грусти с эмоциями в глазах.23
Постинсультная тревога. Обычно наблюдается спустя месяц после перенесенного ОНМК, причем ее частота увеличивается со временем.24 У большинства пациентов ПД возникает в острой стадии (в первые 30 суток), ее возникновение слабо связано с предшествующей в анамнезе депрессией, но довольно сильно зависит от самого инсульта. Постинсультная тревога тесно связана с предшествующей тревогой.24 У пациентов с ПД преобладают постоянное подавленное настроение и потеря интереса, сопровождаемые соматическими или психическими расстройствами, такими как беспокойство, напряжение и сердцебиение. У пациентов с постинсультной тревогой присутствуют страх, напряжение, беспокойство, раздражительность или беспокойство.25
Постинсультная астения. Это субъективное чувство физической или умственной усталости и недостатка энергии. Оно не зависит от физических упражнений или предыдущей активности, приводит к затруднению поддержания даже рутинных действий. При ПД тоже могут иметь место усталость и потеря энергии, но при этом будет также подавленное настроение.26
Постинсультное психотическое расстройство. Может встречаться на разных стадиях инсульта и реабилитации. Этот симптомокомплекс включает галлюцинации, заблуждение и делирий, которые препятствуют функциональному исходу и качеству жизни, а также является неблагоприятным по прогнозу развития деменции.27
Диагностика ПД, как уже сказано, требует от специалиста серьезного подхода и высокой квалификации. Это касается и выбора диагностического инструмента (шкала, опросник, консультация психиатра) и приверженности диагностировать депрессию врачами неврологического или реабилитационного отделения. Немаловажно, что у пациентов с инсультом часто присутствуют афазия, агнозия и нарушения познавательной способности, которые увеличивают сложность распознавания и диагностику ПД.14,28
Комплексная терапия пациентов с ПД
В комплексной терапии ПД применяются различные средства и методы, доказавшие свою эффективность: антидепрессанты, психостимуляторы, электросудорожная терапия (при лекарственной непереносимости и тяжелой, рефрактерной к лечению депрессии), транскраниальная магнитная стимуляция, когнитивно-поведенческая психотерапия.4
Медикаментозная терапия. Препараты первой линии выбора – антидепрессанты, их применение наиболее оправдано патогенетически. Они не только помогают избавиться от депрессии, улучшить эмоциональное состояние и когнитивные функции, но и оказывают положительное влияние на неврологический исход и долгосрочный прогноз.4
Лечение антидепрессантами следует начинать, как только у выживших после инсульта будет диагностирована ПД. Выбор антидепрессанта зависит от симптомов депрессии у пациента, побочных эффектов, особенно у пожилых людей, и взаимодействия с другими препаратами. Клиницистам следует внимательно наблюдать и оценивать реакцию на терапию, особенно в ее начале, из-за возможных нежелательных явлений. Следует иметь в виду, что также существует риск развития маниакального приступа во время лечения. Если это происходит, дозу антидепрессанта следует уменьшить или немедленно прекратить и заменить антиконвульсантом или нейролептиком.29 Через 2‒3 месяца после исчезновения депрессивных симптомов терапия может быть закончена.30
Физиотерапия. Эффективным и безопасным методом лечения для пациентов с рефрактерным PSD может быть транскраниальная магнитная стимуляция (мТМС).31 Однако побочные эффекты (головные боли, желудочно-кишечные реакции, сухость во рту, шум в ушах, судороги) ограничивают широкое применение этого метода.32
Психотерапия и когнитивно-поведенческая терапия (КПТ). Эффективны и помогают социализировать пациентов при лечении легкой и умеренной депрессии.33,34
Ранняя профилактика
Ранняя профилактика может снизить частоту возникновения ПД и стимулировать эффективное восстановление неврологической функции.35 Профилактическое применение как антидепрессантов, особенно СИОЗС, так и психотерапии снижают риск возникновения ПД, улучшают повседневную активность и когнитивную функцию, а также снижают смертность пациентов с инсультом, тем самым улучшают прогноз у пациентов, перенесших инсульт.36,37
Уход за больными
Он очень важен для пациентов с ПД и в острой фазе, и в фазе выздоровления.38 Важна и психологическая поддержка – необходимо помочь пациентам адаптироваться к новому состоянию, обеспечить комфортные условия для сна, чтобы обеспечить адекватный отдых.39 Физические упражнения могут улучшить эмоциональное и физическое функционирование пациентов, тем самым повысить качество их жизни.40
Таким образом, ПД является частым явлением у выживших после инсульта пациентов и серьезно влияет на физические и когнитивные исходы. Своевременная диагностика позволяет распознать лиц с высоким риском ПД. Выбор лечения зависит от характеристик пациента и общего состояния, тяжести симптомов и побочных эффектов. Раннее включение в терапию антидепрессантов способствует как физическому, так и когнитивному восстановлению после инсульта и может увеличить выживаемость после инсульта в долгосрочной перспективе.14,28
К сожалению, очень часто ПД остается нераспознанным, и только в небольшом числе случаев (около 10%) пациенты с этим состоянием получают адекватное лечение. Поэтому особенно важно, чтобы врачи были осведомлены о ПД и умели своевременно распознавать это состояние и правильно помогать своим пациентам и их близким.
Литература
1Каерова Е.В., Журавская Н.С., Матвеева Л.В., Шестёра А.А. Анализ основных факторов риска развития инсульта // Современные проблемы науки и образования. № 6, 2021. URL: https://www.science-education.ru/ru/article/view?id=27342
2Hackett M.L., Pickles K. Part I: frequency of depression after stroke: an updated systematic review and meta-analysis of observational studies. Int J Stroke. 2014 (Dec.), 9 (8), p. 1017‒25.
3Каннер А.М. Депрессия при неврологических заболеваниях. М.: Литтерра, 2007, 159 с.
4Вознесенская Т.Г. Депрессия при цереброваскулярных заболеваниях // Неврол. нейропсихиатр и психосом. № 2, 2009, с. 9‒13.
5Скворцова В.И., Губский Л.В., Стаховская Л.В. и др. Ишемический инсульт / В кн.: Неврология: национальное руководство. Под ред. Е.И. Гусева, А.И. Коновалова, В.И. Скворцовой. М.: ГЭОТАР-Медиа, 2009, с. 593‒615.
6Jiao J.T., Cheng C., Ma Y.J., Huang J., Dai M.C., Jiang C., Wang C., Shao J.F. Association between inflammatory cytokines and the risk of post-stroke depression, and the effect of depression on outcomes of patients with ischemic stroke in a 2-year prospective study. Exp Ther Med. 2021 (Sep.), 12 (3), p. 1591‒1598.
7Pompili M., Venturini P., Campi S., Seretti M.E., Montebovi F. et al. Do stroke patients have an increased risk of developing suicidal ideation or dying by suicide? An overview of the current literature. CNS Neurosci Ther. 2012 (Sep.), 18 (9), p. 711‒721.
8Fu-ying Zhao, Ying-ying Yue, Lei Li, Sen-yang Lang et al. Clinical practice guidelines for post-stroke depression in China. Braz J. Psychiatry. 2021, 40 (3), p. 325‒334.
9Verdelho A., Hénon H., Lebert F., Pasquier F., Leys D. Depressive symptoms after stroke and relationship with dementia: A three-year follow-up study. Neurology. 2004, (Mar. 23), 62 (6), p. 905‒911.
10Göthe F., Enache D., Wahlund L.O., Winblad B., Crisby M., Lökk J., Aarsland D. Cerebrovascular diseases and depression: epidemiology, mechanisms and treatment. Panminerva Med. 2012 (Sep.), 54 (3), p. 161‒170.
11Tang W.K., Chan S.S., Chiu H.F., Ungvari G.S., Wong K.S. et al. Poststroke depression in Chinese patients: frequency, psychosocial, clinical, and radiological determinants. J. Geriatr Psychiatry Neurol. 2005 (Mar.), 18 (1), p. 45‒51.
12Townend B.S., Whyte S., Desborough T., Crimmins D., Markus R. et al. Longitudinal prevalence and determinants of early mood disorder post-stroke. J. Clin Neurosci. 2007 (May.), 14 (5), p. 429‒34.
13Storor D.L., Byrne G.J. Pre-morbid personality and depression following stroke. Int Psychogeriatr. 2006 (Sep.), 18 (3), p. 457‒69.
14Hackett M.L., Yapa C., Parag V., Anderson C.S. Frequency of depression after stroke: a systematic review of observational studies. Stroke. 2005 (Jun.), 36 (6), p. 1330‒40.
15de Man-van Ginkel J.M., Hafsteinsdottir T.B., Lindeman E. et al. In-hospital risk prediction for post-stroke depression: development and validation of the post-stroke depression prediction scale. Stroke. 2013, 44, p. 2441‒2445.
16Jiang X.G., Lin Y., Li Y.S. Correlative study on risk factors of depression among acute stroke patients. Eur Rev. Med Pharmacol. Sci. 2014,18, p. 1315‒1323.
17Brott T., Adams H.P., Jr., Olinger C.P., Marler J.R., Barsan W.G. et al. Measurements of acute cerebral infarction: a clinical examination scale. Stroke. 1989, 20, p. 864‒870.
18Rankin J. Cerebral vascular accidents in patients over the age of 60. II. Prognosis. Scott Med J. 1957, 2, p. 200‒15.
19Mahoney F.I., Barthel D.W. Functional evaluation: the Barthel index. Md State Med J. 1965, 14, p. 61‒65.
20Beck A.T., Ward C.H., Mendelson M., Mock J. An inventory for measuring depression. Erbaugh J. Arch Gen Psychiatry. 1961 Jun; 4, p. 561‒571.
21Radloff L.S. The CES-D Scale: a self-report depression scale for reseach in the general population. Appl Psychol Meas 1977, 1, p. 385‒401.
22Withall A., Brodaty H., Altendorf A., Sachdev P.S. A longitudinal study examining the independence of apathy and depression after stroke: the Sydney stroke study. Int Psychogeriatr. 2011, 23, p. 264‒273.
23Ishizaki J., Mimura M. Dysthymia and apathy: diagnosis and treatment. Depress Res Treat. 2011, 2011, p. 893‒905.
24Campbell Burton C.A., Murray J., Holmes J., Astin F., Greenwood D., Knapp P. Frequency of anxiety after stroke: a systematic review and meta-analysis of observational studies. Int J Stroke. 2013, 8, p. 545‒559.
25Schöttke H., Giabbiconi C.M. Post-stroke depression and post-stroke anxiety: prevalence and predictors. Int. Psychogeriatr. 2015, 27, p. 1805‒1812.
26Staub F., Bogousslavsky J. Fatigue after stroke: a major but neglected issue. Cerebrovasc Dis. 2001, 12, p. 75–81.
27Almeida O.P., Xiao J. Mortality associated with incident mental health disorders after stroke. Aust N Z J Psychiatry. 2007, 41, p. 274‒281.
28Chemerinski E., Robinson R.G. The neuropsychiatry of stroke. Psychosomatics. 2000 (Jan.-Feb.), 41 (1), p. 5‒14.
29Xu X.M., Zou D.Z., Shen L.Y., Liu Y, Zhou X.Y. et al. Efficacy and feasibility of antidepressant treatment in patients with post-stroke depression. Medicine (Baltimore). 2021, 95, e5349.
30Hebert D., Lindsay M.P., McIntyre A., Kirton A. et al. Canadian stroke best practice recommendations: stroke rehabilitation practice guidelines, update 2015. Int. J. Stroke. 2016, 11, p. 459‒84.
31Jorge R.E., Robinson R.G., Tateno A., Narushima K. et al. Repetitive transcranial magnetic stimulation as treatment of poststroke depression: a preliminary study. Biol. Psychiatry. 2004, 55, p. 398‒405.
32Shen X., Liu M., Cheng Y., Jia C., Pan X. et al. Repetitive transcranial magnetic stimulation for the treatment of post-stroke depression: a systematic review and meta-analysis of randomized controlled clinical trials. J. Affect Disord. 2021, 211, p. 65‒74.
33Friedland J.F., McColl M. Social support intervention after stroke: results of a randomized trial. Arch Phys Med Rehabil. 1992, 73, p. 573‒581.
34Nicholl C.R., Lincoln N.B., Muncaster K., Thomas S. Cognitions and post-stroke depression. Br J. Clin. Psychol. 2002, 41, p. 221‒231.
35Wang F. The influence of early prevention of post-stroke depression on the rehabilitation of patients with acute stroke. Chin J. Mod Drug Appl. 2013. 7, p. 98‒99.
36Flaster M., Sharma A., Rao M. Poststroke depression: a review emphasizing the role of prophylactic treatment and synergy with treatment for motor recovery. Top Stroke Rehabil. 2013, 20, p. 139‒150.
37Ramasubbu R. Therapy for prevention of post-stroke depression. Expert Opin Pharmacother. 2011, 12, p. 2177‒2187.
38Clark P.C., Dunbar S.B., Aycock D.M., Courtney E., Wolf S.L. Caregiver perspectives of memory and behavior changes in stroke survivors. Rehabil Nurs. 2006, 31, p. 26‒32.
39Harris A.L., Elder J., Schiff N.D., Victor J.D., Goldfine A.M. Post-stroke apathy and hypersomnia lead to worse outcomes from acute rehabilitation. Transl Stroke Res. 2014, 5, p. 292–300.
40Kang J.H., Park R.Y., Lee S.J., Kim J.Y., Yoon S.R., Jung K.I. The effect of bedside exercise program on stroke patients with dysphagia. Ann Rehabil Med. 2012, 36, p. 512–20.