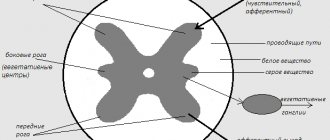
Рецидивирующе-ремиттирующий рассеянный склероз
Рецидивирующе-ремиттирующий рассеянный склероз (РРРС) — это наиболее распространенный тип рассеянного склероза (РС). Такой диагноз ставится примерно в 85% случаев [1]. Так же, как и другие типы заболевания, РРРС возникает, когда иммунная система организма атакует центральную нервную систему, повреждая защищающий нервные волокна белок миелин.
Течение болезни сопровождается различными неврологическими симптомами, такими как [2]:
- повышенная утомляемость;
- нарушения походки;
- зрительные и глазодвигательные расстройства;
- снижение мышечной силы конечностей;
- расстройства чувствительности, мочеиспускания и т.д.
Симптомы могут значительно варьироваться в зависимости от локализации поврежденных нервных волокон.
Рецидивы РРРС длятся не менее 24 часов. В период рецидива все симптомы усиливаются, однако вскоре наступает ремиссия, во время которой симптомы частично или полностью проходят.
Интересный факт
Причины развития рецидивирующе-ремиттирующего рассеянного склероза, как и других типов РС, на данный момент не выяснены. Вероятнее всего, причины кроются в совместном влиянии генетических факторов и факторов окружающей среды (курения, дефицита витамина D, некоторых инфекционных заболеваний) [3].
Для диагностики РРРС используется множество различных методов [4], однако специфических тестов на этот тип заболевания пока нет. Врач-невролог назначит вам комплексное обследование для оценки тяжести заболевания, определения типа течения РС и назначения терапии. Также будет необходимо провести несколько диагностических тестов, среди которых — метод магнитно-резонансной томографии (МРТ). МРТ позволит найти очаги повреждений в головном и спинном мозге, которые позволят предположить наличие РС. В некоторых случаях необходим забор спинномозговой жидкости (люмбальная пункция).
На данный момент не существует лекарства, которое позволило бы полностью и навсегда избавиться от симптомов любого типа рассеянного склероза. Однако существуют различные лекарственные средства, позволяющие контролировать течение заболевания. Также не следует забывать о поддержании физической активности, которая позволит помочь с проблемами подвижности или справиться с мышечной слабостью. Индивидуально подобранная программа упражнений помогает улучшить физическую форму и качество жизни, не вызывая обострения симптомов заболевания или рецидива [5].
Интересный факт
Основу терапии составляют препараты, изменяющие течение РС (ПИТРС). Эти препараты воздействуют на сам патологический процесс — демиелинизацию — и позволяют сократить частоту или даже полностью предотвратить возникновение рецидивов [6].
На рынке существует множество различных лекарственных препаратов, однако необходимо иметь в виду, что подбор терапии строго индивидуален и осуществляется исключительно врачом на основании характера течения заболевания, уже имеющихся заболеваний, а также с учетом ранее назначенной терапии.
Прогноз для пациентов с рецидивирующе-ремиттирующим рассеянным склерозом, как правило, более благоприятный, чем для пациентов с прогрессирующей формой заболевания [7], но течение заболевания необходимо оценивать в динамике, так как поражения нервной ткани со временем накапливаются. Примерно у двух третей пациентов с рецидивирующе-ремиттирующим рассеянным склерозом развивается вторичный прогрессирующий РС [8]. В среднем это происходит через 15-20 лет после начала заболевания [9]. Именно это прогрессирование является важным фактором в прогнозировании возможности развития нетрудоспособности [10].
Несмотря на многолетнее изучение рассеянного склероза (РС), эта проблема остается весьма актуальной. Ее медицинская и социальная значимость обусловлена высокой частотой болезни, поражением лиц молодого трудоспособного возраста с относительно быстрой инвалидизацией при недостаточной эффективности в ряде случаев существующих терапевтических средств.
Благодаря значительному прогрессу в понимании механизмов развития патологического процесса при РС, а также биотехнологическим методам создания новых лекарственных средств и наличию унифицированных критериев для своевременной постановки диагноза РС стало возможным раннее назначение специфического патогенетического лечения, направленного как на купирование симптомов экзацербации, так и на модулирование течения болезни.
В настоящее время при РС общепринятыми являются диагностические критерии, предложенные W. McDonald и соавт. в 2001 г., уточненные в 2005 г., а затем пересмотренные в 2010 г. [48] (см. таблицу).
При ранних клинических проявлениях заболевания, когда еще нет типичного ремиттирующего течения, важным является исключение альтернативных диагнозов [8].
Различные комбинации неврологических симптомов и данных МРТ могут наблюдаться у пациентов при клинически изолированном синдроме (КИС), который в настоящее время определяется как монофазно развившаяся симптоматика, вызванная, предположительно, воспалительным демиелинизирующим заболеванием. При этом монофазность подразумевает впервые развившийся отдельный клинический эпизод с относительно быстрым началом. Возможно одновременное выявление множественных клинических/параклинических проявлений, однако диссеминация во времени не должна быть очевидной. В связи с этим в современной классификации КИС выделяются следующие варианты: тип 1 – клинически монофокальный, по меньшей мере 1 асимптомный МРТ-очаг; тип 2 – клинически мультифокальный, по меньшей мере 1 асимптомный МРТ-очаг; тип 3 – клинически монофокальный; МРТ может быть без патологии; нет асимптомных МРТ-очагов; тип 4 – клинически мультифокальный; МРТ может быть без патологии; нет асимптомных МРТ-очагов; тип 5 – нет клинических проявлений демиелинизирующего заболевания, но есть изменения на МРТ, дающие основания предполагать наличие КИС [42].
Учитывая значительные трудности при постановке диагноза РС в атипичных случаях, в Научном центре неврологии РАМН было проведено клинико-морфологическое исследование при псевдотуморозном течении РС и острой очаговой демиелинизации. Наблюдали 43 пациента, 32 больным из которых диагноз был уточнен на основании гистологического исследования операционного материала, полученного в ходе стереотаксической биопсии или оперативного вмешательства. Были выделены группы с псевдотуморозным моноочаговым процессом; с сочетанием псевдотуморозного очага с субклинической многоочаговой демиелинизацией; с развитием псевдотуморозного течения при обострении достоверного РС; 11 пациентам диагноз был поставлен в результате проведения комплексного исследования и динамического наблюдения.
Оказалось возможным выделить следующие клинические особенности псевдотуморозного течения
демиелинизирующего процесса: типичный для РС возраст начала болезни, одинаковая частота заболевания у мужчин и женщин, преимущественно полушарная локализация псевдотуморозного очага с подострым течением заболевания. При морфологическом исследовании биопсийного и операционного материала были выявлены изменения ткани мозга, характерные для острого очагового демиелинизирующего процесса, основными признаками которого являются деструкция миелиновых волокон белого вещества с уборкой продуктов их распада липофагами, пролиферация и гипертрофия астроцитов, продуцирующих глиальные волокна, воспалительные периваскулярные инфильтраты, состоящие из лимфоцитов, моноцитов и немногочисленных плазматических клеток, гиперемия мелких сосудов и капилляров, отек ткани мозга. Установлено, что распад аксонов в очаге демиелинизации возникает уже на самых ранних этапах развития демиелинизирующего заболевания. Полученные данные позволили уточнить алгоритм обследования больных с псевдотуморозным типом течения патологического процесса и определенные подходы в тактике ведения данных пациентов. Так, при выявлении неоднозначных данных КТ и МРТ в дебюте псевдотуморозного демиелинизирующего заболевания рекомендовано дополнительное комплексное обследование пациента, включая выполнение высокопольной МРТ головного мозга, шейного, грудного отделов позвоночника, регистрацию вызванных потенциалов мозга для исключения «диссеминации патологического процесса в пространстве». В случае развития псевдотуморозного варианта течения болезни в рамках КИС при многоочаговом поражении мозга или при достоверном РС целесообразно проведение пульс-терапии метилпреднизолоном, и в случае отсутствия реакции на данное лечение показана биопсия. Несмотря на то что стереотаксическая операция с целью получения биопсии имеет важное диагностическое значение при выявлении псевдотуморозного очага, расширение возможностей обследования данных больных позволяет избежать в ряде случаев ее проведения.
Еще одним атипичным симптомом при РС, как считалось ранее, являются слуховые нарушения. В ходе проведенного анализа кохлеарных нарушений при РС были обследованы 70 пациентов, из которых у 35 отмечались жалобы на снижение слуха; контрольную группу составили 18 человек.
Клиническими особенностями слуховых нарушений при РС являлся широкий диапазон жалоб, которые варьировали от явлений раздражения, таких как заложенность, шум в ухе, гиперакузия, до явлений выпадения, вплоть до остро возникшей односторонней глухоты. Обращал на себя внимание разнообразный спектр слуховых жалоб: появление слуховых нарушений то с одной, то с другой стороны, сочетание снижения слуха с головокружением, шумом в ухе, а также появление слуховых нарушений в дебюте или при обострении заболевания. Иногда пациенты указывали на какие-либо нарушения слуха только лишь при акцентированном расспросе. Проведенное комплексное аудилогическое обследование позволило исключить кондуктивную форму тугоухости у большинства обследованных пациентов с РС. Так, по результатам аудиометрии, как тональной пороговой, так и в расширенном диапазоне частот – высокочастотной аудиометии, у пациентов с РС с кохлеарными жалобами на стороне хуже слышащего уха и на противоположной стороне, а также в группе пациентов без подобных жалоб выявлено повышение порога восприятия звука на всех частотах по сравнению с контрольной группой, однако более выраженное повышение порогов воздушной проводимости отмечено для высоких частот, что характерно для нейросенсорной тугоухости. Кроме того, при тимпанометрии, оценивающей акустический импеданс среднего уха, получены результаты, свидетельствующие об отсутствии патологии среднего уха и нормальном функционировании слуховой трубы. Наконец, при акустической рефлексометрии, которая является ценным диагностическим тестом для топической диагностики нарушений слуха (в частности, дает возможность разграничения кохлеарных и ретрокохлеарных нарушений) при РС, зафиксировано значительное повышение абсолютных и относительных порогов акустического рефлекса, а также частое его выпадение, что является характерным для ретрокохлеарного поражения. Важно отметить, что при акустической рефлексометрии как у пациентов с жалобами на нарушение слуха, так и у пациентов с РС с головокружением выявлены признаки одно-/двустороннего поражения слухового нерва и слуховых центров продолговатого мозга и моста, более типичное для пациентов с кохлеарными нарушениями. Полученные данные, с одной стороны, подтверждают чувствительность акустической рефлексометрии при выявлении патологии слухового нерва при РС, а с другой стороны, указывают на высокую частоту вовлечения в патологический процесс не только центральных структур, но и ретрокохлеарного неврального поражения даже у пациентов без слуховых нарушений; при этом отмечается существенная роль подобного сочетанного поражения в развитии кохлеарных нарушений при РС. В связи с представленными данным с практической точки зрения важно подчеркнуть, что при обращении к отоларингологам пациентов с жалобами на снижение слуха при выявлении сенсоневральной тугоухости неясного генеза при проведении дифференциальной диагностики необходимо учитывать возможность демиелинизирующего характера процесса, поскольку своевременные постановка диагноза РС и выявление признаков его активности имеют принципиальное значение для адекватной терапии.
В последние годы в связи с достаточно большим выбором препаратов, модулирующих течение РС, и необходимостью их индивидуального назначения подходы к патогенетической терапии РС претерпевают определенные изменения. Предлагается целый ряд терапевтических алгоритмов. Обсуждаются эскалационный (возрастающий) и индукционный подходы: эскалационная схема предполагает начало лечения с более безопасных препаратов с переходом в случае их неэффективности к более агрессивным методам; индукционный подход подразумевает первоначально более агрессивное влияние на иммунную систему, однако использование данного вида терапии может быть ограничено возможностью развития целого спектра побочных эффектов [17, 24].
Одной из групп, работающих в области лечения РС, — Multiple Sclerosis Treatment Consensus Group (MSTCG) — предложена интегрированная схема, основанная на разделении базовой и эскалационной терапии [56]. Согласно данному алгоритму, первоначально необходимо соответствующее лечение обострения с последующим максимально ранним назначением иммуномодуляторов первой линии. При недостаточно эффективном контроле активности болезни необходима эскалация в сторону более интенсивной терапии.
В настоящее время к основным препаратам первой линии относят глатирамера ацетат и интерфероны β (ИФН β). При неэффективности лечения или плохой переносимости возможны переводы больных с одного из этих классов препаратов на другой или на натализумаб, финголимод или кладрибин. Однако при определенных обстоятельствах, в частности при исходно высокоактивном течении РС, терапия может быть начата одним из трех последних препаратов. Согласно рекомендациям MSTCG, необходимо динамическое наблюдение за пациентами, включающее как клиническую оценку, так и ряд лабораторных и инструментальных обследований.
Как уже указывалось, к модулирующим течение РС препаратам первой линии относятся ИФН β и глатирамера ацетат (копаксон). В настоящее время в России зарегистрированы следующие препараты ИФН β: ИФН β-1а для подкожного введения (ребиф, генфаксон); ИФН β-1а для внутримышечного введения (авонекс, синновекс); ИФН β-1b (бетаферон, экставиа, ронбетал), которые отличаются между собой по источнику получения, химической структуре, а также по способу и частоте введения.
Терапевтические эффекты ИФН β, предположительно связаны с влиянием на презентирование антигенов и угнетением пролиферации и активации воспалительных клеток; угнетением продукции провоспалительных цитокинов и изменением цитокинового профиля в сторону противовоспалительного фенотипа; а также уменьшением поступления лейкоцитов в центральную нервную систему через гематоэнцефалический барьер за счет влияния на молекулы адгезии, хемокины и матриксные металлопротеиназы [14, 35, 57]. Вследствие вышеперечисленного уменьшается поражение проводниковых систем ЦНС и нейронов. Кроме того, ИФН β индуцирует синтез фактора роста нервов астроцитами [11], а также усиливает секрецию данного нейротрофина эндотелиальными клетками при их взаимодействии с Т-лимфоцитами (т.е. на уровне гематоэнцефалического барьера), что также определяет его иммуномодулирующее влияние и, возможно, обусловливает непосредственное воздействие на нейроны [10].
Механизмы действия глатирамера ацетата включают конкурентное с основным белком миелина связывание с молекулой II класса главного комплекса гистосовместимости, участвующей в презентировании антигенов, а также активацию Th2-фенотипа CD4+ Т-клеток, проникающих через гематоэнцефалический барьер и секретирующих противовоспалительные цитокины (интерлейкин-4, интерлейкин-10, интерлейкин-13, трансформирующий фактор роста-β), что приводит к угнетению аутоиммунного ответа на множественные антигены миелина [45]. Кроме этого показано, что глатирамера ацетат-специфичные Т-клетки экспрессируют нейротрофический фактор мозгового происхождения и трансформирующий фактор роста-β [4]. Результаты, полученные на модели экспериментального аллергического энцефаломиелита, позволяют предположить, что глатирамера ацетат способствует нейрогенезу [5].
При ремиттирующем РС проведены двойные слепые плацебо-контролируемые испытания бетаферона, ребифа, авонекса и копаксона, продемонстрировавшие их положительное влияние на активность патологического процесса как по клиническим, так и по нейровизуализационным данным [31, 34, 49, 55]. Кроме этого, для ребифа и авонекса при ремиттирующем РС показано замедление прогрессирования неврологического дефицита по шкале EDSS. При исследовании эффективности копаксона и бетаферона также отмечено замедление нарастания неврологических нарушений, однако указанные изменения в данных исследованиях не были статистически значимыми.
При вторично-прогрессирующем РС проведены двойные слепые плацебо-контролируемые исследования эффективности ребифа и бетаферона, продемонстрировавшие снижение числа обострений и уменьшение выраженности иммунно-воспалительных реакций по результатам МРТ. Также при назначении бетаферона показано замедление темпов нарастания инвалидизации пациентов (по шкале EDSS) независимо от исходной степени неврологических нарушений и наличия обострений до или во время исследования [22]. При лечении ребифом отмечен меньший процент пациентов с прогрессированием симптомов при наличии обострений в течение последних 2 лет (в отличие от больных без обострений) [54].
Важно отметить, что при обобщении результатов длительной иммуномодулирующей терапии РС бетафероном, ребифом, авонексом, копаксоном получены данные, свидетельствующие об ее эффективности и безопасности.
Несмотря на противоречивые данные о роли нейтрализующих антител при терапии ИФН β, нельзя исключить снижение клинической эффективности лечения под их влиянием: было показано четкое отрицательное влияние данных антител на клинические (частота обострений) и нейровизуализационные показатели активности РС, а также на прогрессирование инвалидизации [25, 29, 53].
В связи с этим в настоящее время разработаны рекомендации EFNS по оценке антител к ИФН β и клиническому применению измерения нейтрализующих антител. В частности, тесты на нейтрализующие антитела должны выполняться через 12 и 24 мес от начала терапии; измерение нейтрализующих антител должно быть прекращено при их отсутствии в этот период, однако необходимо возобновить исследования при нарастании активности болезни; при выявлении нейтрализующих антител исследование должно быть повторно проведено через 3-6 мес; терапия ИФН β должна быть прекращена у пациентов с высокими титрами нейтрализующих антител, выявляющимися при повторном измерении, с 3-6-месячными интервалами [53].
На фоне терапии глатирамера ацетатом у большинства пациентов вырабатываются связывающие антитела к препарату, что наблюдается уже в первые 3–4 мес после начала лечения [21]. Однако эти антитела не оказывают влияния на эффективность терапии [12].
Важно отметить, что частота обнаружения таких антител отличается при лечении различными препаратами ИФН β, кроме того, они характеризуются различной иммуногенностью (титром продуцируемых нейтрализующих антител). По данным разных исследователей, при использовании авонекса отмечалась наименьшая частота встречаемости нейтрализующих антител и наименьшая иммуногенность по сравнению с другими препаратами ИФН β [28].
Необходимо подчеркнуть, что в последние годы был разработан новый состав ИФН β-1а (ребиф нового состава), в процессе производства которого не используется фетальная бычья сыворотка, а в составе отсутствует человеческий сывороточный альбумин. Подобное улучшение формулы привело к снижению иммуногенности: в исследовании ребифа нового состава продемонстрирована меньшая частота выработки нейтрализующих антител по сравнению с данными использования первоначального состава. При сопоставлении безопасности нового и первоначального составов, с одной стороны, отмечена несколько более высокая частота развития гриппоподобного синдрома, с другой стороны, существенное снижение частоты местных реакций при лечении ребифом нового состава [26].
Кроме этого, при изучении эффективности ребифа нового состава показан быстро наступающий положительный эффект в отношении МРТ-параметров, что отражает раннее благоприятное влияние нового состава, так же как и первоначального состава, на активность болезни [20].
В связи с большим выбором модулирующих течение РС препаратов первой линии достаточно актуальным является сопоставление их клинической эффективности.
В ходе проведенного в Научном центре неврологии РАМН сравнительного анализа иммуномодулирующей терапии РС за 3 года лечения 400 больных РС ИФН β-1b (бетафероном), ИФН β-1a для подкожного введения (ребифом) в дозе 22 мкг или глатирамера ацетата показана одинаково высокая эффективность исследуемых препаратов в отношении снижения числа экзацербаций как при ремиттирующем, так и при вторично-прогрессирующем РС. Продемонстрировано предупреждение нарастания выраженности неврологических нарушений при ремиттирующем РС во всех трех терапевтических группах, при вторично-прогрессирующем РС — при назначении ребифа в дозе 22 мкг и копаксона. На фоне терапии глатирамера ацетатом отмечена меньшая частота встречаемости побочных эффектов на протяжении всех 3 лет терапии по сравнению с подгруппами, получавшими лечение ИФН β [2].
Полученные данные согласуются с результатами недавно завершившихся мультицентровых исследований. Так, при сопоставлении эффективности ребифа и копаксона при ремиттирующем РС (REGARD) [41] через 96 нед терапии не выявлены отличия первично оцениваемого показателя – времени до наступления первого обострения. Вторичные критерии (количество и изменение объема активных очагов в режиме Т2 по данным МРТ, изменения объема очагов, накапливающих контрастное вещество) также не отличались между двумя терапевтическими группами. Однако у пациентов, получавших лечение ИФН β-1а, было значительно меньшее количество накапливающих контрастное вещество очагов в режиме Т1 и комбинированных уникальных активных очагов по сравнению с пациентами, лечившимися глатирамера ацетатом. Небольшое число обострений за время исследования, в отличие от ожидаемого, позволило авторам высказать предположение, что низкая активность заболевания во включенной в исследование популяции пациентов ограничила возможность выявления клинического превосходства того или иного препарата. В другом исследовании при анализе первичного критерия – риска развития обострений – за 2 года терапии также не выявлено отличий при назначении бетаферона и глатирамера ацетата [41].
Обсуждая вопросы терапии, модулирующей течение РС, необходимо отметить, что большое внимание уделяется раннему назначению подобного лечения. Так, ряд проведенных исследований показал терапевтическую эффективность бетаферона, ребифа, авонекса и глатирамера ацетата при КИС [18, 19, 32, 36].
Важной с практической точки зрения является возможность назначения данных препаратов в детском возрасте, в связи с чем необходимо подчеркнуть, что в РФ ребиф разрешен к применению с 12 лет, авонекс – с 16 лет. Препараты ИФН β-1b (бетаферон, экставиа, ронбетал) пациентам до 18 лет разрешены к применению с осторожностью. Глатирамера ацетат разрешен к применению с 18 лет[].
В 2009 г. в России зарегистрирован и разрешен к применению другой ИФН β-1b – экставиа, при этом активная субстанция экставиа и бетаферона поступает от одного производителя, таким образом, препараты абсолютно идентичны по своему составу и качеству [3]. В этом же году был зарегистрирован отечественный ИФН β – ронбетал, активным веществом в составе которого является ИФН β-1b человеческий рекомбинантный. Препарат показан для уменьшения частоты и тяжести обострений у больных с рецидивирующе-ремиттирующим течением РС для замедления темпов прогрессирования заболевания у больных с вторично-прогрессирующим течением РС.
Результаты, полученные в ходе проведенного многоцентрового проспективного рандомизированного сравнительного клинического исследования с включением пациентов с ремиттирующим и вторично-прогрессирующим (с обострениями) течением РС, показали сопоставимость данных о безопасности и переносимости оригинального препарата ИФН β-1b бетаферона и его биоаналога ронбетала, а также позволили сделать предварительное заключение об их сопоставимой эффективности [1]. Так, за 7,5 мес приема препаратов наблюдавшиеся нежелательные явления, включая отклонения лабораторных показателей, в группе, получавшей ронбетал, соответствовали таковым для оригинального препарата. Выявленное в данном исследовании статистически значимое различие частоты развития гриппоподобного синдрома между группами, проходившими терапию ронбеталом и бетафероном (значительно меньшая частота его развития выявлена в группе, получавшей ронбетал), требует уточнения в дальнейших исследованиях. Полученные данные о снижении риска развития обострений на фоне применения ронбетала соответствовала результатам многоцентровых клинических исследований по применению ИФН β. В ходе исследования статистически значимого нарастания балла по шкале EDSS не отмечено, различий средних значений EDSS между группами ни в начале исследования, ни в динамике выявлено не было. Наблюдавшаяся в данном исследовании динамика количества и объема очагов демиелинизации по данным МРТ при терапии препаратами ИФН была аналогична данным международных многоцентровых исследований.
В 2010 г. в России зарегистрированы следующие ИФН β-1а: генфаксон (для подкожного применения), а также синновекс (для внутримышечного введения); для пациентов с ремиттирующим РС зарегистрирован целый ряд препаратов с другими механизмами действия и способами введения: тизабри (натализумаб); мовектро (кладрибин); гилениа (финголимод).
Натализумаб относится к моноклональным антителам, является селективным ингибитором молекул адгезии. Он связывается с α4-субъединицей человеческого интегрина, в большом количестве экспрессирующегося на поверхности всех лейкоцитов, за исключением нейтрофилов. В частности, препарат специфически связывается с α4β1-интегрином, блокируя при этом взаимодействие с соответствующим рецептором, адгезивной молекулой клеток сосудов (VCAM-1). В связи с этим антитела к молекулам адгезии ингибируют один из основных этапов патогенеза РС – взаимодействие с эндотелиальными клетками и миграцию лимфоцитов через гематоэнцефалический барьер. Дальнейший механизм действия натализумаба может быть обусловлен прекращением воспалительных реакций в пораженных тканях путем подавления взаимодействия α4-экспрессирующих лейкоцитов с их лигандами. Таким образом, натализумаб может подавлять воспалительную активность в пораженных тканях и дальнейшее привлечение иммунных клеток к очагу воспаления. Высокая эффективность терапии натализумабом при ремиттирующем РС была продемонстрирована в рандомизированных плацебо-контролируемых исследованиях III фазы. Так, при использовании натализумаба в режиме монотерапии по сравнению с группой плацебо было показано значительное снижение среднегодовой частоты обострений, образования новых или увеличения существующих очагов на МРТ в режиме Т2 и среднего количества накапливающих контрастное вещество очагов, а также уменьшение прогрессирования заболевания [47]. Также была продемонстрирована значительно бoльшая эффективность комбинации натализумаба и авонекса по сравнению с монотерапией авонексом [51].
В настоящее время препарат тизабри показан для монотерапии ремиттирующей формы РС следующим группам больных: пациентам с активным течением заболевания, несмотря на лечение ИФН β; пациентам с быстро прогрессирующим тяжелым ремиттирующим РС. Противопоказаниями к его назначению являются гиперчувствительность к натализумабу или любому из вспомогательных веществ; прогрессирующая многоочаговая лейкоэнцефалопатия (ПМЛ); повышенный риск инфекции условно-патогенными микроорганизмами, в том числе иммунодефицитные состояния; одновременное применение ИФН β или глатирамера ацетата; злокачественные новообразования, за исключением базальноклеточного рака кожи; детский и подростковый возраст. Не следует назначать натализумаб во время беременности без крайней необходимости; если пациентка забеременеет во время приема тизабри, терапию следует прекратить; пациентки, получающие тизабри, должны прекратить кормление грудью. Применение тизабри у пациентов старше 65 лет не рекомендуется из-за отсутствия данных о его безопасности для этой категории больных. Препарат применяется в виде внутривенных инфузий 1 раз в 4 нед. При использовании тизабри необходимо помнить о возможности развития различных побочных эффектов. В частности, его применение может повысить риск развития такого опасного нежелательного явления, как ПМЛ, при этом риск ее развития увеличивается по мере продолжительности терапии, особенно при лечении препаратом более 2 лет. При назначении данного препарата необходимо тщательное наблюдение за пациентами, в том числе мониторинг побочных эффектов: инфекций, включая ПМЛ и инфекции условно-патогенными микроорганизмами; развития гиперчувствительности на введение препарата; побочного влияния на функцию печени и др. В связи с этим разрабатываются специальные программы наблюдения за лицами, получающими тизабри; препарат назначается только после соответствующего информирования пациента, при этом врач и пациент должны в индивидуальном порядке рассмотреть соотношение пользы и риска при лечении препаратом тизабри.
Следующие два новых препарата для лечения ремиттирующего РС: гилениа (финголимод) и мовектро (кладрибин), предназначены для перорального приема. Финголимод является модулятором рецепторов сфингозин-1 фосфата. После фосфорилирования финголимод действует как функциональный антагонист рецепторов сфингозин-1 фосфата 1-го типа, вызывая их смещение с внешней мембраны лимфоцитов на внутреннюю, что делает Т- и В-лимфоциты невосприимчивыми к сигналам, стимулирующим их выход из вторичной лимфоидной ткани [13, 52]. Возникающее в результате этого перераспределение лимфоцитов в лимфоузлы и предотвращение их миграции из лимфоузлов уменьшает поступление аутоагрессивных лимфоцитов в ЦНС [39, 40, 46]. Благодаря липофильности финголимод проникает через гематоэнцефалический барьер и проходит фосфорилизирование в ЦНС [23]. Показано также, что финголимод может оказывать нейропротективное действие и способствует ремиелинизации в ЦНС путем взаимодействия с рецепторами сфингозин-1 фосфата на нейронах [6, 15, 23, 43].
В двух проведенных исследованиях финголимод использовался в двух суточных дозах: 1,25 или 0,5 мг.
В одном из исследований показано преимущество финголимода в обеих указанных дозах в сравнении с ИФН β-1а для внутримышечного введения по таким параметрам эффективности, как частота обострений и данные МРТ (меньшее количество новых или увеличивающихся гиперинтенсивных очагов в режиме Т2; очагов, накапливающих контрастное вещество в режиме Т1; процент уменьшения объема мозга от исходного уровня). Два случая инфекций с летальным исходом были зарегистрированы в группе, получавшей 1,25 мг финголимода: диссеминированная первичная инфекция, вызванная вирусом varicella zoster
, и энцефалит, вызванный вирусом простого герпеса. Другие нежелательные явления у пациентов, получавших финголимод, включали нефатальные случаи герпетической инфекции, брадикардию и атриовентрикулярную блокаду, артериальную гипертонию, отек макулы, рак кожи и повышение активности печеночных ферментов [16].
В другом исследовании пациенты получали финголимод в одной из указанных доз или плацебо. Препарат в обеих дозах значительно снижал риск нарастания инвалидизации; МРТ-показатели активности болезни (появление новых или увеличение существующих очагов в режиме Т2, очагов, накапливающих контрастное вещество, атрофии мозга). Причинами отмены препарата и нежелательными явлениями, связанными с приемом финголимода, были брадикардия и атриовентрикулярная блокада в начале лечения, отек макулы, повышение печеночных ферментов и легкая артериальная гипертония [38].
Надо отметить, что зарегистрированной дозой гилениа (финголимода гидрохлорида) является 0,5 мг перорально 1 раз в сутки; показанием для ее назначения — ремиттирующий РС – для уменьшения частоты клинических обострений болезни и снижения риска прогрессирования нетрудоспособности. Препарат противопоказан при гиперчувствительности к финголимоду или любому другому компоненту препарата, беременности и в период грудного вскармливания. Эффективность и безопасность применения препарата гилениа у детей и подростков в возрасте до 18 лет не установлены. Существует также целый ряд состояний, при которых данный препарат назначается с осторожностью. В связи с этим необходимы тщательное обследование пациента перед назначением препарата, наблюдение за приемом первой дозы, а также динамическое наблюдение на фоне приема препарата и контроль нежелательных явлений.
Механизм действия кладрибина связан с тем, что внутриклеточная аккумуляция его активного метаболита, 2-хлородезоксиаденозина трифосфата, приводит к нарушению клеточного метаболизма, угнетению синтеза и репарации ДНК и, соответственно, апоптозу [9]. Кладрибин преимущественно действует на лимфоциты. Накопление нуклеотидов кладрибина вызывает быстрое и длительное уменьшение количества CD4+ и CD8+ клеток, а также обладает быстрым, но более преходящим влиянием на CD19+ B-клетки с относительной сохранностью других иммунных клеток [9, 27, 30, 50]. Также кладрибин уменьшает уровень провоспалительных цитокинов и хемокинов в сыворотке и спинномозговой жидкости, экспрессию молекул адгезии, миграцию мононуклеарных клеток [7, 33, 38, 44].
В плацебо-контролируемом исследовании у пациентов с ремиттирующим РС, перорально получавших кладрибин в дозе 3,5 мг или 5,25 мг на килограмм массы тела, отмечено значительное снижение частоты обострений, более высокая доля пациентов без экзацербаций, более низкий риск устойчивого на протяжении 3 мес прогрессирования инвалидизации, а также значительное уменьшение количества очагов в головном мозге по данным МРТ по сравнению с группой плацебо. Нежелательные явления, которые чаще отмечались в группах, получавших кладрибин, включали лимфоцитопению, инфекцию herpes zoster
[27].
Мовектро в таблетках, содержащих активное вещество кладрибин (1 таблетка – 10,0 мг), показан к применению для лечения РС рецидивирующего (ремиттирующего) течения. Противопоказаниями для назначения мовектро являются повышенная чувствительность к кладрибину и другим компонентам препарата; острое инфекционное заболевание или обострение хронического заболевания; снижение иммунитета в связи с заболеванием или вследствие приема иммунодепрессантов, включая циклоспорин, метотрексат, митоксантрон, натализумаб, или длительного применения глюкокортикостероидов; вакцинация в течение предшествующих лечению 3 мес аттенуированной вакциной (живые или ослабленные вакцины); беременность, период лактации; возраст до 18 лет (недостаточно клинических данных). В связи с тем, что мовектро содержит сорбитол, у пациентов с непереносимостью фруктозы его применение не рекомендуется. Также существует ряд состояний, при которых данный препарат назначается с осторожностью.
Терапия мовектро проводится курсами; каждый курс состоит в применении 1 или 2 таблеток в течение первых 4 или 5 дней периода в 4 нед (расчет дозы проводится на основании массы тела пациента). Лечение препаратом начинают с 2 лечебных курсов, которые называют «начальная терапия». Интервал между курсами лечения мовектро в рамках «начальной терапии» составляет 4 нед. Через 10 мес после завершения «начальной терапии», на 49-й и 53-й нед курсы повторяют. Эти 2 курса называют «повторная терапия». Как перед началом терапии, так и в период терапии мовектро, необходимо выполнение определенных обследований с целью мониторинга состояния пациента.
При вторично-прогрессирующем и ремиттирующем РС при быстром прогрессировании заболевания и неэффективности средств первой линии, изменяющих течение РС, широко используется цитостатический препарат митоксантрон с целью снижения частоты и тяжести обострений и замедления темпа прогрессирования заболевания. Однако при использовании митоксантрона, как и других цитостатических препаратов, необходимо учитывать возможность развития побочных эффектов, в частности, миелосупрессии и кардиотоксичности, что требует тщательного отбора пациентов и мониторирования соответствующих показателей. Согласно публикации MSTCG [56], максимальная кумулятивная доза составляет 100 мг/м2 поверхности тела. Согласно другим данным, в ряде случаев суммарная доза должна составлять 80 мг/м2 поверхности тела. При этом рекомендуется проведение эхокардиографии перед каждым введением митоксантрона. Продолжение курса препарата возможно только в случае чувствительности пациента к проводимому лечению и сохранения признаков активности заболевания. При назначении препарата молодым женщинам необходимо учитывать возможность развития длительной или постоянной аменореи. Кроме этого, препарат может влиять и на фертильность у мужчин. Описано использование и других иммуносупрессантов: азатиоприна, циклофосфамида.
Наконец, в ряде случаев для снижения частоты и выраженности обострений, замедления прогрессирования инвалидизации при РС используется внутривенное введение иммуноглобулина, также показано снижение риска развития второй атаки и появления новых очагов у пациентов с КИС при его использовании.
Таким образом, за последние годы отмечается значительное расширение спектра препаратов для лечения РС, что обусловлено в том числе регистрацией новых средств с различными механизмами действия. С одной стороны, это увеличивает возможности современной терапии, модулирующей течение РС, с другой стороны, требует индивидуального подхода к подбору лечения с тщательным анализом показаний/противопоказаний и состояний, требующих осторожности, возможных побочных явлений; также необходим тщательный мониторинг состояния пациентов в период лечения с целью оценки как эффективности, так и безопасности назначенной терапии.
[] www.rlsnet.ru.
Заболевания
- 1. Общие положения
1.1. АНО «МИЦЛТ «Юнинова» предлагает пользователю сети Интернет (далее – «Пользователь») использовать свой портал «myclinicaltrial.ru» на условиях, изложенных в настоящем Пользовательском соглашении (далее – «Соглашение»). Любое развитие портала «myclinicaltrial.ru» является предметом настоящего Соглашения. Соглашение вступает в силу с момента выражения Пользователем согласия с его условиями в порядке, предусмотренном п. 1.2. Соглашения.
1.2. Начиная использовать портал «myclinicaltrial.ru»/его отдельные функции, Пользователь считается принявшим условия Соглашения в полном объеме без всяких оговорок и исключений. В случае несогласия Пользователя с какими-либо из положений Соглашения, Пользователь не вправе использовать портал «myclinicaltrial.ru». Если АНО «МИЦЛТ «Юнинова» были внесены какие-либо изменения в Соглашение в порядке, предусмотренном пунктом 1.3. Соглашения, с которыми Пользователь не согласен, он обязан прекратить использование портала «myclinicaltrial.ru».
1.3. Использование портала «myclinicaltrial.ru» регулируется настоящим Соглашением. Соглашение может быть изменено АНО «МИЦЛТ «Юнинова» без какого-либо специального уведомления пользователя, новая редакция Соглашения вступает в силу с момента ее размещения в сети Интернет по указанному в настоящем абзаце адресу, если иное не предусмотрено новой редакцией Соглашения. Действующая редакция Соглашения находится на странице по адресу myclinicaltrial.ru/agreement.
1.4. Любая информация о клинических исследованиях лекарственного препарата для медицинского применения, отраженная на портале «myclinicaltrial.ru», не содержит сведения рекламного характера.
- 2. Данные Пользователей
2.1. Использование портала «myclinicaltrial.ru» означает безоговорочное согласие Пользователя с автоматической передачей АНО «МИЦЛТ «Юнинова» в процессе использования портала «myclinicaltrial.ru» данных файлов cookie и предоставлением АНО «МИЦЛТ «Юнинова» IP-адреса, даты и времени доступа к порталу «myclinicaltrial.ru». Настоящее согласие дается Пользователем на неопределенный срок. Настоящее согласие может быть отозвано Пользователем путем направления соответствующего письменного заявления заказным почтовым отправлением с описью вложения в адрес АНО «МИЦЛТ «Юнинова.
2.2. Файлы cookie, данные IP-адреса, даты и времени доступа к порталу «myclinicaltrial.ru» могут использоваться АНО «МИЦЛТ «Юнинова» для исследовательских и статистических целей, для улучшения функционирования портала «myclinicaltrial.ru». АНО «МИЦЛТ «Юнинова» вправе установить, что предоставление портала «myclinicaltrial.ru» возможно лишь при условии разрешения Пользователем приема и получения файлов cookie. Структура, содержание и технические параметры файлов cookie устанавливаются АНО «МИЦЛТ «Юнинова» и могут изменяться без предварительного уведомления Пользователя.
- 3. Использование портала «myclinicaltrial.ru»
3.1. АНО «МИЦЛТ «Юнинова» вправе устанавливать ограничения в использовании портала «myclinicaltrial.ru» для всех Пользователей, в том числе наличие/отсутствие отдельных функций портала, максимальное количество вопросов, которые могут быть отправлены Пользователем, максимальный размер вопроса, максимальное количество обращений к порталу «myclinicaltrial.ru» и т.д. АНО «МИЦЛТ «Юнинова» вправе запретить автоматическое обращение к порталу «myclinicaltrial.ru».
3.2. Пользователь самостоятельно несет ответственность перед третьими лицами за свои действия, связанные с использованием портала «myclinicaltrial.ru», в том числе, если такие действия приведут к нарушению прав и законных интересов третьих лиц, а также за соблюдение законодательства при использовании портала «myclinicaltrial.ru».
3.3. При использовании портала «myclinicaltrial.ru» Пользователь не вправе загружать, посылать, передавать или любым другим способом размещать и/или распространять незаконный контент; нарушать права третьих лиц и иных образом нарушать нормы законодательства, в том числе нормы международного права.
3.4. Все объекты, доступные при помощи портала «myclinicaltrial.ru», в том числе элементы дизайна, текст, графические изображения, иллюстрации, видео, программы для ЭВМ, базы данных, музыка, звуки и другие объекты интеллектуальной деятельности, а также любой иной контент, размещенный на портале «myclinicaltrial.ru», являются объектами исключительных прав АНО «МИЦЛТ «Юнинова», Пользователей и других правообладателей. Использование элементов содержания и контента портала «myclinicaltrial.ru» возможно только в рамках функционала, предлагаемого порталом «myclinicaltrial.ru Никакие элементы содержания портала «myclinicaltrial.ru», а также любой контент, размещенный на портале «myclinicaltrial.ru», не могут быть использованы иным образом без предварительного разрешения правообладателя.
3.5. Портал «myclinicaltrial.ru» может содержать ссылки на другие сайты в сети Интернет (сайты третьих лиц). Указанные третьи лица и их контент не проверяются АНО «МИЦЛТ «Юнинова» на соответствие тем или иным законодательно установленным требованиям. АНО «МИЦЛТ «Юнинова» не несет ответственность за любую информацию, материалы, размещенные на сайтах третьих лиц, к которым Пользователь получает доступ с использованием портала «myclinicaltrial.ru», за доступность таких сайтов или контента и последствия их использования Пользователем. Ссылка на любой сайт, продукт, услугу, любую информацию третьего лица, размещенная на портале «myclinicaltrial.ru», не является одобрением или рекомендацией указанного сайта, продукта, услуги, информации со стороны АНО «МИЦЛТ «Юнинова».
- 4. Контент Пользователя
4.1. Пользователь самостоятельно несет ответственность за соответствие содержания размещаемого Пользователем контента требованиям действующего законодательства, включая ответственность перед третьими лицами в случаях, когда размещение Пользователем того или иного контента или содержание контента нарушает права и законные интересы третьих лиц, в том числе личные неимущественные права авторов, иные интеллектуальные права третьих лиц, и/или посягает на принадлежащие им нематериальные блага.
4.2. Пользователь признает и соглашается с тем, что АНО «МИЦЛТ «Юнинова» не обязан просматривать контент любого вида, размещаемый и/или распространяемый Пользователем посредством портала «myclinicaltrial.ru», а также то, что АНО «МИЦЛТ «Юнинова» имеет вправе по своему усмотрению отказать Пользователю в размещении и/или распространении им контента или удалить любой контент, который доступен посредством портала «myclinicaltrial.ru». Пользователь осознает и согласен с тем, что он должен самостоятельно оценивать все риски, связанные с использованием контента, включая оценку надежности, полноты или полезности этого контента.
4.3. Пользователь осознает и соглашается с тем, что технология работы портала «myclinicaltrial.ru» может потребовать копирование (воспроизведение) контента Пользователя АНО «МИЦЛТ «Юнинова», а также переработки его АНО «МИЦЛТ «Юнинова» для соответствия техническим требованиям портала «myclinicaltrial.ru».
- 5. Иные положения
5.1. Пользователь использует портал «myclinicaltrial.ru» на свой собственный риск, портал «myclinicaltrial.ru» предоставляется «как есть». АНО «МИЦЛТ «Юнинова» не гарантирует, что портал «myclinicaltrial.ru» соответствует требованиям Пользователя; портал «myclinicaltrial.ru» будет предоставляться непрерывно, быстро, надежно и без ошибок; результаты, которые могут быть получены с использованием портала «myclinicaltrial.ru», будут точными и надежными и могут использоваться для каких-либо целей или в каком-либо качестве; качество какого-либо продукта, услуги, информации и т.д., полученных с использованием портала «myclinicaltrial.ru», будет соответствовать ожиданиям Пользователя.
5.2. Любые информацию и/или материалы, доступ к которым Пользователь получает с использованием портала «myclinicaltrial.ru», Пользователь может использовать на свой собственный страх и риск и самостоятельно несет ответственность за возможные последствия использования указанных информации и/или материалов.
5.3. АНО «МИЦЛТ «Юнинова» не несет ответственности за любые виды убытков, произошедшие вследствие использования Пользователем портала «myclinicaltrial.ru» или отдельных функций портала «myclinicaltrial.ru». При любых обстоятельствах ответственность АНО «МИЦЛТ «Юнинова» в соответствии со ст. 15 Гражданского кодекса Российской Федерации ограничена 10 000 (десятью тысячами) рублей.
5.4. Соглашение представляет собой договор между Пользователем и АНО «МИЦЛТ «Юнинова» относительно порядка использования портала «myclinicaltrial.ru» и заменяет собой все предыдущие соглашения между Пользователем и АНО «МИЦЛТ «Юнинова».
5.5. Соглашение регулируется и толкуется в соответствии с законодательством Российской Федерации. Вопросы, не урегулированные Соглашением, подлежат разрешению в соответствии с законодательством Российской Федерации. Все возможные споры, вытекающие из отношений, регулируемых настоящим Соглашением, разрешаются в порядке, установленном действующим законодательством Российской Федерации. Везде по тексту настоящего Соглашения, если явно не указано иное, под термином «законодательство» понимается как законодательство Российской Федерации, так и законодательство места пребывания Пользователя.
5.6. Если по тем или иным причинам одно или несколько положений настоящего Соглашения будут признаны недействительными или не имеющими юридической силы, это не оказывает влияния на действительность или применимость остальных положений Соглашения.
5.7. Бездействие со стороны АНО «МИЦЛТ «Юнинова» в случае нарушения Пользователем положений Соглашений не лишает АНО «МИЦЛТ «Юнинова» права предпринять соответствующие действия в защиту своих интересов позднее, а также не означает отказа АНО «МИЦЛТ «Юнинова» от своих прав в случае совершения в последующем подобных либо сходных нарушений.