Эндокринная система и гормоны: что это
Эндокринная система представляет собой целый комплекс взаимосвязанных между собой органов и эндокринных желез, синтезирующих гормоны. Они под руководством нервной системы регулируют течение огромного количества протекающих в организме биохимических превращений и работу внутренних органов посредством тех же гормонов.
Гормоны – биологически активные вещества, синтезирующиеся организмом в незначительных количествах и отвечающие за передачу информации другим органам, не меняя своей природы и не вступая напрямую в различные биохимические превращения.
Элементами эндокринной системы являются как непосредственно железы внутренней секреции (поджелудочная, щитовидная, паращитовидные железы), так и отдельные органы, а также части головного мозга, включая гипофиз, гипоталамус, эпифиз, тимус, надпочечники, гонады (яички у мужчин и яичники у женщин). Даже жировая ткань является гормонпродуцирующим органом. Кроме того, эндокринные клетки есть и в ряде других органов, включая сердце, почки и пр.
Каждый из них ответственен за продукцию конкретного гормона, который выделяется в кровь и с ней доставляется непосредственно в органы и ткани мишени, запуская или останавливая протекание того или иного процесса. Благодаря этому не только обеспечивается выполнение важных для жизнедеятельности процессов, но и способность организма чутко подстраиваться под изменения условий внутренней и внешней среды, расти и развиваться.
Взаимодействие гормонов с тканями осуществляется главным образом по принципу обратной связи. То есть синтезированной эндокринной железой гормон доставляется к клеткам-мишеням, запускает определенный процесс, что приводит к выработке другого гормона другой железой, который воздействует на источник продукции первого, давая знать, что нужный процесс осуществлен и тем самым тормозя его синтез. Таким образом, все гормоны и, соответственно, эндокринные органы тесно взаимосвязаны между собой и чутко реагируют на изменения в работе друг друга. Поэтому при возникновении нарушений в одном из органов эндокринной системы неизбежно страдает весь организм.
Таким образом, баланс гормонов очень важен для организма, но он может нарушаться на фоне действия различных факторов, в числе которых:
- стрессовые ситуации;
- хронический недосып;
- ослабление иммунитета;
- курение и злоупотребление алкоголем;
- нерациональное использование лекарственных средств;
- заражение гельминтами и другими паразитами;
- некоторые заболевания.
К сожалению, с подобными факторами может столкнуться каждый человек, поскольку избежать их в условиях современной жизни практически невозможно. Поэтому и нарушения гормонального баланса сегодня встречаются крайне часто, что приводит к неблагоприятным цепным изменениям в работе организма, нарушению протекания множества обменных процессов и развитию самых разнообразных заболеваний, осложнения которых способны приводить даже к летальным последствиям. А потому любые изменения в гормональном фоне требуют медикаментозной коррекции.
Тем не менее мужской организм более стабилен с точки зрения поддержания нормального гормонального фона. У женщин же он может колебаться в силу физиологических изменений, в частности при наступлении беременности, во время грудного вскармливания и при наступлении менопаузы. Кроме того, женский гормональный фон регулярно изменяется в течение каждого менструального цикла, чем объясняется тот факт, что сдавать анализы на женские половые гормоны необходимо строго в определенные дни цикла. В противном случае полученные данные могут быть неинформативными.
Во избежание развития различных заболеваний, обусловленных изменениями гормонального фона, важно его своевременно корректировать, в том числе и при физиологических изменениях, обусловленных менопаузой, поскольку дефицит эстрогенов повышает риск развития не только заболеваний половых органов, но и онкологии.
Сегодня известно более 60 различных гормонов, в число которых входят и половые. Женские половые гормоны называют эстрогенами, мужские – андрогенами. Тем не менее, эта градация довольно условна, поскольку в женском организме синтезируются как эстрогены, так и андрогены, точно так же, как и в мужском. Более того андрогены выступают в качестве основы для синтеза эстрогенов у женщин и играют важную роль в поддержании гомеостаза. Рассмотрим подробнее органы эндокринной системы и их основные гормоны.
Мелатонин – «гормон сна» и не только
В.Д. Забелина, к.м.н., эндокринолог Consilium provisorum, 2006, № 3. – С. 9-12
Гормон мелатонин был впервые выделен из материала бычьих пинеальных (шишковидных) желез в 1958 г. в Йельском университете группой американского дерматолога А. Лернера. Эпифиз является нейроэндокринным органом и обнаружен у всех позвоночных, однако его роль в ходе эволюции менялась. У рыб и амфибий эпифиз еще непосредственно обладает фоторецепцией («третий глаз»), у рептилий и птиц эпифизу свойственна еще секреторная функция, у млекопитающих это уже исключительно секреторный орган. Но у всех видов животных основной функцией эпифиза является передача информации о световом режиме в окружающей среде во внутреннюю среду организма и поддержание таким образом физиологических ритмических колебаний его гомеостаза. Это опосредовано главным образом секрецией основного гормона мелатонина, причем если у некоторых птиц и низших позвоночных эпифиз является генератором биологических ритмов, то у млекопитающих он непосредственно вовлечен в координацию физиологических ритмов организма.
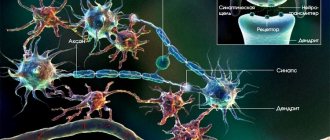
Основным и наиболее изученным гормоном эпифиза является мелатонин, но эпифизом могут секретироваться и некоторые другие производные серотонина и пептидные гормоны. Было выяснено, что мелатонин является индольным производным серотонина и продуцируется ночью с участием ферментов N-ацетилтрансферазы и гидроксииндол-О-метилтрансферазы. У взрослого человека за сутки синтезируется около 30 мкг мелатонина, его концентрация в сыворотке крови ночью в 30 раз больше, чем днем, причем пик активности приходится на 2 ч ночи. Мелатонин транспортируется сывороточным альбумином, после освобождения от альбумина связывается со специфическими рецепторами на мембране клеток-мишеней, проникает в ядро и там осуществляет свое действие. Мелатонин быстро гидролизуется в печени и экскретируется с мочой, основным метаболитом является 6-гидроксимелатонин-сульфат (6-СОМТ), содержание которого позволяет косвенно судить о продукции мелатонина эпифизом.
Особенности секреции мелатонина
Многие субстраты и метаболические пути синтеза мелатонина имеют отчетливый циркадианный ритм. Так, уровень серотонина, предшественника мелатонина, поднимается днем и существенно снижается в темную фазу суток, активность N-ацетилтрансферазы и концентрация мелатонина максимальны ночью и обусловлены высвобождением норадреналина из симпатических нейронов, локализующихся в эпифизе. Практически сразу после синтеза мелатонин секретируется клетками эпифиза – пинеалоцитами в системную циркуляцию. Циркадианный ритм синтеза мелатонина появляется сразу после рождения плода и у доношенных младенцев устанавливается к 9–12 нед жизни, а 2–3 нед позже – у недоношенных детей. Низкие ночные концентрации мелатонина повышаются к 2–3 годам, потом значительно снижаются к 15–20 годам и устанавливаются на уровне взрослого организма. Данные о сезонных вариациях синтеза мелатонина в организме человека статистически недостоверны и противоречивы.
Свет является очень мощным фактором, влияющим на синтез гормона, и даже очень короткое воздействие ярким светом в ночное время быстро и значительно подавляет образование мелатонина. Интересно, что имеются видовые различия подавления синтеза мелатонина светом: на хомяков больше действует голубой свет, на крыс – белый, причем для них достаточно очень малой мощности светового потока, а для земляных белок – в тысячи раз больше. Красный свет подавляет синтез мелатонина по-разному в зависимости от времени суток: в 16.00 сильнее, чем в 24.00.
Достоверных половых различий в синтезе мелатонина не отмечено. В процессе старения циркадианный ритм секреции мелатонина сохраняется, но его среднесуточные концентрации у пожилых людей на 50% меньше, чем у молодых. Однако 33% 70–90-летних людей имеют нормальные дневные уровни мелатонина. При этом следует отметить, что снижение уровня мелатонина при старении не носит «катастрофического характера».
Физические нагрузки изменяют содержание мелатонина: у женщин физические упражнения днем увеличивают дневные уровни мелатонина в крови, но при увеличении интенсивности нагрузок они приходят в норму. Выполнение упражнений поздним вечером (когда физиологически уже повышается секреция мелатонина) замедляло увеличение его концентрации по сравнению с упражнениями днем и утром. Высокоинтенсивные упражнения ночью (при имеющихся высоких уровнях мелатонина) приводили к увеличению его секреции на 50%, при этом на следующие сутки увеличение секреции мелатонина ночью запаздывало на 2–3 ч. Разноречивы данные о влиянии продолжительности сна на уровни мелатонина, однако положение тела отражается на ночных уровнях гормона: увеличивается при лежании на спине и уменьшается при изменении позиции.
Ночные пики гормона существенно снижаются после долгосрочного воздействия магнитных полей низкой частоты. Секрецию мелатонина снижает воздействие поляризованного электромагнитного поля (у электриков, подверженных воздействию поля в 60 Гц, уменьшается выделение метаболитов мелатонина).
Биологические эффекты мелатонина
Мелатонин – ключевой координатор биологических ритмов, но это не единственная его функция. Установлены 3 типа рецепторов к мелатонину – М-1a, M-1b и M-1c, но у людей обнаружены только первые два. Рецепторы M-1b обнаружены в сетчатке глаза, различных отделах мозга, и считается, что именно через них устанавливаются циркадианные ритмы. Рецепторы М-1a обнаружены в гипоталамусе, почках, кишечнике и клетках меланомы.
Мелатонин обладает антигонадотропным действием и рассматривается как гормональный посредник, модулирующий активность репродуктивной системы в зависимости от фотопериодического окружения. У животных описаны задержка полового развития самок и снижение секреции тестостерона у самцов под воздействием высоких концентраций мелатонина.
Помимо гормональных эффектов, мелатонин, как и другие биогенные амины, обладает нейротрансмиттерными функциями, т.е. обеспечивает возбудимость постсинаптических мембран и участвует в проведении нервного импульса. Это действие чрезвычайно важно для обеспечения висцеральных эффектов и интегративных функций, таких как поведение, память и обучение.
Мелатонин – самый сильный из известных эндогенных поглотителей свободных радикалов, сильнейший антиоксидант. В последние годы появились данные, что мелатонин может локализоваться не только в плазме, но и в ядрах клеток, предохранять макромолекулы ядра от оксидативного повреждения во всех субклеточных структурах.
На ранних стадиях эмбрионального развития биогенные амины, в том числе мелатонин, играют роль специализированных клеточных сигнальных молекул, регулирующих процессы клеточного обновления. Установлено, что мелатонин может подавлять клеточную пролиферацию, причем сила его воздействия не уступает мощному цитотоксическому агенту колхицину. Эти результаты коррелируют с экспериментальными данными об антиопухолевых эффектах мелатонина и экстрактов шишковидной железы.
Мелатонин – гормон, образующийся не только в шишковидной железе
Количества гормона, вырабатываемого в шишковидной железе, было бы явно недостаточно для обеспечения столь значительных биологических эффектов мелатонина. Исследованиями было показано, что после удаления пинеальной железы у экспериментальных животных в крови обнаруживаются значимые количества мелатонина. После получения специфических антител к индолалкиламинам оказалось возможным найти и экстрапинеальные источники синтеза мелатонина. Ими оказались энтерохромаффинные клетки желудочно-кишечного тракта (ЕС-клетки), основные клетки-депо серотонина (содержат до 95% всего эндогенного серотонина) – предшественника мелатонина. Количество этих клеток в желудочно-кишечном тракте значительно больше, чем пинеалоцитов. Далее выяснилось, что мелатонин синтезируется не только в них! Синтез этого гормона выявлен и в большом количестве нейроэндокринных клеток воздухоносных путей, легких, под печеночной капсулой, в корковом слое почек и вдоль границы между корковым и мозговым слоем надпочечников, в параганглиях, желчном пузыре, яичниках, эндометрии, предстательной железе, плаценте и внутреннем ухе. В последние годы обнаружили синтез мелатонина и в неэндокринных клетках: в тимусе, поджелудочной железе, мозжечке, сетчатке глаза, в клетках крови – тучных клетках, лимфоцитах – естественных киллерах, тромбоцитах, эозинофильных лейкоцитах, а также в некоторых эндотелиальных клетках. Функционально все клетки, продуцирующие мелатонин, относятся к так называемой диффузной нейроэндокринной системе, универсальной системе адаптации и поддержания гомеостаза организма.
В пределах этой системы выделяют два звена мелатонинпродуцирующих клеток: центральное (включает пинеальную железу и клетки зрительной системы), в котором ритм секреции мелатонина совпадает с ри, и периферическое – все остальные клетки, где секреция гормона не зависит от освещенности. Выдвигается предположение, что экстрапинеальный мелатонин может играть ключевую роль в качестве паракринной сигнальной молекулы взаимодействия клеток и локальной координации клеточных функций, однако полностью роль его до сих пор не ясна, поэтому исследования в этом направлении идут очень интенсивно.
Мелатонин может влиять на опухолевый рост
В ряде исследований на лабораторных животных и в системах культур опухолевых тканей было обнаружено, что мелатонин обладает антиопухолевым, онкостатическим действием. Это чрезвычайно подогрело интерес к этому гормону, и изучение его эффектов идет очень активно. Трудно сделать окончательный вывод об унитарном механизме действия мелатонина на опухолевый рост из-за его многообразных физиологических эффектов. Сюда включаются его влияния на синтез и секрецию гипофизарных и половых гормонов, модуляцию иммунного ответа на наличие опухолевых клеток и прямые цитотоксические эффекты на них как мощного эндогенного антиоксиданта. Имеются предположения, что мелатонин может усиливать экспрессию молекул адгезии и этим препятствовать росту опухоли, так как известно, что большинство злокачественных опухолей имеют нарушения в адгезии клеток и функциональных межклеточных связей. Отечественными исследователями (Т.В. Кветная, И.М. Кветной и соавт.) было показано, что у больных раком толстой кишки, желудка и легкого экскреция 6-СОМТ, метаболита мелатонина достоверно положительно коррелирует с надежным маркером пролиферативной активности опухолевых клеток – ядерным антигеном пролиферирующих клеток (PCNA). Этот показатель отражает фракцию пролиферирующих клеток и дает представление о возможной прогрессии опухоли. Высказано предположение, что определение экскреции 6-СОМТ может быть полезным в динамическом наблюдении за пациентами с заболеваниями раком этих локализаций.
Онкостатический эффект мелатонина in vitro был показан наиболее четко в опытах на культурах клеток MCF-7 рака молочной железы. Отмечалось снижение пролиферативной способности клеток и метастазирования, увеличение числа клеток, которые гибнут в форме апоптоза. Считают, что мишенью для реализации противоопухолевых эффектов мелатонина могут служить ядерные рецепторы этих клеток. Существует связь между наличием на раковых клетках рецепторов к эстрогенам и действием мелатонина: его эффект больше при наличии рецепторов, возможно, мелатонин действует как естественный антиэстроген. В опытах на грызунах было обнаружено, что воздействие постоянного освещения увеличивало частоту развития рака молочных железы и матки, а введение мелатонина в дозе 50–100 мг/сут оказывало протективный эффект на развитие опухолей, мастопатии, фолликулярных кист яичников. Эпидемиологические данные свидетельствуют, что у женщин – работников ночных смен, авиационных служащих (стюардессы, диспетчеры), операторов радио и телеграфа имеется повышенный риск развития рака молочной железы, тогда как у женщин первично слепых (т.е. имеющих световую депривацию) этот риск в 2 раза меньше.
In vitro было показано подавляющее действие мелатонина на рост клеток меланомы, хотя эффект гормона зависел от интенсивности пролиферации опухоли: рост ингибировался при умеренной, но не при высокой пролиферативной активности клеток. Эффекты мелатонина являлись дозозависимыми, но механизм онкостатического действия на настоящий момент не вполне понятен. Мелатонин подавлял также рост клеток увеальной меланомы, характеризующейся высокой степенью метастазирования, что позволяет считать его перспективным препаратом в терапии увеальной меланомы.
В экспериментах было показано ингибирующее влияние мелатонина на рост культур клеток карцином яичника, нейробластом, опухоли гортани, рака мочевого пузыря и некоторых других. Однако остается большое количество неясных вопросов по механизмам действия мелатонина, отсроченных эффектов, и исследования в этих направлениях активно продолжаются.
Влияние мелатонина на сон
Как уже было сказано, роль эпифиза и эпифизарного мелатонина в суточной и сезонной ритмике, режиме сна–бодрствования на сегодняшний день представляется несомненной. У диурнальных (дневных) животных (в том числе у человека) секреция мелатонина эпифизом совпадает с привычными часами сна. В ряде исследований было показано, что повышение уровня мелатонина не является императивным, обязательным сигналом к началу сна. У большинства испытуемых прием физиологических доз мелатонина вызывал лишь мягкий седативный эффект и снижал реактивность на обычные окружающие стимулы. В отличие от мощных «ночных» седатиков-гипнотиков бензодиазепинового ряда мелатонин не вызывает чувства невыносимой усталости и непреодолимой тяги ко сну. При достаточной мотивированности человек сможет преодолеть сомногенное действие мелатонина.
Прием «физиологических» доз мелатонина (0,1–0,3 мг) в утреннее, дневное и вечернее время приводит к увеличению его концентрации в плазме до 50–120 мг/мл, что соответствует ночному уровню гормона у взрослых здоровых людей. После приема per os 2–3 мг мелатонина его уровень в плазме оставался выше нормального в течение 3–7 ч, причем пик концентрации достигался через 60 мин. В эксперименте инфузии мелатонина в дневные часы у здоровых людей приводили к усилению сонливости. Вечерний прием небольших доз мелатонина вызывал снижение латентности и удлинение ночного периода покоя, тогда как подавление продукции мелатонина приводило к разрушению архитектуры сна. Результаты приема как больших (до 80 мг), так и более низких (1–6 мг) доз мелатонина крайне противоречивы, поэтому предпринимаются все новые исследования влияния мелатонина на структуру и качество сна.
Высказывается гипотеза, что роль мелатонина состоит в открытии так называемых ворот сна, в торможении режимов бодрствования, а не в прямом воздействии на сомногенные структуры головного мозга. По мнению физиологов-гипнологов, открытию «ворот сна» предшествует период повышенной активации человека – «запретный период» («запретная зона») для сна, которая довольно резко сменяется «открытием ворот». Есть некоторые свидетельства, что «запретная временная зона» представляет собой пик ежедневного цикла бодрствования. Начало ежевечернего увеличения секреции мелатонина приходится обычно на середину «запретного периода». По достижении его концентрации в крови, соответствующей примерно половине максимального «ночного» уровня, происходит резкий подъем «давления сна», способствующий к переходу от бодрствования ко сну.
Десинхронизация между секрецией мелатонина эпифизом и периодом сна у человека может возникнуть в случае полной слепоты, разрушения эпифиза (оперативное удаление, опухоль, кровоизлияние в эпифиз), при трансмеридианальных перелетах или сменной работе. При этом своевременное введение мелатонина может способствовать быстрому «переводу» биологических часов организма на новый ритм.
В отношении трансмеридианальных перелетов рекомендации таковы: 1) при перелетах на расстояние менее 3 часовых поясов применение мелатонина бесполезно; 2) при перелетах на 3–6 часовых поясов в восточном направлении – прием 0,2 мг мелатонина при отходе ко сну по местному времени для сдвига фазы суточного ри; 3) при перелетах на 3–6 часовых поясов в западном направлении – прием 0,1 мг мелатонина сразу после полуночи по местному времени, если человек в это время не спит, или же при спонтанном пробуждении в ранние утренние часы; 4) при перелетах на 7–12 часовых поясов в любом направлении мелатонин противопоказан, поскольку это может ухудшить субъективное состояние человека.
Применение мелатонина для коррекции биоритмов при сменной работе очень индивидуально, и решение зависит от характера этой работы, освещенности и особенностей личности человека. В идеале должно учитываться индивидуальное изменение концентрации мелатонина до и после приема, что можно уточнить по исследованию мочи и слюны.
В Сомнологическом центре МЗ РФ в 1998–1999 гг. А.М. Вейном, Я.И. Левиным и соавт. проводилось изучение снотворных эффектов мелатонина на качество ночного сна у пациентов с бессонницей (по 3 мг каждый вечер за 30 мин до отхода ко сну). В группе из 40 человек было определено достоверное улучшение сна в целом, в том числе наиболее значительно улучшалось засыпание. Интересно, что чем хуже были исходные субъективные показатели сна, тем сильнее положительное влияние мелатонина.
Теми же авторами был показан положительный эффект меньших доз мелатонина (1,5 мг на прием) на качество ночного сна у больных с фибромиалгиями, при этом и днем улучшалось качество тонкой моторики рук, общее самочувствие и настроение этих пациентов. У больных, перенесших инсульт, после приема мелатонина в дозе 3 мг уменьшалось время засыпания, при инверсии сна отмечалось восстановление биори. Важным эффектом оказалось снижение уровня депрессии, хотя личностная и реактивная тревожность остались без изменений.
Прием мелатонина должен проводиться на фоне очень слабой освещенности (не более 50 люкс), поскольку яркий свет несовместим с его поступлением в организм. Высокая концентрация мелатонина повышает фоточувствительность рецепторов сетчатки и может провоцировать их повреждение ярким светом.
Мелатонин абсолютно нетоксичен, во всяком случае при кратковременном использовании. Но отсутствие острой токсичности даже фармакологических доз препарата (миллиграммы и даже граммы мелатонина) не гарантирует от побочных последствий длительного применения мелатонина в больших дозах. Кроме нарушения биоритма, после приема мелатонина в «неподходящее время» избыток мелатонина может теоретически привести к серьезным эндокринным нарушениям (первичный гипогонадизм у мужчин и аменорея у женщин). Дети вообще очень чувствительны к мелатонину, поэтому его применение у них требует большой осторожности. Не стоит забывать о возможных взаимодействиях мелатонина с другими медикаментами. Особую роль могут играть психотропные препараты, воздействующие на серотонинергическую и норадренергическую передачи в нервной системе, поскольку секреция мелатонина в темное время суток зависит от симпатической (норадренергической) передачи, а серотонин является его непосредственным биохимическим предшественником.
Учитывая, что снотворный эффект «физиологических» доз мелатонина (0,1–0,5 мг на прием) достаточно выражен, желательно стремиться к использованию именно таких невысоких доз препарата.
Эпифиз и мелатонин – звенья в защитной системе организма от стрессов
После экспериментов и прямых клинических наблюдений была сформулирована концепция, что эпифиз и его основной гормон мелатонин входят в защитную систему организма от всяческих неблагоприятных воздействий. Эпифиз и мелатонин играют неспецифическую роль, но эпифизарная поддержка осуществляется на всех уровнях борьбы со стрессом. Отмечается двухфазная реакция в случае длительной стрессовой ситуации: первоначальный спад эпифизарной деятельности в резистентную фазу стресса с дальнейшим резким ее подъемом. В экспериментах на крысах было показано, что мелатонин способен менять отрицательное эмоциональное состояние, демпфировать тревожность, которая провоцируется различными стрессорами, и потому модифицировать патофизиологические сдвиги, возникающие в последующем. Это было подтверждено на здоровых добровольцах: прием низких доз мелатонина снижал чувство тревоги, нормализовал ночной сон с его углублением и уменьшением числа ночных пробуждений.
Согласно многочисленным наблюдениям, гормон стабилизирует деятельность различных эдокринных систем, дезорганизованных стрессом, в том числе ликвидируя избыточный стрессовый адреналовый гиперкортицизм. Важным последствием длительных стрессов является стрессовый иммунодефицит, а мелатонин способствует нормализации иммунологических показателей. Высказывается мнение, что эпифиз играет определенную роль в противодействии химической агрессии, борьбы с различными ксенобиотиками (в том числе фармакологическими препаратами). Было обнаружено, что гиперактивность эпифиза или введение мелатонина провоцируют толерантность ко многим веществам, в первую очередь психотропным средствам. Вспомним, что одной из тяжелых пыток для человека оказывается яркий постоянный свет в помещении принудительного пребывания. Возможно, что длительное воздействие интенсивным светом, особенно в ночное время, может оказывать патогенное воздействие на организм именно из-за подавления биологического ритма синтеза мелатонина. Физиологами изучаются механизмы действия мелатонина в период стрессовых воздействий, и постепенно многие вопросы становятся все яснее. Тем не менее эти проблемы настолько сложны, что требуют дальнейших исследований и экспериментов.
Роль мелатонина в развитии заболеваний сердечно-сосудистой системы, желудочно-кишечного тракта, влияние эпифиза и мелатонина на сезонность обострений заболеваний, изменение в репродуктивной системе женщин также привлекают большое внимание ученых, но на сегодня остается много неясного и спорного, что диктует необходимость дальнейших исследований.
Мелатонин и другие эпифизарные гормоны могут быть отнесены к числу геропротективных. Установлен параллелизм между степенью возрастной инволюции эпифиза и дряхлением тканей. Известно, что при старении снижается степень иммунологической защиты, а мелатонин, как уже неоднократно указывалось, имеет иммуномодулирующую активность.
Антиоксидантная, противоопухолевая, иммуномодулирующая, противотревожная, антидепрессивная и гипногенная активность мелатонина, нетоксичность препарата делают его очень привлекательным для использования в практике лечения большого спектра заболеваний человека, особенно в пожилом возрасте. Несомненно, что исследование мелатонина, его физиологических и фармакологических эффектов будет продолжаться, т.к. это может дать новые терапевтические возможности.
Гипофиз и гипоталамус
Гипоталамус является своеобразным связующим звеном между эндокринной и нервной системой, поскольку он одновременно принадлежит к обеим. Именно он контролирует и объединяет эндокринные механизмы регуляции с нервными. В нем в ответ на получаемые от центральной и вегетативной нервной системы сигналы синтезируются так называемые нейрогормоны, которые ответственны за регуляцию выработки собственных гормонов другими эндокринными железами. Он же контролирует работу гипофиза, являющегося центральным органом эндокринной системы и оказывающего наибольшее влияние на деятельность остальных ее составляющих.
Именно гипоталамус способен отдать гипофизу команду усилить или замедлить продукцию всех остальных гормонов в организме.
Адренокортикотропный гормон
Адренокортикотропный гормон (АКТГ) представляет собой гормон пептидного происхождения, который синтезируется передней долей гипофиза под влиянием вырабатываемых гипоталамусом нейрогормонов. Он ответственен за инициацию синтеза кортизола в надпочечниках, а также андрогенов, т. е. мужских половых гормонов. При этом адренокортикотропный гормон, который еще называют кортикотропином, способствует повышению чувствительности периферических тканей к действию кортикостероидов. В меньшей степени он ответственен за протекание биохимических процессов, отвечающих за образование костной ткани остеобластах.
Уровень АКТГ может колебаться под действием стресса, физических нагрузок, а также изменяется во время сна, беременности и зависит от фазы менструального цикла.
Нормой считается содержание АКТГ в крови в пределах от 0 до 46 пк/мл. Физиологический пик его выработки приходится на 6—8 часов, а минимум — на 18—23 часа. Его концентрация может повышаться при:
- первичной недостаточности коры надпочечников;
- синдроме Нельсона;
- врожденной гиперплазии надпочечников;
- паранеопластическом синдроме;
- синдроме эктопической продукции АКТГ и т. д.
Причиной повышения содержания АКТГ в крови может быть прием препаратов, содержащих глюконат кальция, инсулин, вазопрессин, эстрогены, кортикостероиды, спиронолактон, литий, метоприрон, этиловый спирт.
При длительном сохранении повышенной выработки АКТГ может наблюдаться увеличение размеров надпочечников, а также накапливание в их коре холестерина, аскорбиновой и пантотеновой кислоты, что приведет к ее разрастанию.
Снижение уровня АКТГ может быть следствием:
- вторичной надпочечниковой недостаточности;
- рака коры надпочечников;
- введения кортикостероидов;
- наличия опухоли, продуцирующей кортизол.
Вазопрессин (антидиуретический гормон)
Вазопрессин – пептидный гормон, который синтезируется задней долей гипофиза. Его основной задачей является сужение кровеносных сосудов, что является одним из механизмов регуляции уровня кровяного давления, а именно способствует его повышению. Также вазопрессин ответственен за обратное всасывание воды в почках, что приводит к уменьшению объема отводящейся мочи и поддержанию нормального водно-солевого обмена. Благодаря этому свойству вазопрессин и заслужил свое второе название – антидиуретический гормон.
При дефиците вазопрессина возможно развитие несахарного диабета.
Гормон роста
Соматотропин или гормон роста продуцируется гипофизом и является основным регулятором процесса роста и развития человека. Поддержание его выработки на должном уровне наиболее важно для детей в период с рождения до полового созревания, поскольку от него во многом зависит рост костей. У взрослых он сохраняется и отвечает за регуляцию плотности костей, поддержание мышечной массы, а также участвует в обмене жирных кислот.
Самый высокий уровень соматотропина в крови обычно наблюдается в ночное время. В норме у мужчин его концентрация составляет 0—3 нг/мл, у женщин – 0—8 нг/мл.
Недостаток гормона роста приводит к задержке физического развития детей, что может быть обусловлено опухолями и травмами гипофиза, перенесением менингита или рядом врожденных патологий. У взрослых дефицит соматотропина может приводить к повышению хрупкости костей, снижению объема мышц и концентрации липидов.
Избыток соматотропина наблюдается при опухолях гипофиза, которые обычно имеют доброкачественную природу. Это может выступать причиной гигантизма, формирования грубых черт лица, слабости, замедления полового развития, а у взрослых – акромегалии.
Лютеинизирующий гормон
Лютеинизирующий гормон (ЛГ) – гонадотропный гормоны передней доли гипофиза, который активизирует выработку половых гормонов как у женщин, так и у мужчин. Он стимулирует синтез эстрогена и прогестерона, а также провоцирует разрыв созревшего фолликула в яичнике и наступление овуляции. При этом ЛГ тесно взаимосвязан с эстрогенами, поэтому при колебаниях их уровня возможно и изменение концентрации ЛГ. У мужчин ЛГ влияет на клетки семенников, стимулирую в них продукцию тестостерона.
Повышение синтеза лютеинизирующего гормона возможно при возникновении:
- патологий гипофиза, включая образование злокачественных опухолей;
- поликистоза яичников;
- эндометриоза;
- урологических патологий;
- опухолей яичек.
Уровень ЛГ у женщин напрямую зависит от фазы менструального цикла. В норме он резко повышается с наступлением менопаузы.
В качестве симптомов избытка ЛГ могут выступать частые головные боли, одышка, слабость, нарушения менструального цикла и признаки избытка эстрогенов.
Дефицит гормона наблюдается при нарушении работы гипофиза, выраженном недостатке веса вплоть до анорексии, сильном стрессе. В таких ситуациях могут отмечаться нарушения работы ЖКТ, слабость.
Фолликулостимулирующий гормон
Фолликулостимулирующий гормон или ФСГ представляет собой гликопротеиновый гормон, синтезируемый в передней доле гипофиза и принимающих непосредственное участие в регуляции деятельности половых желез. Его выработку активизирует снижение концентрации половых гормонов, а угнетение – повышение их уровня. В норме уровень ФСГ резко возрастает перед началом полового созревания при развитии вторичных половых признаков.
С установлением менструального цикла у женщин гормон активизирует процесс созревания фолликулов в яичниках и подготавливает их к действию ЛГ, а также стимулирует синтез эстрогенов, т. е. взаимодействует с ними по принципу обратной связи. У мужчин ФСГ оказывает влияние на развитие семенных канальцев и возрастание уровня тестостерона, а также активизирует формирование и созревание спермы в яичках.
Избыток ФСГ возникает при патологиях почек, опухолях гипофиза, алкоголизме, первичной недостаточности яичек, гипогонадизме, эндометриозе. Это сопровождается у женщин прорывными маточными кровотечениями в отсутствии прямой зависимости от фазы менструального цикла или же отсутствием менструации, частыми головными болями.
Дефицит ФСГ может присутствовать при поликистозе яичников, патологиях гипоталамо-гипофизарной системы, истощении, анорексии, карликовости. В таких ситуациях нарушается менструальный цикл, возникают инфекционные или обостряются хронические заболевания половых органов, может возникнуть бесплодие.
Окситоцин
Окситоцин представляет собой нейропептид, накапливающийся в задней доле гипофиза и ответственный за сокращение мышц матки и протоков молочных желез, что приобретает особенную важность во время родов и последующего грудного вскармливания. Кроме того, окситоцин еще называют гормоном доверия, поскольку при увеличении его содержания в крови повышается уровень эмпатии и расположения.
Пролактин
Пролактин – еще один гормон гипофиза, который стимулирует нормальное развитие молочных желез, выработку молока при беременности, а также ответствен за поддержание лактации после родов. Кроме того, он регулирует синтез прогестерона и угнетает продукцию ФСГ, чем обеспечивает сохранение регулярности менструального цикла.
Высокая концентрация пролактина характерна для:
- гипотиреоза;
- образования опухолей гипофиза и гипоталамуса;
- ХПН;
- синдрома поликистозных яичников;
- гипогонадизма;
- сильного стресса.
Это приводит к развитию бесплодия, аменореи (отсутствию менструаций) и галактореи (образованию грудного молока вне наступления беременности и лактации). Это может сопровождаться дискомфортом в груди и головными болями.
В норме повышенный уровень пролактина наблюдается после родов при сохранении грудного вскармливания, что оказывает ановуляторное действие на яичники и снижает вероятность наступления беременности.
Дефицит гормона возникает при недостаточности гипофиза, что типично для:
- синдрома Шихана (некроз гипофиза, обусловленный чрезмерной кровопотерей при родах);
- травм, операций, лучевой терапии, затрагивающих гипофиз;
- приема противоэпилептических препаратов, некоторых кортикостероидов, дофаминэргетиков и т. д.
При снижении концентрации пролактина наблюдается повышенное потоотделение, сильная жажда. Если же у женщины синдром Шихана, происходит прекращение лактации, а затем постепенное уменьшение размера молочных желез, снижение веса, нарушение менструального цикла, снижение либидо.
Тиреотропный гормон
Тиреотропный гормон или ТТГ, прежде всего, отвечает за выработку гормонов щитовидной железы, ответственных за поддержание нормального уровня энергии. Поэтому при изменениях его выработки немедленно происходит нарушение синтеза тиреоидных гормонов, что приводит к развитию соответствующих заболеваний. Причинами нарушения продукции ТТГ гипофизом являются патологии гипоталамуса, а также щитовидной железы. Поэтому повышенные концентрации ТТГ в крови обнаруживаются при:
- гипотиреозе;
- опухолях гипофиза;
- преэклампсии;
- психических заболеваниях;
- недостаточности надпочечников.
Дефицит ТТГ характерен для диффузного токсического зоба, болезни Пламмера, гипертиреоза беременных, а также аутоиммунного тиреоидита и кахексии.
Гормоны эпифиза, шишковидной железы.
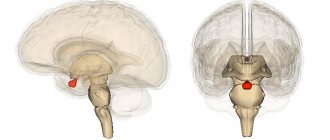
Эпифиз. Роль гормонов эпифиза.
Иначе, эпифиз можно назвать шишковидным телом, представляющим собой эндокринную железу серовато-красноватого цвета, располагающуюся в области среднего мозга человека.
Почему шишковидное тело? Такое название железа получила из-за своей формы (в переводе с греческого Epiphysis — шишка, нарост).
Несмотря на свой небольшой размер, железа является многофункциональным органом эндокринной системы человека.
Основная функция железы — выработка гормона мелатонина.
Мелатонин, чаще его называют гормоном сна, в свою очередь поддерживает физиологическое состояние организма на оптимальном уровне.
Строение эпифиза:
Орган является непарным и находится между двумя полушариями. Размеры железы небольшие, как маленькая горошина с бугристой поверхностью.
Эпифиз условно можно разделить на две части: строму и паренхиму.
Строма представляет собой соединительнотканные перегородки, идущие вглубь органа и разделяющие паренхиму на дольки. Строма-своеобразный каркас органа. Снаружи железа покрыта соединительнотканной капсулой.
Паренхима представлена дольками, в составе которых два типа клеток: секретообразующие пинеалоциты и интерстициальные клетки. Пинеалоциты преобладают в центральных частях долек, и среди них различают светлые и тёмные клетки. Интерстициальные клетки в свою очередь располагаются на периферии долек и выполняют опорную функцию.
Функции эпифиза:
Эндокринная железа выполняет следующие функции в организме человека:
1. Синтез биологически активных веществ – гормонов.
2. Регулирует обмен макроэлементов в организме: кальция, фосфора и магния.
3. Поддержание водно-солевого баланса.
4. Участвует в регуляции: кровяного давления, функции пищеварительного тракта, работы клеток мозга.
5. Отвечает за приспособленность организма к меняющимся условиям освещенности.
Эпифиз отвечает за синтез четырех биологически активных важных веществ:
1. Мелатонин
2. Серотонин
3. Гистамин (биогенный амин)
4. Норадреналин
МЕЛАТОНИН
Представляет собой гормон фотопериодичности, т. е. его синтез напрямую зависит от времени суток. Так, это биологически активное вещество, вырабатывается преимущественно ночью, из-за того, что световые импульсы поступающие через сетчатку глаза днём, вызывают угнетение его синтеза. Свет попадает в глаза и стимулирует сетчатку —> импульсы от сетчатки поступают в нервную систему —> угнетение выработки мелатонина. То же самое можно сказать и о звуке.
Но что же происходит внутри железы днём, когда мелатонин не может синтезироваться? В светлое время суток, идёт активное накопление серотонина.
Учеными доказано, что именно мелатонин, провоцирует у человека чувство сонливости.
В возрасте 9-13 лет, период полового созревания, отмечается максимальная секреция эпифизом мелатонина. С возрастом его значения в крови постепенно уменьшаются, приводя у пожилых людей к бессоннице неясной этиологии. Значение мелатонина в крови у женщин в прямой зависимости от фазы цикла, так, пик содержания приходится на менструацию, а минимальное значение — в период овуляции.
Зачем мелатонин нашему организму?
- Регулирование циркадных (суточных) ритмов — своеобразных «биологических часов» организма. Регулирует сменяющие друг друга циклы сна и бодрствования.
- Иммунностимулирующее действие.
- Блокируя выработку гонадотропных гормонов, синтезируемых гипофизом, поддерживает правильное формирование и функционирование репродуктивной системы женщины, нормализует менструальный цикл и отвечает за его продолжительность.
- Оптимизирует функции щитовидной железы.
- Антиоксидантная функция, нейтрализует свободные радикалы, тем самым приводя к уменьшению симптомов сахарного диабета, депрессии, артериальной гипертензии.
- Тормозит синтез инсулина, медиаторов воспаления, гормона роста.
- Оказывает успокаивающее действие, снижает тревожность.
- Тормозит старение организма и обмен веществ, увеличивая продолжительность жизни.
- Клинические исследования доказали, что мелатонин замедляет рост новообразований. Оказывает противоопухолевое действие.
СЕРОТОНИН
Гормон Серотонин или гормон счастья. как его принято негласно называть, вырабатывается в дневное время суток. По этой причине хороший источником серотонина — прогулки на свежем воздухе. Серотонин является основой для выработки мелатонина. Поэтому его роль гораздо больше для нашего организма, чем просто хорошее настроение.
Его роль для нашего организма:
1. Стимулирует выработку гормона пролактина, необходимого кормящей женщине для поддержания лактации.
2. Регуляция и оптимизация настроения.
3. Анальгезирующее действие при патологиях различного генеза.
4. Стимулирует пищеварение.
5. При аллергических и воспалительных реакциях регулирует процессы свёртывания крови.
6. Влияет на созревание и выход из яичника яйцеклетки у женщин.
ЭПИФИЗ И СОН.
Вырабатываемый эпифизом гормон мелатонин, воздействуя на мозг, оказывает угнетающее действие на биоэлектрическую активность мозга и нервно-психическую деятельность человека, тем самым оказывая снотворный и успокаивающий эффект. Мелатонин для нас, как уникальные внутренние часы, благодаря которым утром нам хочется просыпаться, а ночью спать.
Думаю, вы не раз замечали, как уже вечером постепенно начинает клонить в сон. Потому что, именно в темное время суток происходит синтез гормона, своеобразным образом «укладывающего нас спать». В народе говорят «сон — лучшее лекарство», и это действительно так. Во время сна наша шишковидная железа неустанно трудится, восстанавливая все повреждения и укрепляя организм. Максимальное количество вещества вырабатывается около 2‐х часов ночи, а уже к 9 утра его количество резко уменьшается. Доказано, что при приеме внутрь, мелатонин оказывает снотворное действие, при этом, не нарушая фазы сна.
Препарат Эндолутен содержит пептиды эпифиза, которые активируют синтез клеток шишковидной железы, тем самым обновляя и омолаживая эпифиз, что благоприятно сказывается на его функциях и выработке так необходимых нашему организму гормонов.
ВАЖНО!!! Эндолутен не является гормональным препаратом, этот препарат содержит пептиды, биорегуляторы шишковидной железы, в которой происходит уже секреция гормонов серотонина и мелатонина.
ЭПИФИЗ И КЛИМАКС У ЖЕНЩИН
Женолутен — пептиды яичников
Исходя из исследований зарубежных учёных, в период менопаузы около 50% женщин отмечают у себя проблемы с засыпанием. Связано это с тем, что в этот период, в организме женщины преобладают инволютивные процессы: снижается репродуктивная, а в последствии и гормональная функции яичников.
При старении внутри организма происходят существенные изменения и трансформации в органах и тканях и они не обходят стороной эпифиз. С возрастом орган постепенно утрачивает свою функцию и тем самым вырабатывает меньшее количество мелатонина.
Исследования подтвердили, что при наступлении менопаузы изменяется секреция мелатонина и, как следствие, можно наблюдать не только проблемы с засыпанием, но и формирование различных других заболеваний. Чтобы помочь женскому организму в период менопаузы и облегчить симптоматику климактерического периода Институтом геронтологии и Биорегуляции были разработаны пептиды, биорегуляторы яичников. Препарат Женолутен содержит пептиды, стимулирующие синтез клеток яичников, тем самым обновляя половые функции матки.
Щитовидная железа
Щитовидная железа представляет собой небольшую железу внутренней секреции, расположенную на передней поверхности шеи и состоящей из двух половин, объединенных между собой перешейком. Она продуцирует те самые тиреоидные гормоны, которые имеют тесную взаимосвязь с ТТГ.
Тиреоидные гормоны представляют собой биологически активные вещества, в молекулах которых присутствует йод. Это тироксин (Т4) и трийодтиронин (Т3), которые регулируют процессы роста и развития организма, а также участвуют в регуляции скорости метаболизма. Они повышают потребность тканей в кислороде, а также способствуют повышению артериального давления, частоты и силы сердечных сокращений.
От тиреоидных гормонов зависит энергичность человека, его психологическая энергия и скорость протекания когнитивных процессов. Также они способствуют образованию глюкозы и в печени и ее использованию клетками, при этом они подавляют накопление гликогена. Кроме того, тиреоидные гормоны способствуют более быстрому разложению жира и препятствуют образованию нового.
Поджелудочная железа
Поджелудочная железа расположена в брюшной полости и является не только железой внутренней секреции, но и органом пищеварительной системы. Но ее гормонам отводится особенно большая роль в регуляции белкового, жирового и особенно углеводного обмена. К их числу принадлежат:
- Глюкагон – пептидный гормон, отвечающий за повышение уровня сахара в крови за счет поступления глюкозы в кровь в результате расщепления гликогена. Он также стимулирует выработку инсулина, способствует повышению артериального давления, частоты и силы сердечных сокращений. В высоких дозах он провоцирует расслабление кишечника. Но наиболее важен гормон для обеспечения возможности мобилизации организма в стрессовых ситуациях за счет обеспечения клеток источником энергии – глюкозой.
- Инсулин – отвечает за снижение уровня глюкозы в крови, что делает его одним из наиболее важных гормонов в регуляции обмена углеводов, а также белков и липидов. При дефиците инсулина или нарушениях чувствительности клеток к нему развивается сахарный диабет.
Надпочечники
Надпочечники – парные органы эндокринной системы, расположенные непосредственно над почками. Основными гормонами, синтезируемыми ими, являются:
- Адреналин – гормон страха, который синтезируется, когда человек попадает в стрессовую ситуацию, а также чувствует угрозу жизни. Он обеспечивает мгновенную мобилизацию организма, что приводит к кратковременному увеличению физических возможностей.
- Альдостерон – участвует в регуляции водно-солевого обмена, так как способствует задерживанию натрия и воды, но стимулирует выведение калия.
- Кортикостероиды представлены кортизолом, кортизоном и кортикостероном. Все они обладают мощным противовоспалительным действием и способны оказывать воздействие на весь организм. Также они принимают участие в поддержание нормального уровня сахара в крови, за счет его расщепления и запасания организмом в печени в виде гликогена, а также мышечного тонуса и кровяного давления.
Функционирование надпочечников контролируется гипофизом и гипоталамусом.
Мелатонин – гормон сна и молодости «третий глаз»: прощай, бессонница!
«Сон – лучшее лекарство», «с горем нужно переспать» – эти народные мудрости абсолютно правы. Множество научных исследований подтверждают: кто много спит, тот дольше живет и меньше болеет
В головном мозге есть небольшой орган – шишковидная железа или эпифиз, который древние называли «третьим глазом». Этой железой вырабатывается гормон мелатонин.
НОЧНОЙ ДИРИЖЕР
Именно ночью вырабатывается 70% суточного количества мелатонина. Именно он регулирует биоритмы — помогает приспосабливаться к смене дня и ночи, отправляет в зимнюю спячку животных и гонит нас в кровать с наступлением темноты.
Выработка гормона начинает расти в сумерки, достигает максимума с 0 до 4.00 утра и с рассветом падает.
Мы погружаемся в сон, а мелатонин принимается за работу – восстанавливает, ремонтирует, укрепляет. Ведь он – один из самых сильных природных иммуномодуляторов и антиоксидантов, наиболее мощный поглотитель свободных радикалов – нестабильных молекул, которые, разрушая ДНК, клетки и ткани, способствуют развитию рака и сердечных заболеваний.
Чтобы организм мог осуществлять бесперебойную работу, в нем содержится огромное количество витаминов, аминокислот, гормонов. Одна из этих аминокислот, а именно – триптофан, под действием солнечного света превращается в гормон эпифиза серотонин. А он, в свою очередь, в ночное время суток подвергается химическому и биологическому воздействию и переходит в гормон сна. Именно так чудодейственный гормон эпифиза синтезируется из серотонина, и попадает в кровь.
Серотонин и гормон мелатонин – два гормона, вырабатываемые эпифизом являются незаменимыми для нормальной жизнедеятельности человека.
Ученые утверждают: именно мелатонин способен подарить человечеству 10—15 лет дополнительной качественной жизни.
Наука утверждает, что если в вашей квартире по ночам горит свет, то вы болеете чаще, лишний вес набираете легче и стареете быстрее.
А днём мелатонин совсем не вырабатывается?
Вырабатывается, но в 30 раз меньше, чем днём. Электричество – это благо цивилизации. Но любая медаль имеет оборотную сторону. Сотни тысяч людей работают в ночную смену. Конечно, они спят днём. Этот сон восстанавливает силы, но не компенсирует нарушений суточного ритма работы гормональной системы. Чем больше стаж работы в ночное время, тем больше риск развития ожирения, атеросклероза, гипертонии, диабета и опухолей.
НЕ МЕШАЙТЕ ДИРИЖЕРУ.
Если вы любитель засиживаться за полночь и предпочитаете часть времени, отведенного на сон, занять делами, которые не успели сделать днем. Либо любите засыпать под мирные отсветы телевизора, сегодня я очень постараюсь вас убедить не делать так впредь.
Понимаю, если вы классическая «сова», то безумно трудно уложить себя спать в то время, когда вы полны сил и энергии, а жизнь только начинается.
Засиделись далеко за полночь у компьютера, читали до утра книгу или веселились на вечеринке? Вообще привыкли спать с ночником или под свет огней ночного города сквозь незадернутые шторы?
Будьте уверены: нужного количества мелатонина вы не получили.
УЧЕНЫЕ ПОЛАГАЮТ, ЧТО ИМЕННО ИЗЛИШНЯЯ ОСВЕЩЕННОСТЬ УКОРАЧИВАЕТ ЖИЗНЬ ЖИТЕЛЯМ БОЛЬШИХ ГОРОДОВ, И ДАЖЕ ВВЕЛИ СПЕЦИАЛЬНЫЙ ТЕРМИН «СВЕТОВОЕ ЗАГРЯЗНЕНИЕ»
Функции гормона мелатонина в организме.
• Он регулирует наши биоритмы, периодичность бодрствования и сна и, когда наступает темнота, вызывает состояние сонливости.
• Когда мы меняем часовой пояс, мелатонин помогает процессу адаптации и создаёт новые биоритмы.
• Он принимает участие в регуляции углеводного и жирового обмена, снижает уровень холестерина в крови.
• Мелатонин нормализует артериальное давление.
• Стимулирует иммунную систему и защищает нас от инфекционных и онкологических заболеваний.
• Он обладает антиоксидантными свойствами и замедляет старение организма. Мелатонин называют гормоном молодости. Это самый сильный поглотитель свободных радикалов в нашем организме и защитник от опухолевых процессов.
• Принимает участие в регуляции функций желудочно-кишечного тракта
• Участвует в регуляции функций головного мозга, повышает выработку гормона удовольствия серотонина, снижает синтез гормона стресса кортизола и защищает нас от стрессов и депрессий.
С возрастом производство мелатонина уменьшается, и это является сигналом для всех остальных систем организма, что настало время сдаваться, пора стареть.
Как проявляется недостаток мелатонина в организме?
Этот вопрос достаточно изучен в экспериментах на животных. У группы животных удалялись рецепторы, чувствительные к мелатонину и в результате у них быстрее разрушались клетки накопившимися свободными радикалами, они быстрее старели, у самок раньше начиналась менопауза. У животных развивались ожирение и онкологические заболевания, а также снижалась чувствительность тканей к инсулину, которая ведёт к развитию сахарного диабета 2 типа.
Если в крови человека будет недостаточное количество гормона эпифиза, то:
1. Первые признаки старения появятся уже в 17 лет;
2. Накопление вредных свободных радикалов увеличится в 5 раз;
3. Через полгода человек наберет от 5 до 10 кг лишнего веса;
4. Менопауза у женщин может наступить в 30 лет;
5. Образование раковой опухоли груди у женского населения увеличится до 80%.
Принимать мелатонин лучше курсом — летом и осенью — по 1-1,5 мг исключительно на ночь. Сколько раз в неделю — не важно, можно 2-3 или больше, если вы мучаетесь бессонницей. Ведь мелатонин, не будучи снотворным, облегчает засыпание, снижает частоту ночных пробуждений.
У вас аврал? Примите мелатонин, даже если ложитесь в 4 часа утра. Вы получите необходимое суточное количество гормона, да и заснете быстрее – ведь переутомление вызывает, в том числе и бессонницу.
С помощью мелатонина можно быстро переводить свои биологические часы после перелетов через несколько часовых поясов. Чтобы перестроиться на новый суточный режим, прилетев на место, примите на ночь 1,5 г мелатонина. И уснуть сможете, и весь следующий день будете бодрее. То же сделайте и по возвращении домой.
Противопоказан мелатонин диабетикам (плохо сочетается с антидиабетическими лекарствами), беременным и кормящим, детям до 16 лет, тем, кто подвержен депрессиям, а также при аутоиммунных заболеваниях и в редких случаях аллергии на мелатонин.
5 ПОЛЕЗНЫХ СОВЕТОВ
1. Задергивайте на ночь окна плотными шторами.
2. Не спите с включенным ночником или телевизором.
3. Вставая ночью, не зажигайте свет. Для освещения туалета достаточно тусклой лампочки-ночника, включающейся в розетку.
4. Если засиживаетесь допоздна, освещение комнаты должно быть неярким и уж точно не лампой дневного света.
5. Старайтесь засыпать не позже полуночи: максимум мелатонина вырабатывается с 0 до 4 утра.
Спать ночью, много и регулярно — лучший совет, который можно дать человеку, который хочет быть здоровым и красивым! Вы только посмотрите, как недостаток мелатонина влияет на наш организм. Не знаю как Вам, а мне резко захотелось спать!
Спите, придерживайтесь правильного питания и БУДЕТЕ ЗДОРОВЫ!
Половые гормоны
Половые гормоны всех видов вырабатываются и у мужчин, и у женщин. Но у мужчин преобладают андрогены, а у женщин – эстрогены. Синтезируются они частично в надпочечниках, но в основном в яичниках и яичках.
Прогестерон
Прогестерон синтезируется образовавшимся после разрыва фолликула и наступления овуляции желтым телом. Это временная эндокринная железа, которая постепенно рассасывается. Прогестерон ответственен за подготовку эндометрия (внутреннего слоя матки) к прикреплению оплодотворенной яйцеклетки. Также он задействован в подготовке молочных желез к продукции грудного молока.
Причинами повышения уровня прогестерона выступают кисты желтого тела, опухоли яичников и матки, нарушения функционирования надпочечников, ХПН. При избытке прогестерона наблюдаются:
- маточные кровотечения;
- дискомфорт в боковой части низа живота, молочных железах;
- нарушения менструального цикла;
- повышение нервозности, склонности к депрессивным состояниям;
- быстрая утомляемость;
- резкий набор веса.
Дефицит прогестерона наблюдается при патологиях гипофиза, провоцирующих снижение ЛГ, маточных кровотечениях, сальпингоофорите. В таких ситуациях менструации затягиваются или прекращаются. При этом наблюдается увеличение сексуального влечения.
Эстрогены
Эстрогены синтезируются в яичниках у женщин, а у мужчин в яичках. У женщин они управляют развитием женских половых органов и вторичных половых признаков, а у мужчин ответственны за регуляцию деятельности простаты и яичек. Кроме того, эстрогены участвуют в жировом и минеральном обмене.
Избыток эстрогенов в организме возникает при ожирении, попадании в организм ксеноэстрогенов, дисфункции щитовидной железы, гипотиреозе. Повышение уровня эстрогенов сопровождается:
- увеличением чувствительности молочных желез;
- быстрым набором веса;
- нарушениями МЦ;
- выпадением волос;
- перепадами настроения;
- нарушениями работы кишечника;
- постоянной усталостью.
Дефицит эстрогенов в организме может наблюдаться при:
- заболеваниях внутренних половых органов;
- длительном приеме антагонистов ГнРГ;
- климаксе;
- после химиотерапии.
Если эстрогена вырабатывается в организме недостаточно, это может приводить к оволосению по мужскому типу, огрубению голоса, а также нарушению менструального цикла вплоть до отсутствия менструации. При дефиците эстрогенов наблюдается снижение работоспособности, слабость, нарушения сна, возникает раздражительность и пропадает сексуальное влечение.
Тестостерон
Тестостерон – мужской половой гормон, ответственный за формирование вторичных половых признаков и репродуктивную функцию. У мужчин он синтезируется в яичках, что контролируется ЛГ, и в небольших количествах – в надпочечниках. У женщин же продуцируют тестостерон надпочечники и в малых количествах яичники.
На уровень тестостерона влияет витамин D, который, как было обнаружено недавно, так же является гормоном и антиоксидантом. Но снижение его концентрации чаще всего обусловлено патологиями гипофиза и гипоталамуса, травмами яичек, бесплодием или недоразвитием яичек. Избыток тестостерона может свидетельствовать об опухолях в яичках или надпочечниках, гипертиреозе, поликистозе яичников.
Существует еще множество других гормонов, каждый из которых выполняет свою функцию в организме и важен для него. Это и мелатонин, отвечающий за нормальный сон, и ренин с ангиотензином, обеспечивающие контроль над артериальным давлением, и многие другие.