Статья на конкурс «био/мол/текст»: Прионные заболевания — феномен, открытый в двадцатом веке, и в нем же начавший играть большую роль: увеличение продолжительности жизни в развитых странах привело к тому, что все больше людей стало доживать до «своего Альцгеймера» или «своего Паркинсона». Природа нейродегенеративных заболеваний продолжает оставаться туманной, и ученые пока исследуют только отдельные их аспекты — например, причину развития именно в старческом возрасте или способность передаваться от одних видов живых существ другим.
«Био/мол/текст»-2012
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2012 в номинации «Лучшее новостное сообщение».
Спонсор конкурса — дальновидная компания Thermo Fisher Scientific.
Всё началось с того, что в 20 веке учёные заинтересовались природой необычных заболеваний человека и животных: куру, Крейтцфельда-Якоба, скрэпи. Заметное сходство патологии этих болезней дало основание для гипотезы об их инфекционности, что впоследствии было экспериментально подтверждено. Тогда возник вопрос о возбудителе данных заболеваний. Прежде чем был найден ответ, были выявлены необычайные свойства возбудителей: они не размножаются на искусственных питательных средах, устойчивы к высокой температуре, формальдегиду, различным видам излучений, действию нуклеаз. Очистка инфекционного материала и его изучение позволило провозгласить о том, что «во всём виноват» белок, который 30 лет назад получил название прион (от англ. prion — белковая инфекция).
Так, известные американские учёные — вирусолог и врач Д.К. Гайдушек, раскрывший инфекционную природу прионных болезней, в 1976 г. и биохимик С.Б. Прузинер, который определил прионы и разработал прионную теорию, в 1997 г., — были удостоены Нобелевских премий. Их работы стали импульсом для последующих исследований, благодаря которым были изучены новые виды прионных инфекций. Но, даже несмотря на неугасающий интерес к «прионной теме», образование прионов до сегодняшнего дня остаётся загадкой.
Способ продления жизни больных прионными болезнями
Изобретение относится к ветеринарии, а именно к лечению животных, больных таким инфекционным заболеванием как скрейпи, которое относится к прионным болезням. Для этого животному вводят экстракт бересты. Введение экстракта способствует задержке снижения массы тела и продлению жизни животного. 7 табл., 5 ил.
Изобретение относится к области медицины и ветеринарии и более конкретно оно относится к изысканию средств, которые могли бы быть использованы по крайней мере для увеличения продолжительности жизни людей и животных, инфицированных прионами.
Прионы (сокращение от английских слов «protein infections» — белок инфекционный) являются новым классом инфекционных патогенов, открытие и изучение которых произошло и осуществляется лишь в последние 50 лет, хотя заболевания, ныне относимые к прионным, известны у животных более 200 лет, а у людей — с начала XX века.
Прионы отличаются от всех прочих инфекционных патогенов (вирусов, бактерий и др.) тем, что у них отсутствует какой-либо геном, то есть ДНК или РНК. Предполагается, что именно такие инфекционные агенты вызывают группу неизлечимых дегенеративных заболеваний центральной нервной системы человека и животных. Наиболее известные из них у человека — это болезнь Крейтцфельдта-Якоба (БКЯ) и синдром Гертсмана-Штраусслера-Шейнкера (ГШШ), а у животных — скрейпи овец и губчатая энцефалопатия крупного рогатого скота, называемые иногда в средствах массовой информации чесоткой овец и коровьим бешенством или губчатым энцефалитом. Эти заболевания, независимо от того, у кого они возникли — у человека или животных, сопровождаются морфологическими изменениями тканей мозга и появлением в них амилоидоподобных бляшек, содержащих палочкообразные белковые агрегаты. Уникальная особенность этих заболеваний состоит в том, что они возникают не только в результате инфекции: известны спорадические и наследственные БКЯ и ГШШ, причем вне зависимости от своего происхождения болезнь может передаваться далее инфекционным путем.
По данным Всемирной организации здравоохранения (ВОЗ) и Международного эпизоотического бюро за 1986-2000 годы зарегистрировано около 200 тысяч случаев спонгиоформной энцефалопатии крупного рогатого скота, а также выявлено 85 случаев болезни Крейтцфельдта — Якоба у людей молодого возраста.
Несмотря на крупномасштабные исследования прионов, отмеченные двумя нобелевскими премиями (К.Гайдушек — 1976 г. и С.Прузинер — 1997 г.) до сих пор многие аспекты возникновения и развития прионных инфекций не ясны (продление возбудителем межвидового барьера, патогенная картина заболевания и др.). Нет также каких-либо сведений о средствах профилактики и лечения прионных болезней.
Авторами настоящего изобретения была неожиданно обнаружена способность продлевать жизнь животных, зараженных скрейпи, у такого природного продукта, как экстракт верхнего слоя коры березы — бересты, что позволяет рассматривать его как перспективнвное средство для профилактики прионных инфекций и для лечения людей и животных, больных прионными болезнями.
Исследования проводились на модельных животных — сирийских хомячках, которые инфицировались скрейпи. Использовался экстракт бересты производства ООО «Березовый мир» (г.Москва). Основным компонентом экстракта (свыше 70%) является бетулин.
Материалы и методы исследования
В качестве лабораторной модели использовали 25 сирийских хомячков 3-х недельного возраста, обоего пола, массой 25-30 г.
Каждое животное, находящееся в опыте, было идентифицировано по окраске и/или с помощью красителя — бриллиантового зеленого. Животных разбили на 3 группы: две (1-я и 2-я) — контрольные, одна (3-я) — опытная.
1-я группа (контроль безвредности препарата, 5 особей). Животных разделили на 2 клетки: группа 1 а — 3 хомячка (получали испытуемый препарат) и группа 16-2 хомячка (не получали препарат). Животные содержались в другом помещении отдельно от хомячков других групп.
2-я группа (контроль экспериментальной инфекции, 10 особей). Животных содержали в 2-х клетках по 5 хомячков в каждой. Все животные — самки.
3-я группа — опытная (10 особей)
Все животные данной группы получали испытуемый препарат по выбранной лечебно-профилактической схеме. Животных содержали в 2-х клетках по 5 хомячков в каждой. Одна клетка — 5 самок, другая — 5 самцов.
В качестве возбудителя скрейпи использовали штамм 263 К, хранившийся при -20°С. Возбудитель прошел 2 пассажа на сирийских хомячках. Инфекционный титр — 6,5 Ig LD50/мл;
Схема проведения эксперимента включала:
1) Введение испытуемого препарата с профилактической целью.
2) Экспериментальное заражение контрольных и опытных животных возбудителем скрейпи.
3) Введение испытуемого препарата с лечебной целью.
4) Прижизненные и посмертные исследования животных опытной и контрольных групп.
Испытуемый препарат разводили на жидком крахмале и вводили хомячкам перорально (через зонд) из расчета 100 мкг/г веса животного по следующей лечебно-профилактической схеме: 5 раз до инфицирования возбудителем скрейпи, 5 раз спустя 35 дней после инфицирования и 5 раз в терминальной стадии болезни.
Препарат дважды вводили 3 хомячкам группы 1а (контроль безвредности препарата) и 10 хомячкам группы 3. Животным группы 1а (2 хомячка) и группы 3 (5-ти хомячкам, оставшимся в живых), находящимся в терминальной стадии заболевания, препарат вводили дополнительно (5 раз в течение 5 дней). При этом 2 хомяка (самцы) погибли уже после 2 введений препарата, 3 хомячка (самки) получили препарат в полном объеме.
Экспериментальное заражение контрольных и опытных животных.
Подготовка инфекционного материала.
Стерильно из центра мозга хомячка с экспериментальной инфекцией скрейпи отбирали 3 г образца, растирали в стерильной ступке и разводили в 2,7 мл раствора Хенкса с антибиотиками (100 ед. стрептомицина). Материал переносили в стерильный флакон и центрифугировали на настольной угловой центрифуге при 2000 об/мин в течение 15 мин. Из отобранной после центрифугирования надосадочной жидкости брали 0,3 мл раствора и разводили в 2,7 мл раствора Хенкса (разведение 10-2) и использовали непосредственно для заражения.
Сирийских хомячков (группы 2 и 3) заражали приготовленной ex tempore суспензией мозга хомячка с экспериментальной инфекцией скрейпи в разведении 10-2 на растворе Хенкса в объеме 0,03 мл на животное (примерно 100 летальных доз). Животных инфицировали интрацеребрально путем введения в правую гемисферу большого мозга под легким эфирным наркозом. Контрольным животным (группа 1) вводили по 0,03 мл суспензии мозга интактных животных (разведение 10-2), приготовленной, как описано выше.
Вся работа с лабораторными животными проводилась в соответствии с рекомендациями ВОЗ.
Продолжительность эксперимента: 4,5 месяца (9 августа-24 декабря 2004 г.).
Прижизненные исследования животных.
Включали в себя контроль за поведением, внешним видом и весом животных: Взвешивание хомячков осуществляли с использованием электронных весов ВЭ-15И (ОАО «Масса», С.-Петербург, Россия), утром, до кормления, с периодичностью 3-4 дня (2 раза в неделю).
Экспериментальных животных оценивали по следующим признакам:
1. Неспецифические признаки:
— состояние кожного покрова (волосяного покрова, блеск, тусклость, наличие и характер лишенных волос участков);
— состояние слизистых (глаза, ротовая полость, целостность, наличие эрозий, язв, рубцов, кровоизлияний);
— подвижность;
— аппетит.
2. Специфические признаки:
Начальная стадия:
изменение поведения (неадекватная реакция на внешние раздражители (свет, звук, прикосновение, причинение боли)
— возбуждение или заторможенность реакций. Стадия развития неврологической симптоматики заболевания:
— нарушение двигательных функций (нарушение координации, тремор, нарушение походки, слабость в конечностях, парезы);
— резкое похудание (кахексия).
Терминальная стадия (необратимые изменения):
— неподвижность;
— паралич конечностей и дыхательных мышц.
Посмертные исследования животных.
1) Гистологические исследования.
У экспериментальных животных находящихся в последней фазе терминальной стадии заболевания под глубоким эфирным наркозом стерильно забирали головной мозг и селезенку и помещали либо в 4% раствор нейтрального формалина (для гистологических исследований), либо в морозильник на -20°С.
Гистологические препараты готовили по общепринятой методике. Из головного мозга вычленяли кусочки ткани из различных его отделов: коры полушарий большого мозга, подкорковых ядерных групп, мозжечка, продолговатого и спинного мозга. Готовили парафиновые препараты, стандартным способом получали срезы и окрашивали их гематоксилином и эозином и Конго красным.
Результаты анализировали в световом микроскопе «Biostar» (США) при увеличении в 200-600 раз.
2) Иммуноблоттинг (ИБ). Иммунологическое обнаружение возбудителя скрейпи в ЦНС экспериментальных животных осуществляли с использованием тест-системы «Prionics-Check Western» (Phonics AG, Швейцария). Положительным контролем служил положительный антиген тест-системы. В качестве первичных моноклональных антител использовали моноклональные антитела к белку PrP: прилагаемые к тест-системе мышиные анти-PrP IgG1 (рабочее разведение 1:5000), Am 308 (аналог коммерческих антител Am 3F4, титр 1:5000) и Am 6H4 (титр 1:5000). Работу с тест-системой осуществляли согласно инструкции исполнителя.
Статистическая обработка результатов.
При статистической обработке экспериментальных данных вычисляли среднеарифметические величины, их доверительные интервалы и проводили оценку достоверности различий числовых результатов по критерию Стьюдента. Разницу считали статистически достоверной при р<0,05.
Прижизненные исследования животных
Клиническая картина заболевания у опытных (2 и 3-я группы) и контрольных (1-я группа) животных с экспериментальным скрейпи.
Развитие экспериментального скрейпи изучали у 20 сирийских хомячков (группа 2 и 3).
Ежедневное наблюдение за опытными животными не выявило изменений со стороны шерстяного покрова у опытных и контрольных животных в течение 2-2,5 месячного срока. На 10-12 неделях наблюдения у опытных животных была отмечена некоторая вялость, взъерошенность шерстяного покрова и снижение двигательной активности, сопровождающееся потерей аппетита. На 16-й неделе у экспериментально зараженных хомячков наблюдали выпадение шерсти и сильный тремор головы. В этот период опытные животные значительно отличались в развитии от контрольных: вес тела снижался на 20-40%, постепенно прогрессировала слабость задних конечностей, парезы. Животные при движении опрокидывались на спину и с трудом принимали прежнее положение тела. Отмечали замедленную реакцию на раздражители. Продолжительность инкубационного периода составила 3-3,5 месяца, продолжительность заболевания составляла 0,5-1,5 месяца. Основными симптомами развития экспериментального скрейпи являлись: выпадение шерсти, атрофия мышц, тремор, развитие парезов конечностей и туловища. При этом летальность среди инфицированных хомячков к концу срока наблюдения составила 95% (пало 19 животных из 20 под наблюдением). Как правило, развитию неврологической симптоматики предшествовало: снижение веса (до 40% от максимального). Среди контрольных животных (группа 1) гибели не отмечено.
Обобщенные данные по развитию скрейпи в группах 2 и 3 представлены в таблице 1.
Как видно из таблицы 1, введение препарата не влияет на показатели инкубационного периода и на продолжительность развития специфической симптоматики скрейпи у сирийских хомячков (р>0,05). Отмечена разница у самцов и самок по чувствительности к скрейпи. Самцы гибли быстрее, поэтому в качестве основного критерия при сравнении показателей контрольных и опытной групп животных были взяты однополые животные — самки.
Расчеты достоверности полученных результатов представлены в таблицах 2-5.
Изучение динамики массы тела сирийских хомячков с экспериментальным скрейпи.
Первичные данные по динамике массы тела сирийских хомячков групп 1, 2 и 3 представлены в Таблице 6.
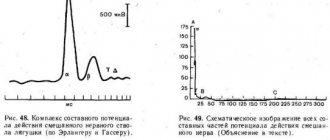
Графические изменения массы тела (средний показатель группы) у хомячков, не получавших (группа 2) и получавших испытуемый препарат (группа 3), в сравнении с массой тела контрольных хомячков показаны на фиг.1. Сравнение кривых динамики потери массы тела самок и самцов групп 2 и 3 представлено на фиг.2, 3 и 4.
Видно, что применение испытуемого препарата по лечебно-профилактической схеме у хомячков группы 3 приводило к задержке потери массы тела более чем на 2 недели, по сравнению с хомячками группы 2 (22 октября и 8 октября соответственно).
Введение препарата третий раз 5 хомячкам группы 3, находящимся в последней фазе терминальной стадии развития заболевания, привело к замедлению падения массы тела и сроков гибели 3-х самок опытных животных, по сравнению с аналогами группы 2.
Выживаемость сирийских хомячков с экспериментальным скрейпи. Обобщенные данные по срокам жизни сирийских хомячков с экспериментальным скрейпи представлены в таблице 7.
Как видно из таблицы 7, сроки жизни хомячков групп 2 и 3 варьируют в широких пределах, средние показатели практически идентичны (р>0,05), если не принимать во внимание пол животных.
Однако отмечена разница по срокам жизни у самок сирийских хомячков 2-й и 3-й групп. Самки группы 2 погибали в среднем на неделю раньше, чем самки группы 3, получавшие испытуемый препарат. Следует подчеркнуть, что одно животное (самка, серый окрас), получавшее препарат, продолжало жить еще 3 недели после завершения эксперимента.
Самцы сирийских хомячков более чувствительны к скрейпи, чем самки. Они погибали в среднем на неделю раньше, чем зараженные самки.
Посмертные исследования животных
Гистологические исследования мозга сирийских хомячков с экспериментальным скрейпи.
Для исследования брали мозг животных, находящихся в последней фазе терминальной стадии заболевания. Исследовали по одному животному каждой группы.
У животных, находящихся в терминальной стадии заболевания, отмечены специфические изменения, характерные для инфекции скрейпи: спонгиоформные изменения в корковом слое и гиппокампе, гибель нейронов, диффузная пролиферация астроглии, субэпендимарный глиоз, амилоидоз стенок сосудов и другие. Отмечено образование амилоидных бляшек непосредственно в ткани ЦНС.
Обнаружение PrPSc в ЦНС сирийских хомячков с экспериментальным скрейпи методом иммунного блоттинга.
РгРSc отличается от нормального PrPc по устойчивости к протеазе К: после обработки протеазой нормальная форма PrP разрушается, в то время как молекулярный вес PrPSc уменьшается от его первоначального размера 32-35 kD к меньшему размеру 27-30 kD. Остающийся протеазо-устойчивый фрагмент PrPSc выявляется иммуноблотингом как PrP27-30 (фиг.5).
Иммунологическое обнаружение возбудителя скрейпи в образцах мозга экспериментальных животных осуществляли, как описано выше.
В качестве первичных антител использовали моноканальные антитела 308 (аналог 3F4), титр 1:5000.
Изложенные результаты исследований позволяют заключить, что испытуемый препарат (экстракт бересты) является безвредным и не оказывает патологического воздействия на организм хомячков. Все животные 1-й контрольной группы были клинически здоровыми в течение всего периода наблюдения.
При интрацеребральном заражении сирийских хомячков заболевание скрейпи развивается специфически. Инкубационный период в среднем составил у животных в группе 2 — 73,3±6,21 дней, в группе 3 — 75,7±8,10 дней (самцы — 72,8±2,86 дней, самки — 78,6±10,31 дней). Продолжительность развития болезни до гибели животных в группах 2 и 3 составила 22,1±4,68 и 19,5±9,63 (самцы — 15,4±1,36 и самки — 23,6±12,24) дней соответственно.
Основными симптомами развития экспериментального скрейпи являлись: снижение массы тела, выпадение шерсти, атрофия мышц, тремор, развитие парезов конечностей. Потеря веса у животных наблюдалась за 1-3 недели до развития клинических проявлений заболевания. Летальность среди инфицированных хомячков к концу срока наблюдения составила 95% (пало 19 животных из 20 инфицированных).
Посмертные исследования животных гистологическим методом и идентификация возбудителя в иммуноблоттинге подтвердили эффективность экспериментального заражения животных 2-й и 3-й групп. Гистологическими исследованиями подтверждено наличие специфических морфологических маркеров развития скрейпи в ЦНС сирийских хомячков. В корковом слое головного мозга отмечена гибель нейронов, спонгиоз, пролиферация астроглии и астроглиоз, амилоидоз. Прионный белок PrPSc был обнаружен в ЦНС сирийских хомячков с экспериментальным скрейпи в группах 2 и 3.
Использование испытуемого препарата с лечебно-профилактической целью показало следующее (сравнение самок 2-й группы с самками 3-й).
Отмечена 2-недельная задержка снижения массы тела у животных, получавших испытуемый препарат, по сравнению с хомячками, не получавшими препарат. Причем самки теряли вес на 3 недели позже, чем контрольные аналоги, а самцы — на 1 неделю.
Установлено, что продолжительность жизни самок группы 3, получавших испытуемый препарат, была в среднем на 1 неделю больше, чем у аналогов группы 2. При этом после третьего введения испытуемого препарата в терминальной стадии болезни одна самка продолжала жить еще 21 день.
Посмертные изменения были аналогичны у животных обеих групп.
На основании результатов проведенных экспериментов можно сделать общее заключение о том, что в остром опыте было отмечено воздействие испытуемого препарата на организм экспериментально зараженных хомячков. Эффект воздействия заключался в задержке времени начала снижения массы тела у опытных животных и увеличении продолжительности их жизни.
Способ продления жизни животного, инфицированного скрейпи, путем введения ему экстракта бересты.
Биологическая сущность прионов
Рисунок 1. Метафора нейродегенеративного поражения мозга — это губка, в которую превращается нервная ткань в результате массовой гибели нейронов.
Молекула приона не является чем-то экзотическим: в «нормальной» форме она имеется на поверхности нервных у каждого из нас. При этом мы отлично себя чувствуем, и наши нервные клетки живы и здоровы. Однако это всё до тех пор, пока наш нормальный белок не «переродится» в аномальную форму. А если это случится, то приведёт к ужасающим последствиям: инфекционная форма прионов имеет свойство «склеиваться» с другими молекулами и, мало того, «конвертировать» их в эту же самую форму, вызывая «молекулярную эпидемию». В результате этой полимеризации на нервной клетке появляются токсичные белковые бляшки , и она погибает [1]. На месте погибшей клетки образуется пустота — вакуоль, заполненная жидкостью. С течением времени будет исчезать один нейрон за другим, а в мозге — образовываться всё больше «дыр», пока, наконец, мозг не превратится в губку (рис. 1), за чем неминуемо последует смерть.
Существует упрощенное представление, что полимеризованные прионные фибриллы «протыкают» нейрон, что вызывает его гибель. На самом деле это не совсем так: предшествующие фибриллярной стадии сферические агрегаты прионов также обладают токсичностью (по крайней мере, для болезни Альцгеймера): «Альцгеймеровский нейротоксин: ядовиты не только фибриллы». — Ред.
Но как может нормальный природный белок (обозначается PrPC) вдруг стать патологическим (PrPSc; Sc — от слова «scrapie»)? Что должно произойти? Как и в случае «обычной» инфекции, для такой трансформации необходима встреча с молекулой инфекционного приона. Существуют два пути передачи этой молекулы: наследственный (за счёт мутаций в гене, кодирующего белок) и инфекционный. То есть внедрение приона может произойти неожиданно — например, при употреблении в пищу недостаточно хорошо прожаренного или сваренного мяса (в котором должна присутствовать форма PrPSc), при переливании крови, при трансплантации органов и тканей, при введении гормонов гипофиза животного происхождения.
И тогда происходит удивительное событие: нормальные молекулы белка, контактируя с патологическими, сами превращаются в них, изменяя свою пространственную структуру (механизм трансформации остаётся загадкой и по сей день) [1]. Таким образом прион, как самый настоящий инфекционный агент, заражает нормальные молекулы, запуская цепную реакцию, разрушительную для клетки.
Отдельные нозологические единицы
Прионные болезни человека видоспецифичные. В основном они распространяются только среди особей одного вида. Но учеными была продемонстрирована межвидовая передача (преодоление межвидового барьера): это произошло у скрепи овец с ее передачей коровам (коровье бешенство). Передача заболевания от животного к человеку, несмотря на многие подозрения, не была продемонстрирована.
Ряд заболеваний имеет наследственное происхождение, часть является инфекционной. Иногда болезнь возникает неожиданно, без возможности профилактики.
Куру
Болезнь существовала только в Папуа-Новой Гвинее в племенах людоедов, потреблявших мозги мертвых. Она проявляется тремором («куру» означает «тремор»), нарушениями речи, равновесия (атаксия). Через несколько месяцев наступает смерть. После остановки каннибализма, заболевание куру исчезло.
Болезнь Крейцфельдта-Якоба (Creutzfeldt-Jakob disease)
Это редкое расстройство, поражающее пожилых людей (чаще всего 50-70-летних). Его течение относительно быстрое, смерть наступает через несколько месяцев (до года) от проявления первых симптомов. Нейроны быстро гибнут, развивается прогрессивная деменция, не имеющая известного лечения. Существует некоторая наследственная предрасположенность к этому заболеванию:
- Спорадическая форма. Заболеваемость составляет 1-2/1000000. Проблемы начинаются примерно в возрасте 65 лет. Расстройство возникает в виде острого прогрессирования деменции (в течение 2-3 месяцев), атаксии, миоклонуса. Возможностей, как продлить жизнь нейронам при этом прионом заболевании, нет, пациент умирает через 5-12 месяцев после появления первых симптомов.
- Ятрогенная форма. Возникала у пациентов, получавших гормон роста человека из трупных гипофизов (сегодня он готовится рекомбинантно), пересадкой твердых оболочек, перикарда, роговицы. Существует риск нейрохирургической передачи. Заражение возможно также при переливании.
- Семейная форма. Это генетическая форма с мутацией в гене PRNP и психоневрологической симптоматикой.
- Новый вариант. Характеризуется психиатрическими симптомами (тревога, депрессия, изменения в поведении), прогрессирующим мозжечковым синдромом, миоклонусом, другими неврологическими симптомами. В отличие от спорадической формы, новый вариант типичен медленным развитием вирусной инфекции; прионная болезнь затрагивает более молодые возрастные группы. Передача происходит алиментарным путем (при потреблении мяса пораженных животных). Инкубационный период – более 10 лет. В мире на сегодняшний день погибло около 200 человек.
- Детский вариант болезни Крейцфельдта-Якоба – болезнь Альпера. Имеет те же проявления, что и заболевание у взрослых; в дополнение сопровождается стеатозом печени.
Болезнь Герстманна-Штрюсслера-Шейнкера (Gerstmann-Sträussler-Scheinker disease)
Болезнь Герстманна-Штрюсслера-Шейнкера – это очень редкое аутосомно-доминантное наследственное заболевание, начинающееся в 3-4-ой декаде жизни. Проявляется медленным замедлением работы нейронов прионами, прогрессирующей дисфункцией мозжечка и спинного мозга. Признаки:
- атаксия;
- пирамидные симптомы;
- дизартрия;
- дисфагия;
- постепенно развивающаяся деменция.
Статья в тему: Упражнения при плоскостопии у детей — комплекс тренировок дома с видео
В начале расстройства могут возникнуть апатия, депрессия. Средняя продолжительность заболевания – около 4-5 лет. Было описано несколько мутаций PRNP, связанных с этим расстройством.
Фатальная фамильярная инсомния (Fatal familiar insomnia)
Это очень редкое заболевание, приводящее к дегенерации ядра таламуса. Основные симптомы:
- прогрессирующая бессонница;
- вегетативная и эндокринная дисфункция;
- дизартрия;
- атаксия;
- миоклонус;
- пирамидные симптомы.
Дистрофия мозга по воздействием вируса приона
Развиваются когнитивные нарушения, появляются спутанность сознания и галлюцинации. В терминальной стадии развивается полная инсомния. Пациенты умирают в течение 3 лет от проявления первых признаков. Заболевание связано с мутацией PRNP D178N-129M. Существует также спорадическая форма расстройства.
Некоторые сведения о прионах
Исследователи отмечают:
- прионный белок включает 254 аминокислотных остатка и «весит» 33–35 килодальтон [2];
- ген, кодирующий белок PrP, найден у человека, млекопитающих и птиц [1];
- для полного уничтожения прионного белка нужна температура не менее 1000 градусов [1]!
- возможно, прионы принимают участие в межклеточном узнавании и клеточной активации [3];
- не исключено, что функцией прионов является подавление возрастных процессов [3];
- при развитии клинических проявлений прионных заболеваний нет ни признаков воспаления, ни изменений в крови;
- предполагается, что прионы участвуют в развитии шизофрении и миопатии;
- механизм действия прионов и их превращения из нормальной формы в патологическую остаётся неясным.
2.Причины
Фатальная семейная бессонница – наследуемое прионное заболевание. Лишь на стыке двух веков удалось установить непосредственную причину, которая кроется в мутации одного из генов (замена аспарагина производной от него кислотой), в результате чего организм начинает продуцировать белок прионного типа. Накапливаясь в таламусе, прионы вызывают лавинообразную дегенерацию и перерождение функциональной ткани в амилоидные бляшки, которые, в свою очередь, грубо нарушают проводимость нейронных импульсов. Дезорганизуется циркадный ритм (чередование сна и бодрствования), а затем и ряд других функций и показателей, – в частности, артериальное давление, работа эндокринных желез, терморегуляция и т.д.
Посетите нашу страницу Терапия
Условия возникновения заболеваний
Условия возникновения прионовых болезней уникальны. Они могут формироваться по трём сценариям: как инфекционные, спорадические и наследственные поражения. В последнем варианте главную роль играет генетическая предрасположенность [2].
Знаменитый исследователь прионов Стэнли Прузинер (Stanley Prusiner) выделяет две поразительные особенности, присущие таким нейродегенеративным заболеваниям, как болезнь Крейтцфельда-Якоба, болезнь Альцгеймера и болезнь Паркинсона. Первая заключается в том, что более 80% случаев заболевания — спорадические (то есть, случайные, возникающие «сами собой»). Вторая: несмотря на то, что большое количество мутантных белков, специфичных к определённой болезни, экспрессируется в процессе зародышевого развития, формы наследования этих нейродегенеративных заболеваний проявляются позже. Это предполагает, что некоторые процессы происходят во время старения, которое «дает волю» болезнетворным белкам [5]. Более 20 лет назад автор утверждал, что данный процесс включает случайный рефолдинг (пересворачивание) белка в неправильно свёрнутый, что соответствует переходу в инфекционное состояние — прион.
Интересные факты насчет болезни Альцгеймера: ее вероятность может повышаться вследствие хронического недосыпания («Новый шаг к пониманию болезни Альцгеймера: возможно, недосыпание является одним из факторов риска»), а сам альцгеймеровский нейропептид (β-амилоид Aβ) может быть частью системы врожденного иммунитета («Возможно, β-амилоид болезни Альцгеймера — часть врождённого иммунитета»). — Ред.
В последнее десятилетие интерес к этой теме возобновился в связи с возможностью развития диагностики и эффективной терапии [5]. Появилось множество различных объяснений для возрастных нейродегенеративных болезней, — например, окислительная модификация ДНК, липидов и/или белков; соматические мутации; измененный врождённый иммунитет; экзогенные токсины; несоответствия ДНК—РНК; нарушение работы шаперонов; отсутствие одного из аллелей гена [5]. Альтернативным комплексным разъяснением служит то, что различные группы белков могут формировать прионы. Несмотря на то, что небольшое количество прионов может быть удалено посредством путей белковой деградации, их чрезмерное накопление с течением времени позволяет прионам самостоятельно распространяться в организме (рис. 2), что приводит к нарушению деятельности центральной нервной системы [5].
Рисунок 2. Процессы нейродегенерации, вызванной прионами. Сверху: накопление «нормального» прионного белка повышает его вероятность перехода в токсичную конформацию, которая описывается бóльшим содержанием β-структуры. Прионы наиболее патогенны в форме олигомеров; после образования фибрилл токсичность снижается. В зависимости от того, о каком конкретно прионном белке идет речь, в патологическом состоянии он может образовывать бляшки, клубки или тельца включения. Возможные пути лекарственного вмешательства: (I) снижение кон белка-предшественника; (II) ингибирование образования прионной формы; (III) уничтожение токсичных агрегатов. Снизу: Наследственная старческая нейродегенерация объясняется двумя событиями: наличием мутантной формы предшественника и образованием из него приона, готового к олиго- и полимеризации с образованием токсичных форм.
[5]
Лабораторная диагностика и лечение
Диагностика базируется на внутримозговом заражении мышат или хомяков, у которых медленно (до 150 дней) развивается соответствующее заболевание, если пациент был болен [2]. Часто проводится гистологическое исследование головного мозга погибших животных [2].
К сожалению, до настоящего времени еще не разработаны эффективные методы лечения прионовых болезней, хотя попытки предотвратить конформационный переход нормального белка в аномальный производятся. Поэтому самым надёжным способом предупреждения развития инфекционных форм является профилактика [2].
Особенно актуальным становится решение «прионного вопроса» в связи с нарастающей угрозой возникновения эпидемии через инвазивные медицинские операции и даже при приёме лекарственных средств.
Бессонница
Частые пробуждения, проблемы с засыпанием, чувство усталости по утрам — все это признаки нарушения сна.
При любых заболеваниях, в том числе, инфекционных, организм расходует резервы, питательные вещества — белки, аминокислоты, витамины и микроэлементы. Все они нужны для того, чтобы организм выполнял жизненно важные функции — восстанавливал ткани, эффективно справлялся с болезнью.
Все другие потребности временно отодвигаются на второй план. В том числе и поддержание необходимого уровня нейромедиаторов в головном мозге. Нейромедиаторы — это биологически активное химическое вещество, передающее электрохимический импульс от одной нервной клетки к другой. В первую очередь затрагиваются тормозные нейромедиаторы, которые обладают успокаивающим, расслабляющим действием. Это одна из причин, почему после стрессов и болезней возникает бессонница.
Немаловажен и психологический аспект. Любой стресс и болезнь занимают наши мысли, мы привыкаем тревожиться и думать о них. Когда заболевание или стрессовая ситуация отступают, мы не всегда способны сразу переключиться на позитивное мышление.
В целом до трех дней после болезни нарушение сна может быть допустимым. Если ситуация не меняется, можно говорить о непростом течении болезни. Это означает, что нейромедиаторы вызывают целый каскад биохимических и гормональных реакций, из-за чего биологические функции организма сбиваются. Наладить нормальный режим сна может помочь невролог, сомнолог или врач превентивной медицины, который назначит пациенту щадящее лечение, способное быстро восстановить его сон.
Перспективы
По-видимому, интерес к прионам не угаснет до тех пор, пока предположения на их счёт полностью не подтвердятся и не будут найдены эффективные способы лечения прионных заболеваний. В статье [6] говорится о необходимости современного исследования, которое требует тщательного рассмотрения чужеродных прионов в экстраневрональных тканях.
В качестве модельных объектов авторы использовали мышей: две линии, которые трансгенно экспрессировали овечий прионный белок, и одну линию, которая экспрессировала человеческий прионный белок (рис. 3). Задачей было сравнить эффективность межвидовой передачи инфекции посредством тканей мозга и селезёнки. Внутримозговое заражение чужеродным прионным белком выражалось в отсутствии или небольшом количестве инфекционного агента в мозгах этих мышей. Однако инфекционные чужеродные прионы обнаруживались в селезёнке на более ранних этапах заражения в сравнении с моментом, когда были использованы нейротропные прионы, тем самым определяя, что лимфатическая ткань может быть более пермиссивной к распространению чужеродных прионов по сравнению с мозгом.
Рисунок 3. Способность приона хомяков Sc237 заражать и передаваться при введении в мозг или селезенку трансгенным мышам, имеющим прионный белок PrP овцы (tg338; белые мыши) или человека (tg7; серые мыши). Число заболевших/инъецированных мышей показано в скобках; ниже приведено среднее время жизни (в днях).
[6]
Чем вызвана эта предпочтительная репликация прионов в лимфатических тканях, пока неизвестно. Однако полученные данные показывают, что человек может быть более чувствительным к чужеродным прионам, чем предполагалось ранее на основании присутствия прионов в мозгу, и по этой причине бессимптомный переносчик прионной болезни может быть не распознан. Это ещё раз подтверждает, что такая могущественная биомолекула как прион таит в себе немало загадок, раскрытие которых, возможно, поможет в понимании ряда неразрешимых проблем человечества…
3.Симптоматика, диагностика
Фатальная семейная бессонница манифестирует в зрелом возрасте, причем триггерный (пусковой) механизм до сих пор не вполне ясен. Главным, осевым симптомом заболевания является полная неспособность человека уснуть. Соответственно, мозг, лишенный жизненно необходимого ему режима и вынужденный беспрерывно бодрствовать, все больше истощается. Распространение прионов и трансформация мозгового вещества вызывает также ряд грубых неврологических и психических нарушений вплоть до деменции (утрата памяти и интеллекта), галлюцинаций, аффективных и двигательных расстройств, в терминальной фазе – комы. Симптоматика прогрессирует и утяжеляет психосоматический статус пациента от полугода до нескольких лет (в развитии болезни различают четыре стадии), после чего результирует неизбежным летальным исходом.
Общей характеристикой всех прионных инфекций является сложность диагностики. Окончательный диагноз устанавливается, как правило, патоморфологически при посмертном вскрытии. При подозрении на фатальную семейную бессонницу необходимо, прежде всего, тщательное медико-генетическое изучение анамнеза. Назначают также визуализирующие томографические исследования; иногда информативен лабораторный анализ спинномозговой жидкости, отбираемой посредством пунктирования.
О нашей клинике м. Чистые пруды Страница Мединтерком!
Литература
- Абрамова З.И. Исследование белков и нуклеиновых кислот. Казань: Казанский государственный университет, 2006. — 157 с.;
- Новиков Д.К., Генералов И.И., Данющенкова Н.М. Медицинская микробиология. Витебск: ВГУ, 2010. — 597 с.;
- Прудникова С.В. Микробиология с основами вирусологии. Красноярск: ИПК СФУ, 2008;
- Поздеев О.К., Покровский В.И. Медицинская микробиология. М.: Гэотар-мед, 2001. — 765 с.;
- S. B. Prusiner. (2012). A Unifying Role for Prions in Neurodegenerative Diseases. Science
.
336, 1511-1513; - V. Beringue, L. Herzog, E. Jaumain, F. Reine, P. Sibille, et. al.. (2012). Facilitated Cross-Species Transmission of Prions in Extraneural Tissue. Science
.
335, 472-475; - Carolina Pola. (2012). Prion escape to spleen. Nat Med
.
18, 360-360; - Элементы: «10 фактов о прионах и амилоидах»;
- Элементы: «Геометрия белковых тел»;
- Charles Weissmann. (2012). Mutation and Selection of Prions. PLoS Pathog
.
8, e1002582.