Мультисистемная атрофия – прогрессирующее нейродегенеративное заболевание, симптоматически относящееся к группе патологий «паркинсонизм-плюс». Его также классифицируют как патологию вегетативной системы. Мультисистемная атрофия характеризуется необратимым поражением определенных участков головного мозга и частично спинного мозга, что не связано с действием определенных провоцирующих факторов. Лечение направлено на некоторое облегчение симптоматики, на данный момент не существует доказанных методов излечения или остановки прогрессии этого заболевания.
О заболевании
Множественной системной (мультифокальной, мультисистемной) атрофией называют обширную дегенерацию глиальных клеток во всех структурах головного мозга (ГМ). Сокращенно болезнь записывают МСА или MSA. Мультисистемная атрофия быстро прогрессирующее тяжелое заболевание, при котором в патологический процесс часто вовлекается спинной мозг, приводя к уменьшению тканей центральной нервной системы инвалидности.
Дегенерация провоцирует появление:
- слабоумия;
- дрожательного паралича — синдром паркинсонизма;
- дисфункциивегетативной нервной системы;
- атаксии мозжечка — расстройство двигательной и речевой функции;
- недостаточности пирамид — нарушается работа ЦНС.
Справка! МСА является редкой неизлечимой патологией, встречается преимущественно у мужчин. Заболеваемость составляет менее 6 случаев на 100000 населения.
Во время развития болезни поражаются подкорковые ядра (базальные ганглии) внутри полушарий ГМ.Они расположены между промежуточным мозгом и лобными долями. Состоят из полосатого тела, серого и белого вещества, нигральной (черной) субстанции, субталамического ядра. На гистологическом исследовании в олигодендроглиоцитах обнаруживаются накопления альфа-синуклеина во включениях цитоплазмы. Это несвойственно составу клеток нейроглии.
В результате дегенерации подкорковых ядер нарушается:
- координация движений;
- регуляция мышечного тонуса;
- чувствительность восприятия зрительных, слуховых и прочих раздражений;
- регулирование трофики, обмена, дыхания, мочеиспускания, иных вегетативных функций;
- выработка рефлексов, память, другая регуляция высшей нервной деятельности.
МСА чаще выявляют у людей старше 50 лет, которые работали с вредными и токсическими веществами, пестицидами, формальдегидом, растворителями. В группе риска состоят пациенты с болезнью Паркинсона, Альцгеймера. Опасность заключается в том, что патология вызывает необратимый процесс в мозге с гибелью нервных клеток. С момента появления симптомов длительность жизни не превышает 15 лет. Смерть чаще наступает вследствие нарушения дыхания или сепсиса.
Рисунок 1. Отображение мозга при томографии
До 2021 года в МКБ―10 мультисистемная атрофия была причислена к коду G90.3 под названием «полисистемная дегенерация». Сейчас в справочнике остался паркинсонический тип МСА под шифром G23.2 «MSA-P» и мозжечковый – G23.3 «MSA-C». В МКБ-10-КМ патология о под номером G90.3.
Патогенез
Мультисистемная атрофия – это прогрессирующая дегенерация и последующая гибель нервной ткани с поражением определенных структур центральной нервной системы. Этот процесс является необратимым, его скорость мало зависит от проводимого лечения.
Основная причина клеточного повреждения при мультисистемной атрофии – патологическое накопление α-синуклеина (альфа-синуклеина) в цитоплазме и ядрах нейронов и глии. В норме этот белок продуцируется в небольших количествах и концентрируется в основном в пресинаптических окончаниях нейронов. Он участвует в регуляции везикулярного транспорта (переноса веществ внутри клеток с помощью особых пузырьков) и, скорее всего, влияет на обмен дофамина.
При мультсистемной атрофии меняется структура α-синуклеина и нарушается процесс его естественной метаболической деградации. Он становится нерастворимым и начинает связываться с другими белками, формируя в цитоплазме нитевидные структуры и целые конгломераты. Образующиеся внутриклеточные включения нарушают процесс нервной передачи и, вероятно, оказывают нейротоксическое действие.
Первоначально возникают глиоз и синаптическая дисфункция. Вскоре они дополняются сокращением размеров и количества аксонов, нарастающей и распространяющейся нейродегенерацией. Нейроны и глиальные клетки начинают массово погибать, что макроскопически выглядит как прогрессирующая атрофия нервной ткани с преимущественным поражением определенных зон.
Хотя мультисистемная атрофия относится к синуклеинопатиям, в головном мозге при этом заболевании появляются и другие патологические цитоплазматические включения. Нередко в небольшом количестве обнаруживаются тельца Леви, амилоидные клубки и другие белковые конгломераты. Это усугубляет нейродегенерацию, хотя и не сказывается ключевым образом на клинической картине.
Кроме того, у ряда пациентов с мультисистемной атрофией обнаруживаются антитела к клеткам голубого пятна (особой подкорковой структуры головного мозга). Их значение пока окончательно не выяснено, ученые исследуют возможность использования этих данных для повышения точности прижизненной диагностики заболевания.
Причины развития
Ученые продолжают изучать причины, механизм развития и провоцирующие факторы МСА. Однозначного подтверждения нет о наследственной предрасположенности к развитию болезни. У ребенка врожденная атрофия ГМ бывает при злоупотреблении женщины во время беременности лекарствами, спиртным, наркотиками.
В ходе диагностики врачи выявляют возможные причины мультисистемнойатрофии:
- болезнь Паркинсона либо Альцгеймера;
- контакт с нейротоксическими веществами;
- изменчивость гена «α-синуклеин»;
- отравление алкоголем, наркотиками у людей с зависимостью;
- травма головного и/или спинного мозга;
- гипоксия тканей ГМ.
Патогенез плохо поддается изучению, поскольку неизвестны точные причины мультисистемной атрофии. В ходе исследований обнаружено накопление тау-протеинав пораженных олигодендроглиоцитах. Это выявляют в мозжечке, пирамидах, коре ГМ, рогах спинного мозга в области грудного и крестцового отдела хребта. Одновременно повреждаются дофаминовые рецепторы, черная субстанция, скапливаетсяα-синуклеин в нейроглиальных клетках.
Справка! МСА характерно асимметрическое уменьшение белого вещества, нарушение передачи нервных импульсов. Нейроны страдают меньше олигодендроглиоцитов.
Распространенность
Работа с пестицидами или другими токсичными веществами повышает риск развития в будущем мультисистемной атрофии
По современным данным, мультисистемная атрофия относится к спорадическим заболеваниям и не имеет явной наследственной предрасположенности. Описанные в литературе редкие семейные формы оливопонтоцеребеллярной атрофии считаются другой нозологией.
Распространенность мультисистемной атрофии в мировой популяции составляет в среднем 1,9–4,4 случаев на 100 тыс. населения. Но эти данные ориентировочные и скорее всего заниженные, что объясняется недостаточной диагностикой заболевания в общемедицинской сети. По статистике специализированных неврологических центров, около 8,2% случаев паркинсонизма обусловлены мультисистемной атрофией. А истинная распространенность этого заболевания, скорее всего, составляет не менее 4,8–5,5 случаев на 100 тыс. населения.
Классификация
Медики выделяют три формы МСА в зависимости от того, какой синдром выявляется ведущим. Если это невозможно установить, пациенту диагностируют смешанный тип болезни.
Классификация патологии:
| Ведущий симптом | Тип мультисистемной атрофии | Отличительные черты |
| Паркинсонизм | Стриатонигральный тип МСА | Замедленные движения, лицо маскообразное, застывание в одной позе, симптом «воздушная подушка», тремор конечностей, согнутость суставов, снижение подвижности. Дегенерации больше подверженстриатум, черная субстанция. |
| Вегетативная недостаточность | Синдром Шая-Дрейджера | Дисфункция желез и органов, тазовые нарушения, гипотензия, храп, апноэ. |
| Мозжечковая атаксия | Оливопонтоцеребеллярный тип МСА | Ухудшение равновесия, нарушение мелкой моторики, непроизвольное движение глазных яблок, мышечная слабость. Дегенерации больше подвержен мозжечок, мост, оливы. |
В классификаторах врачи предлагают убрать синдром Шая-Дрейджера, поскольку вегетативная недостаточность сопровождает все формы МСА. В МКБ-10 указан только мозжечковый и паркинсонический тип болезни.
Симптомы
Первый признак МСА – начало прогрессирования болезни в старшем возрасте после 45 лет. Симптомы развивается быстро. У большинства людей сразу проявляется паркинсонизм, двигательные нарушения. В 40% случаев дегенерация стартует с вегетативной дисфункции.
Изменения в начальной стадии пациентом не всегда замечается. Среди первых признаков указаны тазовые нарушения: эректильная дисфункция, трудности с мочеиспусканием или дефекацией, недержание мочи/кала. Каждый пятый заболевший с момента прогрессирования мультисистемной атрофии начинает падать. Причиной считается ортостатическая гипотензия, мышечная слабость, дисфункция мозжечка.
Справка! Прогрессированию МСА характерно присоединение к ведущему синдрому других симптомокомплексов. То есть, у человека одновременно проявляется вегетативная недостаточность в сочетании с признакамипаркинсонизма и мозжечковой атаксии.
Отличия симптомов разных типов МСА
Первичные симптомы зависят от класса мультисистемной атрофии. При стриатонигральном типе МСА сразу заметны признаки болезни Паркинсона. Вначале организм откликается на лечение леводопой, затем эффективность лекарств теряется, усугубляются вегетативные расстройства.
Первичные признаки паркинсонического типа мультисистемной атрофии:
| Симптом | Пояснение |
| Брадикинезия | Все произвольные движения замедляются. Человек медленнее ходит, говорит, пишет, читает вслух. Координация движений и речи сохраняется. Длительный разговор или необходимость движения вызывает быструю утомляемость. |
| Ригидность | Скованность движения, напряжение мышц, отвечающих за сокращение, разгибание. Подбородок почти касается ключичной зоны. В горизонтальном положении на спине голова не лежит на подушке, но это исчезает после засыпания. Конечности полусогнуты в крупных суставах, туловище сгибается вперед, позвоночник сутулый. При пассивном движении конечностью (выполняет доктор) под пальцами врач ощущает вязкое сопротивление мышц. |
| Постуральная неустойчивость | Человек не может сохранить равновесие. Это не связано с ортостатической гипотонией, потемнением в глазах, гипертензией. |
| Тремор | Мышцы туловища, шеи, рук, ног дрожат во время движения или покоя. Тремор исчезает, когда пациент выполняет противоположное действие. То есть, перестает либо начинает двигаться. |
При оливопонтоцеребеллярном типе МСА на первом плане стоят симптомы мозжечковой дисфункции. Пациент начинает семенить (уменьшается длина шага). Отмечается шаткость походки, скованность мышц, ухудшение общей координации движений и мелкой моторики. Тремор усиливается при приближении к цели движения. Затрудняется смена быстро чередующихся действий.
При мозжечковом типе мультисистемной атрофии проявляется дизартрия и глазодвигательная (окуломоторная) дисфункция. Их симптомы:
- Приглушенность голоса;
- Растянутое произношение слов;
- Скандированная речь;
- Нарушение модуляция звука, фонации, дыхания во время произношения;
- Ритмичное непроизвольное движение глазных яблок (нистагм).
Синдром Шая-Дрейджера при МСА проявляется расстройством функций тазовых органов, желез. Бывает обморок, коллапс из-за падения давления. К признакам относят нарушение мочеиспускания, опорожнения кишечника, снижение слюнотечения, слезотечения, потоотделения. Отмечается во время сна движения глаз, разговор, кратковременная остановка дыхания. У мужчин ухудшается эрекция, развивается импотенция.
Справка! Прогрессирование МСА проявляется усугублением симптомов 1―3 типов мультисистемной атрофии. Клиника дополняется слабоумием, параличом или парезом, неадекватным поведением, осложнениями дегенерации.
Медицинские интернет-конференции
Введение. Мультисистемная атрофия (МСА) и прогрессирующий надъядерный паралич (ПНП) – нейродегенеративные заболевания, которые раньше относились к группе болезней «паркинсонизм-плюс». В основе клинической картины – синдром Паркинсона с низкой эффективностью специфической терапии, когнитивные нарушения и дополнительные симптомы, на основании которых в дальнейшем и были определены отдельные нозологии [1]. И при МСА, и при ПНП поражаются подкорковые и стволовые структуры.
Оба заболевания, мультисистемная атрофия и прогрессирующий надъядерный паралич, встречаются в неврологической практике в основном как спорадические; мультисистемная атрофия имеет несколько типов развития и течения болезни, которые могут быть представлены как «чистыми», так и «смешанными» вариантами [2], для прогрессирующего надъядерного паралича также характерны различные клинические варианты дебюта, развития заболевания, описаны как традиционные, так и необычные и нетипичные сочетания симптомов [3,4], что приводит к существенным трудностям в диагностике каждого из этих заболеваний. На ранних стадиях, когда симптомы выражены еще неярко, а клинические синдромы находятся в процессе формирования, данные заболевания имеют значительное количество общих черт в виде синдрома паркинсонизма, вегетативной недостаточности, глазодвигательных нарушений, псевдобульбарного синдрома, когнитивных нарушений, эмоционально-личностных расстройств и нарушений сна, что вызывает существенные трудности в проведении дифференциальной диагностики.
В настоящее время проблема дифференциальной диагностики данных болезней представляет интерес как из-за различного прогноза в плане развития деменции и сохранения самостоятельности пациента [4], так и из-за выявления семейных случаев и при мультисистемной атрофии, и при прогрессирующем надъядерном параличе, в связи с чем предполагается, что генетические факторы могут влиять на патогенез и развитие этих заболеваний. По данным молекулярно-генетических исследований, один из вариантов мультисистемной атрофии связан с мутацией в гене COQ2, расположенном в области 4q21.22-q21.23 [5], семейный вариант прогрессирующего надъядерного паралича – с мутацией в гене МАРТ, расположенном в области 17q21.31 [6].
Описание клинического случая. В качестве иллюстрации сложности проведения дифференциального диагноза между мультисистемной атрофией и прогрессирующим надъядерным параличом приводим описание клинического случая динамического наблюдения за пациенткой М., 60 лет, несколько раз проходившей лечение в различных отделениях Воронежской городской клинической больницы скорой медицинской помощи № 1.
Впервые в поле зрения врача-невролога пациентка М. попала, когда находилась на лечении в гинекологическом отделении ВГКБМСП № 1 по поводу вульвовагинита и вульводинии. К неврологу была направлена на консультацию.
Жалобы и история развития заболевания.
Пациентку беспокоили периодические головные боли, эпизоды повышения АД до 150/90, ощущение перебоев в работе сердца, ухудшение зрения (с -5 диоптрий до -9 за последние 3 года). В качестве основной жалобы предъявляла неустойчивость при ходьбе, частые падения, особенно в сырую слякотную погоду. При падении ушибается, получает ссадины. Сознания не теряет. Дважды больная «предчувствовала» падения: шла по улице и поняла, что сейчас упадет. Попыталась этого не допустить, однако все равно упала. Случайный прохожий, помогавший подняться, заметил: «От чего же вы упали, ведь даже не споткнулись?!». Несколько лет назад был эпизод, когда больная шла по улице, почувствовала шаткость при ходьбе и резкое отклонение в сторону, «стало уводить». Пациентка попыталась «откорректировать курс», однако это не удалось сделать, поэтому, чтобы не выйти на проезжую часть, ей пришлось взяться за столб и некоторое время за него держаться. Затем состояние улучшилось, больная смогла продолжить путь. После установления в процессе беседы доверительных отношений с врачом, пациентка призналась, что помимо неустойчивости и падений ее беспокоит учащенное мочеиспускание, иногда доходящее до нескольких раз в час, с императивным характером позывов, нарушение в связи с частым мочеиспусканием ночного сна, трудности в общении, профессиональной деятельности. Беспокоит учащенная дефекация (часто вместе с мочеиспусканием), жидкий стул. В настоящее время помимо учащенного мочеиспускания жалуется на покалывание и жжение в области наружных половых органов при мочеиспускании, связывает это с обострением вульвовагинита.
Пациентка считает, что здоровье ее нарушилось около 3-х лет назад, когда больная самостоятельно выдавила и прижгла бриллиантовой зеленью фурункул во влагалище. Вскоре после этого появились дизурические жалобы: неприятные ощущения при мочеиспускании, ощущение, что в мочеиспускательном канале есть какое-то образование, инородное тело или воспалительный инфильтрат. Больная отметила также более частые позывы на мочеиспускание, акт мочеиспускания периодически бывал болезненным. Сначала лечилась самостоятельно «от цистита», принимала различные антибиотики, затем обращалась к урологам, был диагностирован острый, затем хронический цистит, который часто обострялся, что подтверждалось анализами мочи, ультразвуковым исследованием мочевого пузыря. Пациентка в течение последних двух лет по поводу гиперактивного мочевого пузыря по рекомендации урологов принимает препарат спазмекс. Начинала прием с минимальных доз, препарат давал положительный эффект, но периодически все равно приходилось увеличивать дозу лекарственного средства. В настоящее время пациентка отмечает существенное снижение эффективности препарата, особенно в течение последних нескольких месяцев, недель. Для поездок, работы пользуется прокладками, при прогулках по городу строит маршруты так, чтобы можно было зайти в какое-либо учреждение в туалет. Пациентка отмечает, что все позывы на мочеиспускание сильные, прохождение мочи по мочеиспускательному каналу чувствует хорошо. Количество принимаемой жидкости оценивает как небольшое или среднее, около 1,5-2 литров. Жажду отрицает.
Анамнез жизни.
Работает юристом, разведена, проживает с сыном, страдающим психическим заболеванием. У пациентки также есть дочь, живущая отдельно со своей семьей. Несколько лет назад был вывих ключицы в автоаварии, восстановилась быстро и хорошо, вернулась к работе. Онкологические, венерические заболевания, туберкулез, болезнь Боткина, отрицает. В течение ряда лет отмечались аллергические реакции на пыльцу растений. На продукты питания, медикаменты аллергию отрицает. Наблюдалась у ЛОР-врача с диагнозом аллергический ринит.
Неврологический статус. Больная в ясном сознании, контактна, адекватна, правильно ориентирована. Обращает на себя внимание телосложение и походка: пациентка астенического телосложения, высокая, плечи развернуты назад, голова также несколько запрокинута назад, спина прямая, практически не сгибается и не двигается при ходьбе. При этом несколько избыточны движения в области тазового пояса, походка «разболтанная», шаг широкий, ноги ставит далеко друг от друга. Ретроколлис.
Речь правильная, с богатым словарным запасом, эмоционально окрашенная, с яркими интонациями. Темп речи умеренный, ближе к медленному, речь несколько неплавная, тягучая. Голос хорошо модулирует, однако по тембру «надтреснутый, шероховатый», имеет носовой оттенок. При проверке когнитивных функций с помощью краткого исследования когнитивного состояния, теста рисования часов, монреальской шкалы оценки когнитивных функций и батареи лобных тестов получены нормальные результаты.
Зрачки равные, округлой формы, обычного диаметра, живо реагируют на свет. Глазные щели D=S, движения глазных яблок по горизонтали в полном объеме, по вертикали – с особенностями: затруднены следящие движения вверх и вниз, трудности с фиксацией взора в этих положениях, при длительном нахождении неврологического молоточка в этих позициях больная очень быстро отводит взор. Болезненность, тошноту, головокружение, двоение в этих положениях глаз отрицает. Затруднены также движения глаз в верхние и нижние косые положения. Возможно, имеет место формирование пареза взора вверх и вниз. Корнеальные рефлексы живые, симметричные. Чувствительность на лице не изменена, нижнечелюстной рефлекс оживлен, симметричный. Лицо симметричное. Глотание сохранено. Язык по средней линии, без атрофий и фасцикуляций, розовый, влажный. Определяются умеренно выраженные симптомы орального автоматизма: хоботковый, назолабиальный. Объем активных движений в конечностях полный, парезов нет. Мышечный тонус повышен по экстрапирамидному типу во всех группах мышц, в том числе в аксиальной мускулатуре. Выявляется феномен восковой гибкости, феномен Нойка-Ганева ярко представлен с 2-х сторон. Глубокие рефлексы с рук умеренные, без разницы сторон, с ног – ближе к низким, также симметричные. Чувствительность в области конечностей, живота не изменена. От проверки чувствительности в аногенитальной зоне больная отказалась. В позе Ромберга больная легко пошатывается вправо. Пальце-носовую пробу выполняет с легкой интенцией справа. Пяточно-коленную пробу выполняет с атаксией справа. Выявляются нерезко выраженные адиадохокинез, гиперметрия, дисметрия слева. Менингеальных знаков нет.
Таким образом, по результатам расспроса пациентки и первичного осмотра были выявлены следующие нарушения: гипокинетико-ригидный синдром с преобладанием тонуса мышц в аксиальной мускулатуре и формированием разгибательной позиции тела, псевдобульбарный синдром, глазодвигательные нарушения, нарушения походки, постуральная неустойчивость и падения, мозжечковые расстройства, нарушения сна, вегетативные расстройства в виде нарушений мочеиспускания и артериальной гипертензии. Большинство этих симптомов могут встречаться при обоих обсуждаемых заболеваниях (синдром паркинсонизма, псевдобульбарный синдром, нарушения сна). Тем не менее, некоторые из них более характерны для МСА (мозжечковые симптомы, вегетативные расстройства), тогда как другие – для ПНП (разгибательная поза при ходьбе, постуральная неустойчивость, парезы взора по вертикали, особенно вниз).
Пациентке было рекомендовано дообследование:
- МРТ головного мозга.
- ЭЭГ.
- Осмотр окулиста, эндокринолога.
- Гликемический профиль, уровень гликозилированного гемоглобина, контроль электролитов (калий, натрий, кальций) в динамике.
- Измерение объема потребляемой жидкости за сутки и объема выделяемой мочи за сутки, общий анализ мочи, ведение дневника мочеиспусканий.
- Определение концентрации эстрогенов в крови, антидиуретического гормона.
Через 3 месяца пациентка была осмотрена повторно (в период госпитализации в урологическое отделение по поводу обострения хронического цистита). На ЭЭГ – вариант возрастной нормы, на МРТ головного мозга – легкое расширение боковых желудочков, на глазном дне – ангиопатия сетчаток, отклонений со стороны биохимических показателей, в содержании гормонов и электролитов выявлено не было, эндокринолог не выявил заболеваний эндокринной системы. Согласно дневнику мочеиспусканий, их количество колебалось в различные дни от 8 до 27 за сутки, ночных – от 1 до 7. За эти 3 месяца у пациентки появились жалобы на ухудшение памяти на текущие бытовые события, профессиональная память не страдает. Беспокоит изменение почерка: стал более небрежным, неаккуратным. За последние 3 месяца похудела на 2 кг. В плане нарушений мочеиспускания отмечает, что бывают «хорошие дни», когда учащенное мочеиспускание беспокоит мало, и «ужасные», когда больная постоянно бегает в туалет. Пациентка обратила внимание на следующее: приняв анальгетик для снятия головной боли, заметила снижение количества походов в туалет в этот вечер, в дальнейшем несколько раз «экспериментировала», принимая анальгетик в те дни, когда мочеиспускание было особенно частым, прием лекарства приводил к некоторому урежению мочеиспускания.
В неврологическом статусе определяются следующие изменения: повторное исследование когнитивных функций выявило наличие умеренных когнитивных нарушений: по краткому исследованию когнитивного состояния (MMSE) – 26 баллов, по Монреальской шкале (MoCA) – 24 балла. В наибольшей степени нарушилось отсроченное воспроизведение запоминаемых слов и счет. Другие тесты выполнялись хорошо. Отмечается парез взора вверх, затруднение движений глазных яблок вниз, нарушение плавности горизонтальных движений глаз. В остальном в неврологическом статусе динамики нет.
Принимая во внимание, что учащенное мочеиспускание в данный период может быть связано с обострением хронического цистита, а также тот факт, что сформировался парез взора вверх, ухудшились движения глазных яблок вниз, появились умеренные когнитивные расстройства в виде нарушений памяти и счета, более правомочным представлялся диагноз прогрессирующего надъядерного паралича, при котором отмечается синдром паркинсонизма с преобладанием тонуса в аксиальной мускулатуре и формированием разгибательной позиции, отсутствует на ранней стадии изменение длины шага, скорости ходьбы, типичны глазодвигательные нарушения, особенно вертикальные парезы взора или офтальмоплегия, а когнитивные нарушения, достаточно быстро достигающие степени деменции. Соответственно данному диагнозу, ожидалось прогрессирование симптомов паркинсонизма, усиление постуральной неустойчивости, глазодвигательных нарушений, дальнейшее ухудшение когнитивных функций с последующим развитием деменции.
Через 10 месяцев состоялся следующий осмотр больной, когда пациентка попала в неврологическое отделение больницы с острой нейропатией лицевого нерва справа на фоне переохлаждения. Пациентка отмечает, что эпизоды неустойчивости случаются с той же частотой, однако падений стало меньше, объясняет это тем, что теперь «внимательно смотрит под ноги». Основной жалобой остается учащенное мочеиспускание с императивными позывами. В неврологическом статусе помимо выраженной асимметрии половины лица, усилились нарушения почерка, появились черты мегалографии, в остальном динамики нет: сохраняется повышение мышечного тонуса во всех группах мышц по экстрапирамидному типу, в том числе в аксимальной мускулатуре, ретроколлис, однако выраженность его та же, ограничены движения глазных яблок вверх, объем движений вниз и по горизонтали достаточный, но движения неплавные. Сохраняются имевшиеся мозжечковые расстройства, когнитивные нарушения не прогрессируют: MMSE 27 баллов, MoCA – 24 балла, другие тесты – норма. Принимая во внимание тот факт, что типичного для ПНП быстрого неуклонного прогрессирования заболевания не отмечается, когнитивные функции остаются сохранными, пареза взора вниз, тем более полной офтальмоплегии – нет, отмечается нарастание мозжечковых расстройств, стойкость вегетативных нарушений в виде резко учащенного мочеиспускания с императивными позывами уже вне обострения хронического цистита, диагноз ПНП, согласно критериям NINDS-SPSP [7], требует пересмотра.
В данной ситуации более вероятным представляется диагноз мультисистемной атрофии, при которой также могут иметь место глазодвигательные нарушения, но они, как правило, не достигают степени пареза взора или офтальмоплегии, часто встречаются когнитивные нарушения, которые, однако, не достигают степени деменции. Что же касается разгибательной позиции туловища, то она является частым, но не облигатным симптомом ПНП.
Мнение о том, что у данной пациентки клиническая картина заболевания более соответствует диагнозу мультисистемной атрофии, чем ПНП, подтверждает следующее наблюдение: спустя 3,5 года от момента последней госпитализации в ВГКБСМП № 1, т.е. через 4 года и 7 месяцев от момента первого знакомства, с пациенткой состоялась случайная встреча в вестибюле больницы, куда она пришла проведать родственницу. Больная узнала врача, рассказала, что у нее усилились расстройства мочеиспускания, присоединились эпизоды неудержания мочи, постоянно пользуется памперсами, вынуждена была полгода назад оставить успешную юридическую практику, в настоящее время работает только как приглашенный консультант, а все остальное время заботится о сыне и помогает дочери с внуками: сопровождает в школу и на дополнительные занятия, проверяет уроки. Речь у больной несколько замедленная, с элементами дизартрии, эмоционально окрашенная, голос слегка охриплый, горизонтальные движения глаз сохранены (легко переводит взор с одного предмета на другой, движения вверх ограничены, вниз — немного), походка с явлениями мозжечковой атаксии, поза при ходьбе с запрокинутой головой, развернутыми назад плечами.
Заключение. Таким образом, на основании анализа представленного случая можно заключить, что клинический метод является ведущим в диагностике заболеваний, при которых отсутствуют патогномоничные симптомы, четко очерченные изменения при нейровизуализации, биохимические, инструментальные маркеры. Динамическое наблюдение за пациентами, у которых отмечаются симптомы, соответствующие нескольким заболеваниям со сходной клинической картиной, является крайне важным для уточнения диагноза. Как видно из описания данного случая, на более ранних этапах развития заболевания клиническая картина может больше соответствовать одному диагнозу, а на последующих – другому. В описанном наблюдении представляет интерес тот факт, что у пациентки сочеталось несколько симптомов, характерных для разных заболеваний, например, разгибательная позиция туловища и раннее развитие постуральной неустойчивости, более характерные для ПНП, и вегетативные нарушения и мозжечковые симптомы, более характерные для МСА. Возможно, это связано с некоторыми элементами патогенеза, общими для двух заболеваний [8].
Методы диагностики
Обследоваться надо у невролога. Для постановки диагноза нужно динамическое наблюдение пациента с применением церебрального МРТ. В случае противопоказаний проводят компьютерную томографию ПЭТ, ОФЭКТ.
В начале развития МСА МРТ не покажет атрофических изменений мозговой ткани, но поможет исключить опухоль, энцефалит, рассеянный склероз. Через 1―3 года интенсивной прогрессиивыявляют расширение IV желудочка, выраженную дегенерацию подкорковых ганглий, нижней половины моста, мозжечка, скорлупы.
На осмотре невролог оценивает наличие вегетативной недостаточности в комбинации спаркинсонизмоми/или дисфункцией мозжечка.
Мультисистемная атрофия не подтверждается, если:
- МСА начала развиваться до 30 либо после 75 лет;
- вегетативная недостаточность не сочетается ни с мозжечковой дисфункцией, ни с паркинсонизмом;
- патология также есть у близких родственников (семейный анамнез);
- у пациента выявлена деменция, признаки похожей на МСА болезни;
- лечение паркинсонизма эффективно лекарствами леводопы.
Для постановки диагноза ортостатической пробой исследуют функции вегетативной нервной системы. Нарушение работы тазовых структур выявляют при проведении электромиографии сфинктеров.
На развитие мультисистемной атрофии указывает наличие:
- ортостатической гипотензии — снижение давления после принятия вертикального положения;
- нерегулярного тремора;
- холодности стоп и кистей, скованности их сочленений;
- храпа, который вновь появился либо усилился;
- плача или смеха, несоответствующих переживаемой эмоции;
- тяжелых нарушений речи, голоса — дизартрия, дисфония;
- затрудненных вдохов — инспираторная одышка;
- недержания мочи;
- нарушений эректильной функции;
- кривошеи с наклоном головы к груди — антероколлис;
- непроизвольных движений мимических мышц, языка — орофациальная дистония;
- искривления позвоночника в грудопоясничном переходе с наклонением туловища вперед — камптокормия;
- учащения случаев падения;
- мозжечкового синдрома/паркинсонизма + вегетативной недостаточности.
Справка! МСА достоверно подтверждается патоморфологическим исследованием нейроглии. При жизни биоматериал с глиальными клетками получают посредством биопсии мозга или ткань изымает патологоанатом во время вскрытия.
Этиология
На настоящий момент мультисистемная атрофия считается заболеванием неуточненной этиологии, не выявлены и конкретные факторы риска.
По данным проведенных исследований (P.A.Hanna et all, 1999), предшествующий продолжительный контакт с токсическими соединениями установлен у 11% заболевших. Поэтому предрасполагающим моментом для некоторых людей может стать работа на вредных производствах, связанных с формальдегидом, органическими растворителями, пестицидами.
Но контакт с потенциально токсичными соединениями все же не может рассматриваться как однозначный этиологический фактор. Скорее всего, речь идет об индивидуальной повышенной чувствительности нервной системы к поступающим извне веществам. В то же время пока не выявлено генетических аномалий, свойственных именно этому заболеванию. Предполагают, что определенное значение может иметь полиморфизм в гене белка α-синуклеина, патологическое накопление которого связывают с развитием мультисистемной атрофии.
Исключены также инфекционная и эндокринная причины такой нейродегенерации.
Лечение
Людей с МСА лечат препаратами симптоматической терапии. Они помогают убрать выраженность паркинсонизма, мозжечковой атаксии и других признаков дегенерации головного мозга.
В симптоматическое лечение мультисистемной атрофии включают:
- медпрепараты леводопы;
- вазоактивные средства;
- нейрометаболические лекарства;
- массаж, водные процедуры, ЛФК, другие методы физиотерапии;
- диету с соблюдением нормы потребления соли;
- немедикаментозные способы устранения ортостатистической гипотензии.
Паркинсонизм в начальных этапах прогрессии МСА лечат комбинированными средствами леводопы с бенсеразидом, карбидопой. Его заменяют при плохой переносимости или неэффективности препаратами альтернативной терапии. При атрофии всех типов используют агонисты дофаминовых рецепторов, лекарства с веществом амантадин.
Проявления мозжечковой атаксии убирают методами физиотерапии. Для облегчения состояния МСА назначают средства с клоназепамом, габапентином, буспироном, пропранололом и прочими веществами.
При тазовых нарушениях на фоне атрофии используют лекарства:
- Силденафил (при эректильной дисфункции);
- Макрогол, слабительные средства (в случае запоров);
- Антагонист альфа1-адренорецепторов + холинергический препарат (задержка мочи);
- Антихолинергическое средство (непроизвольное или болезненное мочеиспускание).
При нарушениях функций мочевого пузыря дополнительно к лекарствам показана периодическая либо постоянная катетеризация органа. Из альтернативных препаратов применяют уколы ботулотоксина. Эти инъекции также назначают для лечения дыхательных расстройств, каптокормии, слюнотечения, дистонии на фоне МСА.
При ортостатической гипотензии показано спать на кроватях с возвышением изголовья, пить много воды, богатой минералами. Надо носить компрессионные чулки. Нельзя переедать, резко вставать после пробуждения. Рекомендуется обучиться изометрическим маневрам. Прописывают минералокортикоиды, гипертензивные средства с мидодрином.
При нарушениях дыхания показана вентиляция легких либо трахеостомия. Камптокормию лечат методами физиотерапии. Лекарствами с зопиклономили клоназепамом устраняют расстройства сна из-за МСА. При депрессии прописывают селективный ингибитор обратного захвата серотонина (группа антидепрессантов).
Справка! Клиницисты продолжают искать новые методы лечения мультифокальной атрофии. Этиологическую терапию нет возможности применять, пока невыяснены причины и механизм развития МСА.
Осложнения
К последствиям прогрессирования МСА относят урогенитальные инфекции, цистит, уретрит, воспаление почек. Бактерии могут проникнуть в кровь и вызвать сепсис. На фоне дыхательных нарушений чаще развивается пневмония, ночное апноэ.
При мультисистемной атрофии возможно поражение продолговатого мозга. Это осложняется расстройством глотательной функции, вызывает смерть из-за паралича дыхательного центра или асфиксии. Вследствие дегенеративных процессов нарушается также работа сердца, сосудистой системы, мозговое кровообращение.
Прогноз и продолжительность жизни
МСА – неизлечимая патология с необратимыми изменениями мозга. Поэтому прогноз выздоровления негативен. Лечение облегчает проявления мультисистемной атрофии, но не способно остановить или затормозить дегенерацию нейроглии. Качество жизни быстро ухудшается, человек не может себя сам обслуживать.
Смерть наступает в среднем через 7 лет после проявления первых признаков болезни. При вялотекущем прогрессировании продолжительность жизни удваивается. Смерть вызывают осложнения МСА: инфекции, сердечная или дыхательная недостаточность, нарушение мозгового кровообращения.
Методы профилактики
Поскольку до конца не изучены причины и патогенез МСА, специфическая профилактика не разработана. Врачи рекомендуют при работе с нейротоксическими веществами пользоваться респираторами и прочими средствами индивидуальной защиты.
Для профилактики генетической предрасположенности беременной женщине категорически запрещено курить, употреблять наркотики, алкоголь, принимать лекарства с тератогенным и эмбриотоксическим свойством. Лекарства назначает только врач по строгим медицинским показаниям.
Что нужно запомнить?
- При мультисистемной атрофии в мозге происходит необратимая дегенерация тканей центральной нервной системы.
- Причины возникновения и механизм развития продолжают исследоваться.
- В справочнике МКБ-10 оставили два типа болезни: паркинсонический и мозжечковый.
- В клинике МСА присутствуют 2―3 синдрома одновременно: вегетативная недостаточность в сочетании с мозжечковой дисфункцией и/или паркинсонизмом.
- В ходе диагностики пациента тестируют на различные виды расстройств ЦНС, делают томографию мозга.
- Лечение мультифокальной атрофии головного мозга заключается в применении симптоматической терапии.
- Сепсис, бульбарный паралич и иные осложнения МСА приводят к смерти.
- Прогноз на выздоровление отсутствует, пациент живет максимум 15 лет.
- Профилактика МСА не разработана, поскольку невыяснены причины болезни.
Литература
- Шиндряева H.H., Белова А.Н., Левин О.С. Мультисистемная атрофия — распространённость в Нижнем Новгороде. Сборник материалов научно-практической конференции «Вегетативные расстройства в клинике нервных и внутренних болезней -2009» 2009 г.
- Шиндряева H.H., Левин О.С. Вегетативные проявления у больных с мультисистемной атрофией. Сборник материалов III научно-практической конференции «Вегетативные расстройства в клинике нервных и внутренних болезней» 2010 г.
- Дамулин И.В., Яхно H.H., Гончаров O.A. Сравнительная оценка нарушений высших мозговых функций при различных типах церебральной атрофии.// Журн. неврологии и психиатрии С.С.Корсакова -1990.
- Пономарев, В.В. Редкие неврологические синдромы и болезни. -СПб. Фолиант.
- Brown RG, Lacomblez L, Landwehrmeyer BG, Bak T, Uttner I, Dubois B, Agid Y, Ludolph A, Bensimon G, Payan C, Leigh NP; for the NNIPPS Study Group (August 2010). “Cognitive impairment in patients with multiple system atrophy and progressive supranuclear palsy”. Brain. 133(Pt 8): 2382—93.
- Swan L, Dupont J (May 1999). “Multiple system atrophy”. Phys Ther. 79(5): 488—94. PMID 10331752.
- American Psychiatric Association. Diagnostic and statistical manual of mental disorders, 4th edition, (DSM IV).// Washington, DC: American Psychiatric Association, 1994.
- The Consensus Committee of the American Autonomic Society and the American Academy of Neurology (1996). “Consensus statement on the definition of orthostatic hypotension, pure autonomic failure, and multiple system atrophy”. Neurology. 46(5): 1470. PMID8628505.
Диагностика
Диагностика мультисистемной атрофии основывается на анализе клинической картины и данных нейровизуализационных методик. При этом обязательным признаком является наличие вегетативной недостаточности, что подтверждается специальными клиническими тестами и суточным мониторингом уровня артериального давления. Достоверной и доступной лабораторной диагностики этого заболевания на данный момент пока не разработано.
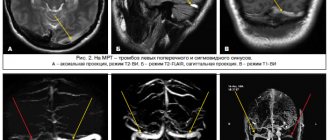
МРТ головного мозга может выявить ряд характерных признаков:
- Изменение интенсивности сигнала от скорлупы и бледного шара, атрофия скорлупы, появление гиперинтенсивной (в режиме Т2) щелевидной полоски по наружному краю скорлупы.
- Атрофия ствола и мозжечковых структур. Изменения захватывают червь, кору полушарий, средние ножки мозга, основание моста.
Определенный (полностью достоверный) диагноз возможен лишь при патоморфологическом посмертном исследовании нервной ткани. Признаками заболевания служат плотные глиальные цитоплазматические включения и дегенеративные изменения в оливопонтоцеребеллярной и нигростриарной области.