Сегодня бактериальный менингит является мало распространенным заболеванием, которое может диагностироваться в любой точке мира. К данной патологии у некоторых народов существует генетическая предрасположенность, но в каждой возрастной группе болезнь может развиваться по многим причинам. Передается эта разновидность менингита воздушно-капельным путем, особенно легко можно инфицироваться при нахождении в одной комнате с больным человеком. Данное заболевание имеет свои особенности, симптоматику и методы терапии, которые отличаются от иных форм менингита.
Характеристика и описание проблемы
Вам будет интересно:Агрегация сперматозоидов: что это значит, причины и лечение, последствия патологии
Бактериальный менингит – болезнь головного и спинного мозга инфекционного характера, что провоцируется бактериями группы стрептококков. Патология способствует развитию воспалительного процесса в оболочках ЦНС. Распространенность менингита незначительная, но он легко передается от инфицированного человека к здоровому, что может стать причиной эпидемии среди населения. Главные изменения наблюдаются в мягкой и паутинной оболочках мозга, часто в патологический процесс вовлекается и серое вещество.
Вам будет интересно:»Витапрост Форте»: инструкция по применению, отзывы
В медицине бактериальный менингит у взрослых и детей делят на следующие разновидности:
- стрептококковый;
- стафилококковый;
- пневмококковый;
- менингококковый;
- неопределенный.
Заболевание является стремительно прогрессирующим, поэтому требует незамедлительного лечения. При отсутствии терапии увеличивается риск развития осложнений и даже смертельного исхода, актуально это в детском и старческом возрасте, а также при сниженном иммунитете человека.
Заражение мозговых оболочек развивается из-за попадания в них бактерий. Происходит это в результате реакций организма на патогенные микроорганизмы. В организме человека происходит активация множества физиологически-активных веществ и лейкоцитов в сочетании с повреждением эндотелия. Все это становится причиной отека мозга, способствует увеличению внутричерепного давления и снижению кровотока в головном мозге.
Результаты и обсуждение
Этиологическая структура БМ в обследованной нами выборке пациентов представлена в табл. 1.
Таблица 1. Этиологическая структура БМ у обследованных больных (n=55)
Как видно из табл. 1, более половины обследованных пациентов страдали генерализованной менингококковой инфекцией, что подтверждает ее ведущую роль в возникновении БМ у детей.
В нашем исследовании у 41 (74,5%) больного обнаружен отягощенный преморбидный фон: перинатальное поражение ЦНС — у 14 (34%), частые ОРВИ — у 13 (32%), анемия — у 7 (17%), персистирующая герпесвирусная инфекция — у 7 (17%), а также их сочетание в разных комбинациях.
У пациентов с сопутствующей соматической и/или неврологической патологией БМ протекал достоверно тяжелее, что подтверждается результатами статистического анализа клинических данных (р
<0,05).
Неврологические осложнения БМ
Одним из наиболее частых неврологических осложнений является отек головного мозга. У 11 (20%) больных в остром периоде БМ определялись признаки отека головного мозга, возникшего на 2—3-й день заболевания, с прогрессирующим нарушением сознания, двигательным беспокойством, артериальной гипертензией, тахикардией, судорогами.
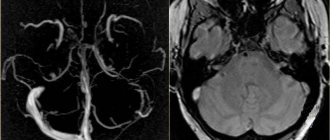
При отеке головного мозга на НСГ у обследованных пациентов было обнаружено диффузное повышение эхогенности паренхимы мозга и борозд, их расширение аналогично наблюдениям других авторов [4]. На КТ/МРТ обычно выявлялось снижение плотности вещества мозга, нарушение дифференциации белого и серого вещества.
Следует отметить, что эффекты осмотических диуретиков в традиционно используемых дозировках при БМ значительно ниже, чем при лечении травматического и ишемического отеков головного мозга. В нашей клинике имеется успешный опыт проведения инфузионной терапии маннитолом 4 раза в сутки (учитывая его довольно быстрое выведение); в этом случае необходимо контролировать осмолярность сыворотки крови. Начальную дозу дексаметазона целесообразно вводить до назначения антибиотикотерапии; используемые схемы считаются одинаково эффективными (дексаметазон 0,4 мг/кг 2 раза в сутки или 0,15 мг/кг 4 раза в сутки, продолжительностью до 4 сут) [5]. В настоящее время подтвержденных рандомизированных исследований о непосредственном воздействии кортикостероидов на отек головного мозга нет [6—8].
У 5 (9%) пациентов в остром периоде БМ имелась неврологическая пароксизмальная симптоматика, которая была представлена генерализованными (клонические) или сложными фокальными (моторные) эпилептическими приступами с вторичной генерализацией: у 2 (3,6%) пациентов с генерализованной менингококковой инфекцией; у 2 (3,6%) — с пневмококковым менингитом и у 1 — с гемофильным менингитом. Эпилептические приступы возникали на 2—4-е сутки от начала заболевания. Появление генерализованных судорог в дебюте БМ следует считать проявлением общемозговых расстройств, возникающих в результате острой метаболической энцефалопатии; наличие фокальных приступов предполагает очаговое поражение вещества мозга.
Согласно нашему опыту, эпилептические приступы эффективно купируются стандартными противоэпилептическими препаратами внутривенно; их профилактика в остром периоде БМ осуществляется пероральным назначением барбитуратов (глюферал) из расчета 3—5 мг/кг в сутки. Детям с относительно легким течением БМ, отсутствием повторных эпилептических приступов и эпилептических изменений на электроэнцефалограмме (ЭЭГ) противосудорожную терапию следует отменить сразу после выписки из стационара.
В нашем исследовании относительно частым осложнением БМ была субдуральная эмпиема. У 1 больного с пневмококковым менингитом развилась односторонняя субдуральная эмпиема в комбинации с абсцессом лобно-височной области, у 2 (3,6%) — с менингококковой инфекцией — односторонний субдуральный выпот. Субдуральная эмпиема является источником инфекции и способствует переходу острой стадии БМ в хроническую или рецидивирующую. Субдуральная эмпиема, также как и абсцесс головного мозга, предполагает наличие у пациента первичных очагов ЛОР-инфекции. У 7 (12,7%) больных БМ в анамнезе было упоминание о этмоидите и мастоидите. При затянувшемся течении БМ (чаще у младенцев) возможно образование абсцессов и без первичного очага инфекции. Субдуральная эмпиема может достигать больших размеров и, сдавливая головной мозг, демонстрировать клиническую картину растущей субдуральной гематомы (прогрессирующие нарушение сознания от угнетения до комы, многократная рвота, выбухание большого родничка у младенцев, эпилептические фокальные приступы, персистирующая лихорадка). Анализ ЦСЖ позволяет дифференцировать субдуральную эмпиему от субдурального выпота. При субдуральной эмпиеме клеточный состав ЦСЖ содержит преимущественно нейтрофилы.
Субдуральный выпот в остром периоде БМ встречается нередко, но его клинические проявления редки — обычно это признаки повышенного внутричерепного давления. У большинства из обследованных нами пациентов (5,5%) при субдуральном выпоте на НСГ, КТ и МРТ обнаружено скопление жидкости, сдавливающей вещество мозга, поэтому ведение таких пациентов должно предполагать возможность консультации нейрохирурга.
Лечение субдуральной эмпиемы, абсцесса головного мозга хирургическое, профилактика заключается в санации очагов первичной ЛОР-инфекции. Если субдуральный выпот не сдавливает церебральные структуры, оперативное вмешательство не требуется.
Глазодвигательные расстройства (косоглазие, диплопия, птоз) свидетельствуют о вовлечении в патологический процесс корешков черепных нервов. В нашей работе глазодвигательные расстройства были транзиторными и через 3—7 дней от начала заболевания движения глазных яблок полностью восстановились: у 2 (3,6%) пациентов с пневмококковым менингитом и у 1 — с гемофильным менингитом.
К частым сосудистым осложнениям БМ относят венозные тромбозы [9—10]. В нашем исследовании у 1 больного с гемофильным менингитом обнаружен тромбоз кавернозного синуса. В пользу него говорит поражение глазодвигательного нерва. Тромбоз кавернозного синуса имеет большое диагностическое значение в плане объективизации возможного очага первичной инфекции (этмоидит). При этмоидите на МРТ отек слизистой придаточных пазух или ячеек сосцевидного отростка дает такое же изменение сигнала, как и гнойное воспаление, поэтому в этих случаях верифицировать очаг первичной инфекции лучше с помощью КТ или рентгенографии. МР-венография позволяет выявить тромбоз венозного синуса и кортикальных вен.
Лечение венозных тромбозов включает назначение антикоагулянтов и умеренной дегидратации в возрастных дозировках. Большое значение имеет медикаментозная седация пациента, так как повышение внутричерепного давления может привести к разрыву вен в полости черепа. Их профилактика должна включать назначение антикоагулянтов и свежезамороженной плазмы.
В табл. 2 представлены неврологические осложнения БМ у детей разных возрастных групп в зависимости от вида возбудителя. У 26 (47,3%) пациентов с БМ обнаружены те или иные неврологические осложнения, среди которых в остром периоде заболевания у 11 (20%) больных выявлен отек головного мозга.
Таблица 2. Неврологические осложнения БМ у обследованных детей в зависимости от вида возбудителя (n=55) Примечание. У ряда пациентов выявлено более одного осложнения, в связи с чем их сумма не соответствует общему числу пациентов.
Таким образом, проведенное исследование подтвердило, что у детей, перенесших БМ, остается довольно высокая частота неврологических осложнений, имеющих серьезные последствия для жизни и развития ребенка.
Исходы БМ.
У 19 (34,5%) пациентов отмечался благоприятный исход БМ (выздоровление), среди них 17 (89,5%) детей перенесли генерализованную менингококковую инфекцию и 2 (10,5%) — гемофильный менингит. У 25 (45,5%) пациентов выявлен астеноневротический синдром (сравнительно благоприятный исход БМ), среди них 15 (60%) пациентов перенесли генерализованную менингококковую инфекцию, 5 (20%) — гемофильный менингит и 5 (20%) — пневмококковый менингит. Астеноневротический синдром характеризовался хронической или эпизодической головной болью напряжения, нарушением сна, эмоциональными расстройствами, поведенческими нарушениями. Жалобы на головную боль, как правило, появлялись на 2—3-й неделе от начала БМ, усиливаясь при умственной и/или физической нагрузке. У детей раннего возраста нарушались практически все фазы сна, появлялись ночные страхи, сноговорение. У детей старшего возраста наблюдались навязчивые движения, поведенческие расстройства.
У 2 (3,6%) пациентов с менингококковой инфекцией и у 1 — с пневмококковым менингитом диагностирована симптоматическая фокальная эпилепсия, требующая длительной противоэпилептической терапии (в течение 2 лет от последнего приступа под контролем ЭЭГ).
При вовлечении в патологический процесс слухового нерва возможным исходом БМ является нейросенсорная тугоухость, обнаруженная у 2 (3,6%) больных гемофильным менингитом и у 1 — пневмококковым менингитом. Аналогичные данные были получены в исследованиях М.Н. Сорокиной и соавт. [11]: у 2—3% больных БГМ обнаружена нейросенсорная тугоухость, гемипарез.
По данным разных авторов, избирательности в природе инфекционного возбудителя для возникновения нейросенсорной тугоухости нет (стрептококк, пневмококк, менингококк, гемофильная палочка и др.), а из предрасполагающих факторов обычно отмечается тяжелое течение БМ [12—14]. Чаще страдают структуры внутреннего уха [15], в некоторых случаях в сочетании с поражением вестибулярной части нерва. Слух может снижаться в первые дни БМ, но при благоприятном течении болезни слух восстанавливается в первые 2 нед заболевания. Н.В. Скрипченко [16] выделила группу риска больных по развитию нейросенсорной тугоухости, к которой относятся пациенты, перенесшие пневмококковый и гемофильный менингит, манифестирующие с ОРВИ или патологии верхних дыхательных путей (отит). В этой же работе были определены некоторые особенности течения БМ: вовлечение в остром периоде заболевания краниальных нервов и повышение уровня белка в ЦСЖ более 2,2 г/л при снижении уровня глюкозы менее 2,1 ммоль/л.
При выраженной нейросенсорной тугоухости целесообразна кохлеарная имплантация. При вестибулярном головокружении и неустойчивости рекомендуется короткий курс симптоматического (аналоги гистамина, нейролептики, барбитураты, бензодиазепины, антихолинергические препараты в возрастных дозировках) и вестибулярная реабилитация.
У 2 (5,4%) больных с генерализованной менингококковой инфекцией неблагоприятным исходом была арезорбтивная гидроцефалия (в 1 наблюдении требующая проведения шунтирующей операции), обусловленная снижением всасывающей способности пахионовых грануляций воспаленной паутинной оболочкой головного мозга. Клинически гидроцефалия проявляется увеличением размеров головы, выбуханием и напряжением большого родничка, расхождением швов черепа, расширением ликворных пространств; у детей старшего возраста — выраженной головной болью, появлением застоя на глазном дне. Гидроцефалия верифицируется на НСГ, КТ и МРТ в виде расширения желудочковой системы мозга за счет избыточного скопления ЦСЖ.
Консервативное лечение гидроцефалии направлено прежде всего на устранение бактериального возбудителя; также назначается диакарб (до санации ЦСЖ) из расчета 50—100 мг/кг в сутки у младенцев или до 750 мг в сутки у детей старшего возраста. Дренирующие операции показаны, когда гидроцефалия и клинические признаки повышения внутричерепного давления сохраняются или нарастают, несмотря на консервативное лечение. Профилактика гидроцефалии заключается в назначении своевременной и адекватной антибактериальной терапии.
У 2 (3,6%) больных с генерализованной менингококковой инфекцией и 1 больного с пневмококковым менингитом выявлены двигательные нарушения (спастический тетра-, гемипарез). У 1 больного, перенесшего пневмококковый менингит, выявлена энцефалопатия смешанного (инфекционно-токсический) генеза (см. клинический случай). Исходы Б.М. у обследованных детей и их дифференциация в зависимости от вида возбудителя представлены в табл. 3.
Таблица 3. Исходы Б.М. у обследованных детей в зависимости от вида возбудителя Примечание. У ряда пациентов выявлены различные клинические исходы БМ, в связи с чем их сумма не соответствует общему числу пациентов.
Эпидемиология
В развитых странах заболевание наблюдается в 80 % случаев у людей, которым меньше шестнадцати лет. Чаще всего болеют представители мужского пола. В 10 % случаев данная патология приводит к смертельному исходу, еще у 10 % инфицированных развиваются стойкие неврологические нарушения. Рост заболеваемости наблюдается в зимний период, в первую очередь из-за климатических условий (перепады температур, повышение влажности), а также длительного пребывания в закрытых помещениях. Каждые десять лет наблюдается увеличение частоты заболеваемости.
Вам будет интересно:Дефекация — что это такое?
Как передается бактериальный менингит, описано выше, распространен он во всех государствах мира, особенно в странах Африки, здесь патология встречается в 500 случаев на 100 000 человек. Длительное время данная патология считалась детской, так как, по данным статистики, раньше она наблюдалась у детей в возрасте 12-18 месяцев. После внедрения вакцинации заболевание стало часто наблюдаться и у взрослого населения. Сегодня патология диагностируется в 33 % случаях среди всех инфекционных болезней ЦНС.
Причины развития болезни
Гнойный бактериальный менингит могут вызвать различные бактерии (см. выше), в том числе и сальмонеллы, клебсиеллы и синегнойная палочка. Эти микроорганизмы обитают в окружающей среде и в организме человека. При воздействии негативных факторов они начинают стремительно размножаться и инфицируют клетки головного мозга.
Существует много причин, по которым заболевание может поражать организм каждого человека:
- травмы головы;
- снижение иммунитета;
- перенесение тяжелых воспалительных заболеваний;
- генетическая предрасположенность некоторых народов;
- инфицирование от переносчика инфекции.
Как и любое инфекционное заболевание, бактериальный менингит передается пищевым или воздушно-капельным путем, а также при непосредственном контакте с носителем инфекции: во время рукопожатия, поцелуя, чихания, использования общих предметов обихода. Поэтому медики рекомендуют строго соблюдать правила личной гигиены.
Актуальные проблемы диагностики и лечения бактериальных менингитов
Бактериальные гнойные менингиты (БГМ) занимают одно из ведущих мест в структуре нейроинфекций; заболеваемость ими находится в пределах 5–10 на 100 тыс. населения. Среди причин смертности от инфекционных болезней они занимают десятое место и второе после СПИДа в структуре летальности в инфекционных стационарах. Несмотря на наличие большого выбора антибактериальных препаратов, средств патогенетической терапии, летальность на протяжении последних 40–50 лет не снижается и остается в следующих пределах: 15–50% при пневмококковом менингите, 5–15% — при менингококковой инфекции, 3–20% — при гемофильном менингите. Клинически БГМ характеризуются такими синдромами, как лихорадочно-интоксикационный (гипертермия, миастения, миалгия, анорексия, токсическое поражение сердечно-сосудистой системы (ССС), центральной нервной системы (ЦНС) и вегетативной нервной системы и т. д.) и менингеальный (диффузная головная боль, сопровождающаяся тошнотой и рвотой, гиперестезия кожи, наличие ригидности мышц затылка, положительные симптомы Кернига, Брудзинского), а также характерными изменениями в спинно-мозговой жидкости — СМЖ (резкое повышение ликворного давления, изменение прозрачности, повышение уровня белка и лактата, высокий нейтрофильный плеоцитоз, снижение уровня глюкозы). При распространении воспалительного процесса на вещество мозга и развитии отека-набухания головного мозга присоединяется общемозговой синдром (нарушения сознания и психики, генерализованные судороги) и очаговая неврологическая симптоматика (парезы черепных нервов, конечностей, тазовые нарушения, мозжечковая симптоматика, патологические рефлексы и др.).
За 5 лет в ИКБ № 2 г. Москвы наблюдались 2148 больных БГМ, из них 776 в ОРИТ (37,2%). Лабораторно (бактериологически, реакция латексной агглютинации — РЛА) расшифрована этиология менингита у 38% больных. У 60% больных менингококковой инфекцией диагноз установлен клинически. Среди лабораторно подтвержденных случаев болезни менингококковый менингит (ММ) составил 64%, пневмококковый менингит (ПМ) — 21,3%, менингит, вызванный гемофильной палочкой типа В (HiВ-менингит) — 9,3%, однако в этиологической структуре детей HiВ-менингит находится на втором месте после менингококкового. 5,3% составили менингиты стафилококковой, стрептококковой, листериозной, клебсиеллезной, эшерихиозной этиологии. За последние 3 года, по нашим наблюдениям, имеется тенденция к более тяжелому течению болезни. Так, в 2004 г. в ОРИТ госпитализированы 37,8% больных, в 2005 г. — 39,1%, в 2006 г. — 49,9%, т. е. половина всех больных БГМ.
Причинами тяжелого состояния и летальности пациентов, поступивших в ОРИТ, в 86,1% являлись отек головного мозга (ОНГМ), ОНГМ в сочетании с инфекционным токсическим шоком (ИТШ), менингоэнцефалит. Летальность существенно колебалась в разные годы. Так, в 2005 г. она составляла 5,2%, а в 2006 г. выросла до 13,5%. Она существенно увеличилась при менингококковом, гемофильном менингитах и при менингитах неустановленной этиологии, составив соответственно в 2005 г. 3,8%, 0%, 5,9%, а в 2006 г. — 9,7%, 15,7%, 13,6% (табл. 1).
Рост летальности при гемофильном менингите за последний год обусловлен развитием у трех больных ИТШ. На 162 больных гемофильным менингитом, наблюдавшихся в течение последних 20 лет, летальность составила 3,7%.
Проведенный анализ диагностики, результатов лечения БГМ показывает, что наиболее актуальными практическими проблемами на современном этапе являются:
- ранняя клиническая диагностика на догоспитальном этапе и транспортировка больных в специализированные отделения;
- правильная оценка тяжести состояния больного с последующей адекватной терапией на догоспитальном уровне;
- ранняя диагностика и лабораторное подтверждение диагноза в стационаре;
- адекватная этиотропная терапия на всех этапах;
- ранняя оценка эффективности этиотропной терапии;
- квалифицированная интенсивная терапия и реанимация тяжелых больных в ОРИТ специализированных стационаров.
В Москве, несмотря на проведение постдипломной подготовки, чтение лекций и другие образовательные мероприятия, значительная часть больных госпитализируется в поздние сроки, часто после 2–3-кратного обращения больные направляются в непрофильные стационары. Так, при HiВ-менингите средний срок госпитализации составляет 3,2 сут; больные госпитализировались в пять различных стационаров, и только 54% — в ИКБ № 2. Однако летальность в ИКБ № 2 составляет 3,7%, а в непрофильных стационарах — 23,5%, т. е. выше более чем в 6 раз.
Установлено, что в ОРИТ поступают больные БГМ в поздние сроки, в среднем на 3,5 ± 0,2 дня болезни, в то время как в боксированное отделение (БО) практически в первые 2 дня (на 1,6 ± 0,3 дня болезни) (р < 0,001). В 38,3% случаев позднее поступление было обусловлено ошибочными диагнозами при первичном обращении больных за помощью. Причем в 2005 г. частота ошибок составила 27,3%, в 2006 г. — 45,8%, т. е. возросла в 2 раза.
По данным сопроводительных документов за 2005–2006 гг. установлено, что наиболее частыми ошибочными диагнозами при типичной клинической картине гнойного менингита были острое нарушение мозгового кровообращения (ОНМК), острая респираторная вирусная инфекция (ОРВИ), пиелонефрит, пневмония, алкогольный делирий, пищевая токсикоинфекция, холецистит, острая передозировка психотропных препаратов, отит, острый аппендицит, острая задержка мочи. Ошибочная диагностика приводила к тому, что больные госпитализировались в непрофильные стационары (23,4%), где в среднем до расшифровки диагноза проводили 1,8 сут и соответственно не получали необходимую квалифицированную помощь. Отмечались также случаи гипердиагностики, когда в ОРИТ (9,8%) и БО (16,6%) госпитализировались больные с подозрением на менингит, у которых диагностировались ОНМК, опухоль мозга, отравление психотропными препаратами, вторичный отогенный менингит, эпилепсия, ОРВИ, остеохондроз. Гипердиагностика также является отрицательным фактором для больных БГМ, так как в связи с тяжестью состояния возникала проблема перевода в профильный стационар и оказания специализированной помощи.
В стационаре исход болезни в значительной степени зависит от быстроты диагностики БГМ и его этиологической расшифровки, поскольку при отсутствии дополнительных симптомов БГМ различной этиологии клинически неразличимы.
На основании клинико-лабораторных данных этиологический диагноз установлен у 74% больных (в том числе только у 48% с использованием бактериологического метода и РЛА). При этом хотелось бы подчеркнуть роль посева крови. Гемокультуры получены у 58% больных HiВ-менингитом, 27% — ПМ и у 16% — генерализованной формой менингококковой инфекции (МИ). Результаты бактериологического исследования могут быть улучшены путем совершенствования техники исследования (забор материала, транспортировка, качество сред). Однако кардинальное повышение частоты расшифровки диагноза возможно только путем внедрения метода полимеразной цепной реакции (ПЦР). Так, еще в 1998–2000 гг. использование ПЦР позволило установить этиологию БГМ более чем у 80% больных.
При использовании рутинных методов диагностики наибольшие диагностические трудности представляют больные с 2–3-значным нейтрофильным или смешанным плеоцитозом СМЖ. В этой группе могут быть больные вторичными БГМ при сепсисе, абсцессах мозга, первичными БГМ в ранние сроки болезни или леченные антибиотиками, больные туберкулезным менингитом, вирусными нейроинфекциями в ранние сроки, субарахноидальными кровоизлияниями. Суммированные дифференциальные критерии представлены в таблица 2.
Мы придаем существенное диагностическое значение концентрации лактата в СМЖ и крови и их соотношению, что основано на результатах обследования в динамике более 200 больных.
Основные принципы и стандарты антимикробной терапии известны. Нами используются следующие препараты для эмпирической терапии БГМ: в зависимости от возраста применяется цефтриаксон, цефотаксим, ампициллин. В зависимости от выделенного возбудителя назначается этиотропная терапия: при менингококковом менингите — пенициллин, цефтриаксон, цефотаксим, цефепим; при пневмококковом — пенициллин, цефтриаксон, ванкомицин, меропенем, ципрофлоксацин; при HiВ-менингите — цефтриаксон, цефотаксим, пефлоксацин; при менингитах, вызванных энтеробактериями, — цефтриаксон, цефотаксим, пефлоксацин, цефепим; при стафилококковом — ванкомицин, рифампицин, оксациллин, меропенем, линезолид; при синегнойном — цефтазидим, ципрофлоксацин, цефоперазон, цефепим; при листериозном — ванкомицин, цефтриаксон, ампициллин; при лептоспирозном — пенициллин, ампициллин, цефотаксим; при менингите, вызванном бактероидами — метронидазол, Ко-тримоксазол, меропенем; при менингите, вызванном энтерококками, — ампициллин, амикацин, ванкомицин, меропенем. При тяжелом течении БГМ применяется эндолюмбальное введение ванкомицина, амикацина. Все более актуальной становится проблема резистентности возбудителей. За последние годы более отчетливо выявляется тенденция к появлению резистентных штаммов возбудителей к препаратам, используемым в практике лечения менингитов. Так, 4% штаммов менингококка и 3% пневмококков были устойчивы к пенициллину. Регистрируются отдельные полирезистентные штаммы менингококка и пневмококка.
Пока существует выбор препаратов 4–5 разных групп, а частота выделения резистентных к отдельным препаратам составляет не более 5–6%, эта проблема решается путем замены, однако в ближайшие годы проблема «старения» антимикробных препаратов в отношении лечения БГМ может стать очень острой, особенно если учесть стремление практикующих врачей широко применять, часто без достаточных обоснований, антибиотики, особенно новые. В результате появляются штаммы возбудителей менингитов, резистентные не только к пенициллину, левомицетину, но и к фторхинолонам, меропенему.
Другая проблема — отсутствие эффекта при лечении препаратами, к которым данный штамм возбудителя чувствителен. Этот феномен мы наблюдали в разных группах больных с частотой от 15 до 30%, что можно продемонстрировать на примере HiВ-менингита (рис.).
| Рисунок. Чувствительность HiB к антибиотикам, % |
Причины многообразны, в том числе:
- недостаточный пассаж препарата через гематоэнцефалический барьер (ГЭБ);
- наличие зон бионедоступности возбудителя;
- недостаточная доза или низкое качество препарата;
- несоответствие данных о чувствительности возбудителя in vitro и in vivo.
Нужно отметить, что у разных больных при одинаковых дозах препарата его концентрация в СМЖ различается в десятки раз. Недостаточный пассаж антибиотика может быть обусловлен особенностями патологического процесса и недостаточной ликворопродукцией. Так, при поступлении почти у 20% больных БГМ наблюдается ликворная гипотензия. По мере стихания воспалительного процесса уменьшается проницаемость ГЭБ, процесс резорбции СМЖ преобладает над ликворопродукцией, что отчетливо отражается на фармакокинетике препарата.
Существенное влияние на этот процесс оказывают диуретики, кортикостероиды. О наличии зон бионедоступности свидетельствуют частые высевы культуры возбудителя, особенно пневмококка, из трупного материала у умерших после длительного применения антибиотиков. Эти зоны создаются в сгустках экссудата, энцефалитических очагах, очагах размягчения мозговой ткани, гематомах, ячейках субарахноидального пространства, в желудочках мозга при вентрикулите. В этих случаях целесообразно (при чувствительности возбудителя) использование супермассивных доз пенициллина, применение интракаротидного и эндолюмбального методов введения антибиотиков. Применение препаратов низкого качества, в частности цефтриаксона индийского производства, нередко сопровождается обострением процесса, а иногда вообще неэффективно.
К сожалению, в последние годы особенности фармакокинетики антимикробных препаратов в условиях ОРИТ при проведении интенсивной терапии не изучались и, соответственно, отсутствуют рекомендации о коррекции с этих позиций антимикробной и патогенетической терапии.
Изучение чувствительности возбудителя является важным критерием, определяющим выбор препарата, но только в случае методически правильного исследования. Кроме того, имеются данные о том, что бактерии резко меняют свою активность при изменении условий существования. Не исключено, что эти изменения могут влиять на результаты определения чувствительности возбудителя, однако вопрос нуждается в изучении. Таким образом, проблема повышения эффективности этиотропной терапии БГМ требует фундаментальных исследований.
Сложной является оценка эффективности антибактериальной терапии в ранние сроки, особенно у больных с тяжелым течением БГМ, что часто приводит к необоснованной замене антибиотика. Так, например, при HiВ-менингите замена произведена у 68% наблюдавшихся нами больных, а обоснованная — только у 28%.
При принятии решения о замене препарата следует иметь в виду, что:
- у тяжелых больных оценка эффективности лечения возможна при ММ не ранее 2 сут, при HiВ-менингите — не ранее 3 сут, при ПМ — не ранее 3–5 сут;
- клинические показатели недостаточно информативны, так как улучшение состояния может быть связано с временным эффектом дегидратационной и дезинтоксикационной терапии, а ухудшение состояния, включая нарастание общемозговой, менингеальной и очаговой симптоматики, возможно и при эффективной антибактериальной терапии вследствие церебральных и экстрацеребральных осложнений (нарастание ОНГМ, внутричерепные гематомы, эпидурит, герпетическая инфекция, пневмония и др.);
- через 1–2 дня от начала лечения, даже при адекватной антимикробной терапии, возможен высев возбудителя из СМЖ, плеоцитоз может нарастать. В то же время при неэффективной терапии возможно снижение плеоцитоза;
- по нашим данным, наиболее ранними и информативными критериями эффективности этиотропной терапии являются: клеточный состав СМЖ, концентрация белка и глюкозы, лактата, pH, парциальное давление кислорода pO2 ликвора (табл. 3).
Совокупность этих данных в большинстве случаев позволяет в течение 2–3 сут реально оценить эффективность лечения и принять обоснованное решение о продолжительности лечения тем же препаратом или о его замене. Однако необходимо отметить, что при ПМ положительная динамика этих показателей может выявляться на 1–3 дня позже.
Следующим аспектом является своевременное решение об отмене антибиотика. По нашим данным, продолжительность антибиотикотерапии больных БГМ увеличивается в среднем на 1 сут за 8–10 лет. Так, в 1960–1970 гг. продолжительность пенициллинотерапии составляла в среднем 7 сут, после 2000 г. — 10 сут. В части случаев, особенно при необходимости замены препаратов в процессе лечения, пролонгирование лечения целесообразно, но существуют типичные ситуации, когда показаний для продолжения антибиотикотерапии нет.
- Длительная лихорадка при полном регрессе неврологической симптоматики и санации СМЖ, при отсутствии каких-либо гнойно-септических осложнений (пневмония, пиелит, эндокардит, постинъекционный абсцесс, инфицированный интравазальный катетер).
- Длительная лихорадка чаще всего наблюдается у больных HiВ-менингитом и менингококцемией. У таких больных причиной лихорадки чаще всего являются инфекционно-аллергические артриты, миокардит. У маленьких детей температура может нормализоваться после отмены антибиотиков. Эффективны нестероидные противовоспалительные препараты.
- Длительное сохранение лимфоцитарного плеоцитоза СМЖ в пределах от 100 до 200–300 кл/мкл при отсутствии неврологической симптоматики, нормальном уровне глюкозы и лактата СМЖ. По нашим данным, в этих случаях основную долю (более 90%) составляют Т-лимфоциты, главным образом Т-хелперы (СД4), а иммунорегуляторный индекс резко возрастает, достигая 4,8–5,5. Одновременно в несколько раз повышается содержание иммуноглобулинов различных классов. Таким образом, воспаление носит асептический характер и обусловлено местной реакцией иммунной системы.
Реже допускается преждевременная отмена антибиотиков — обычно у больных ПМ и HiВ-менингитом при удовлетворительном общем состоянии, регрессе неврологических показателей, невысоком плеоцитозе в пределах 40–100 в 1 мкл, при сохранении в СМЖ нейтрофилов 20–30%, снижении уровня глюкозы и повышении лактата, что свидетельствует о сохранении активности возбудителя. Нужно также учитывать такие показатели, как неврологически отягощенный преморбидный фон, волнообразность течения менингита, медленная санация СМЖ.
Преждевременная отмена антибиотиков в этих случаях приводит через несколько суток к обострению болезни.
Важнейшим направлением в снижении летальности является совершенствование методов интенсивной терапии и реанимации. Результат лечения в значительной степени обусловлен квалификацией врачей и среднего медицинского персонала, соблюдением в отделении санитарно-гигиенического режима. В ОРИТ должны работать врачи, имеющие два сертификата — реаниматолога и инфекциониста. Существенное снижение летальности может быть достигнуто благодаря превентивной интубации и раннему переводу больных с синдромом ОНГМ на искусственную вентиляцию легких (ИВЛ), до развития тяжелых степеней гипоксемии, отработке оптимальных режимов ИВЛ, отработке показаний для применения петлевых и осмотических диуретиков, кортикостероидов.
Таким образом, повышение эффективности качества оказания медицинской помощи больным БГМ является реальной перспективой. Оно может быть достигнуто за счет повышения уровня подготовки врачей поликлиник, скорой помощи и непрофильных стационаров по нейроинфекциям, улучшения диагностики в стационарах путем внедрения ПЦР, РЛА, совершенствования бактериологической диагностики, определения чувствительности к антибактериальным препаратам стандартизированными методами, включения в число рутинных методов обследования определения уровня лактата в СМЖ и крови, использования современных схем применения антибактериальных препаратов, объективных методов оценки их эффективности и определения на этой основе показаний для их замены, оптимизации продолжительности курса лечения, внедрения в практику ОРИТ превентивной интубации больных с тяжелым течением БГМ и раннего их перевода на ИВЛ, совершенствования методов патогенетической терапии.
Ю. Я. Венгеров, доктор медицинских наук, профессор М. В. Нагибина, кандидат медицинских наук, доцент Т. Э. Мигманов, кандидат медицинских наук, доцент Р. Н. Быкова В. Б. Ченцов, кандидат медицинских наук Г. В. Крючкова Т. Ю. Смирнова Т. И. Свистунова, кандидат медицинских наук В. А. Мясников МГМСУ, КБ № 2, Москва
Группа риска
Но при попадании инфекции в организм менингит развивается не всегда. Для его возникновения необходимы особые условия: расстройство иммунной системы и пропускная реакция организма. При присутствии этих факторов вредоносные бактерии свободно проникают в кровеносную систему и перемещаются в головной мозг. Поэтому в группу риска входят:
- лица, имеющие хронические заболевания;
- люди, злоупотребляющие алкоголем и никотином, наркотиками;
- ВИЧ-инфицированные;
- дети до трех лет.
Симптомы и признаки патологии
Вам будет интересно:Лучший детский психиатр в Москве: отзывы
Обычно бактериальный менингит симптомы проявляет не сразу. Длительность инкубационного периода зависит от возраста и состояния здоровья человека, но обычно он составляет четырнадцать дней. После этого заболевание начинает проявлять первые признаки, которые схожи с теми, что и при иных инфекционных болезнях:
- увеличение температуры тела;
- сильная головная боль, головокружение, лихорадка;
- воспаление верхних дыхательных путей, назофарингит;
- тошнота, сопровождающаяся периодической рвотой;
- отсутствие аппетита, диарея;
- гиперестезия и повышение мышечного тонуса.
Диагностика
Диагностика заболевания представляет определенные трудности в начальных этапах заболевания (единственными проявлениями которого может быть симптомы ОРВИ), однако в острый период диагностировать заболевания достаточно просто. При неврологическом осмотре выявляются симптомы раздражения мозговых оболочек (симптомы Брудзинского, Кернига, Гийена и другие). Свет и звуки усиливают головную боль. У детей часто развивается гидроцефальный крик.
Основу инструментальной диагностики бактериального менингита составляет взятие цереброспинальной жидкости. Давление ликвора повышено, ликвор может выходить напряженной струей. Сама жидкость мутная, вязкая. При анализе ликвора обращает на себя внимание клеточно-белковая диссоциация, преимущественно нейтрофильного характера. Количество клеток может превышать 1000 на 1 мкл. Происходит также снижение уровня глюкозы и электролитов. Посев ликвора на среды выявляет бактериальную природу заболевания, при необходимости проводят анализ на чувствительность к антибиотикам.
Специфические признаки
К специфическим признакам болезни относят:
- Симптом Кернинга. В данном случае человеку не удается поднять в горизонтальном положении прямую ногу на девяносто градусов.
- Симптом Брудзинского. Характеризуется невозможностью прислонить к груди голову, поднять плечи при нажатии на щеку, согнуть ноги при надавливании на лобковую область, непроизвольным сгибанием второй ноги при попытке согнуть первую.
В особо тяжелых случаях симптомы бактериального менингита у взрослых проявляются в виде геморрагической экзантемы, когда по всему телу появляются сосудистые звездочки или большие участки подкожных кровоизлияний. Затем происходит отек мозга, судороги и одышка, у человека развивается кома и отек легких.
У новорожденных детей заболевание проявляется напряжением родничка и неврологической симптоматикой. Нередко патология осложняется менингоэнцефалитом или эпендиматитом. В этом случае развивается сильная сонливость, парез и паралич, гидроцефалия. При отсутствии должной терапии заболевание развивается очень быстро, на протяжении одних суток. Поэтому при проявлении первых симптомов необходимо незамедлительно обратиться к врачу.
Как распознать менингит?
Менингококковая инфекция – крайне опасная и потенциально смертельная бактериальная инфекция, самая эффективная защита от которой – вакцинация. Шапка никак не защищает от менингита.
Менингит может начинаться как обычная ОРВИ: с насморком, болью в голе, повышенной температурой, и распознать на этом этапе серьёзное заболевание крайне сложно.
Наиболее уязвимы менингиту маленькие дети, а заболеть можно в любом возрасте.
Основные симптомы менингита:
- Высокая температура
- Сильная головная боль, плохо купирующаяся НПВП
- Рвота, часто сопровождающая головную боль
- Светобоязнь, звукобоязнь
- Напряжение (ригидность) затылочных мышц
- Запрокидывание головы назад
- Спутанность сознания, заторможенность, сонливость
- Судороги
- Напряжение, пульсация большого родничка (у малышей)
- Геморрагическая сыпь (ярко красные пятна с неровными краями)
Если вы заметили какие-либо из этих признаков у себя или членов своей семьи, то незамедлительно обращайтесь к врачу! Чаще всего болезнь развивается очень быстро и есть вероятность гибели ребёнка в первые часы заболевания!
Осложнения и последствия
Для здоровья человека последствия бактериального менингита имеют катастрофический характер. Одним из самых опасных осложнений выступает отек головного мозга, провоцирующий развитие комы, паралич органов дыхания и летальный исход. Также патология может стать причиной нарушения психики и деятельности ЦНС.
Часто последствия бактериального менингита у взрослых и детей бывают следующие:
- гидроцефалия;
- патологии почек и сердца;
- потеря слуха;
- васкулит, провоцирующий паралич ЧМН;
- инфаркт мозга, сопровождающийся фокальными судорогами, что постепенно переходят в эпилепсию;
- абсцесс головного мозга.
У детей после заболевания нередко развивается умственная отсталость, нарушение речи и памяти, расстройства психики. Часто наблюдается апатия, пассивность или, наоборот, агрессивность.
Диагностические мероприятия
Постановка такого диагноза, как гнойный бактериальный менингит, может быть проведена только при наличии результатов всех лабораторных анализов и люмбальной пункции, которую проводят путем введения иглы в позвоночник для сбора цереброспинальной жидкости.
В медицине используют следующие диагностические методики:
- Сбор и изучение анамнеза, изучение симптоматики патологии.
- Лабораторные анализы крови и мочи для определения воспалительного процесса и поражения внутренних органов.
- Спинномозговая пункция и исследование полученного материала.
- Бакпосев слизи из носа на наличие менингококка или пневмококка.
- ПЦР и ИФА.
- МРТ для выявления гидроцефалии, абсцесса.
- Исследование крови на кислотно-щелочной баланс.
Первичный диагноз ставится на основании менингиального комплекса симптомов, признаков интоксикации и синдрома воспаления в цереброспинальной жидкости. По результатам комплексного обследования ставят окончательный диагноз.
Материал и методы
Обследовали 55 пациентов с БМ в возрасте от 2 мес до 12 лет (средний возраст больных — 3,5±0,36 года). В выборке преобладали мальчики (58%).
У пациентов оценивали соматический статус, неврологические нарушения и глубину расстройства сознания с помощью шкалы комы Глазго (Glasgow Coma Scale — GCS).
Всем пациентам были проведены бактериологическое исследование слизи из носоглотки, микроскопия крови «в толстой капле», посев крови на стерильность, клинический и биохимический анализы крови, серологическое исследование крови в парных сыворотках — реакция непрямой гемагглютинации, реакция латекс-агглютинации, иммунологическое исследование сыворотки крови и цереброспинальной жидкости (ЦСЖ) с определением уровней интерферона-α, β и γ, прокальцитонина и неоптерина методом иммуноферментного анализа (ИФА). В лаборатории онтогенеза и коррекции системы интерфероногенеза Федерального научно-исследовательского центра эпидемиологии и микробиологии им. Н.Ф. Гамалеи исследовали обмен цитокинов методом ИФА.
В Центре молекулярной диагностики научно-исследовательского института эпидемиологии было проведено молекулярно-генетическое исследование сыворотки крови и ЦСЖ для амплификации генетического материала микроорганизма методом полимеразной цепной реакции.
Для диагностики церебральных осложнений были проведены нейросонография (НСГ) в отделении лучевой диагностики Инфекционной больницы № 2, компьютерная (рентгеновская) томография головного мозга (КТ) — в отделении лучевой диагностики той же больницы, магнитно-резонансная томография головного мозга (МРТ) — в отделении лучевой диагностики Детской городской клинической больницы им. З.А. Башляевой.
Статистическая обработка данных осуществлялась с помощью программ R Studio, Excel. Использованы критерии χ2 Пирсона, Уилкоксона и Андерсона—Дарлинга. Для контроля групповой вероятности ошибки использован метод Холма. Уровень достоверности выбран равным 0,05.
Терапия заболевания
Лечение бактериальных менингитов осуществляется в условиях стационара с применением интенсивной терапии. Антибактериальные препараты широкого спектра действия и хинолоны назначаются еще до получения результатов диагностики. Лекарства вводятся внутривенно или методом инъекций в канал спинного мозга. При этом за пациентом должно проводиться постоянное наблюдение, в случае возникновения судорог или припадков ему оказывают необходимую помощь. При появлении судорог назначаются противосудорожные медикаменты и препараты для снижения внутричерепного давления. Также совместно проводится терапия сопутствующих патологий. Врач выписывает жаропонижающие, обезболивающие и противовоспалительные препараты.
Также медики должны следить за водно-солевым балансом пациента, проводить соответствующие лечебные мероприятия в случае обезвоживания организма в результате диареи и рвоты. Так как бактериальный менингит часто приводит к развитию осложнений, необходимо следить и за состоянием внутренних органов, осуществлять контроль над кровяным давлением.
Для устранения симптомов интоксикации проводят дезинтоксикационную терапию, назначают диуретики. Но такие мероприятия противопоказаны при отеке мозга. Для лечения патологии используют и глюкокортикостероиды для устранения воспалительного процесса, что дает возможность снизить риск развития летального исхода и появление отдаленных осложнений. В случае необходимости проводят искусственную вентиляцию легких.
Лечение менингита
Лечение назначается в зависимости от возбудителя менингита.
Бактериальный менингит требует лечения в стационаре с внутривенным введением антибиотиков и глюкокортикостероидных препаратов, которые снижают риски осложнений и помогают выздоровлению.
При вирусном менингите антибиотики будут бесполезны. Чаще всего заболевание проходит самостоятельно в течение нескольких недель. При лёгкой форме необходим постельный режим с соблюдением питьевого режима, а также приём обезболивающих препаратов.
При более тяжёлой форме вирусного менингита назначают симптоматическое лечение и поддерживающую терапию. А если причиной заболевания является вирус герпеса, то в этом случае будет назначено введение противовирусных препаратов.
Бывают также случае, когда причину менингита выявить не удаётся, тогда врач назначает терапию вслепую, куда входят и антибиотики, и противовирусная терапия. Это продолжается до тех пор, пока точная причина не будет выявлена.
При грибковом менингите назначаются противогрибковые препараты, но так как эти препараты могут иметь сильные побочные эффекты, лечение назначается только после того, как из лаборатории придёт подтверждение грибковой природы менингита.
Если менингит вызван аллергическими реакциями или аутоиммунными заболеваниями, но их могут лечить препаратами кортизона. В других случаях лечение может не понадобиться, так как причина может пройти сама по себе.
Реабилитация
После лечения патологии пациент должен находиться под наблюдением у невролога на протяжении двух лет. В первый год он должен проходить обследование один раз в три месяца, а затем один раз в полгода. Восстановление после заболевания является сложным и многогранным процессом, который включает:
- Соблюдение диеты. Все продукты, употребляемые в пищу, должны быть вареными или приготовленными на пару. Рекомендуется употреблять нежирное мясо и рыбу, молочные продукты, компоты и кисели.
- Физиотерапия, которая включает массаж, электрофорез, электросон, магнитотерапию.
- ЛФК с применением гимнастических упражнений, роботизированных тренажеров.
- Эрготерапия, направленная на бытовую адаптацию человека из-за снижения физических возможностей пациента.
- Когнитивная терапия для восстановления внимания, мышления и памяти.
Бактериальный менингит: профилактика
С целью профилактики менингита необходимо соблюдать все правила антисептики при терапии ЧМТ, а также изолировать пациентов, которые инфицированы, в отдельные палаты. Медики рекомендуют своевременно проводить вакцинацию против данного заболевания. При контакте с носителем инфекции необходимо посетить врача для назначения антибактериального препарата с целью профилактики менингита. Необходимо вести здоровый образ жизни, соблюдать правила личной гигиены, следить за своим здоровьем, своевременно проводить лечение хронических заболеваний.
Менингит выступает опасной болезнью, которую лучше предупредить, чем потом лечить. Нередко заболевание приводит к серьезным проблемам со здоровьем, которые носят постоянный характер.
Источник