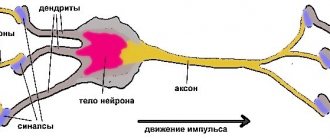
Миоклоническая эпилепсия — разновидность эпилептических приступов. Характеризуется более мягким течением. Впервые болезнь проявляется у младенцев или детей раннего возраста. Дебют миоклонической эпилепсии во взрослом возрасте нетипичен. Данная форма заболевания характеризуется вялым подергиванием мышц. Симптомы напоминают тики или гиперкинезы. В некоторых случаях возможно тяжелое течение. В международной классификации болезней МКБ-10 миоклоническая эпилепсия имеет код G40.3.
Пройти диагностику и лечение заболевания в Москве можно в Юсуповской больнице. Обследование проводят опытные неврологи и эпилептологи с использованием современного медицинского оборудования. Терапия соответствует европейским стандартам качества и безопасности.
Причины миоклонической эпилепсии
В настоящее время точные причины развития миоклонической эпилепсии не установлены. Однако, врачи выделяют несколько предрасполагающих факторов. Среди них:
- Наследственная предрасположенность. Определенные виды миоклонической эпилепсии имеют наследственную обусловленность. Например, болезнь Унферрихта-Лундборга, синдром Драве. Если у одного из родственников была диагностирована эпилепсия, то последующие поколения находится в группе риска. Вероятность возникновения заболевания составляет 20-30%.
- Внутриутробная инфекция. Некоторые инфекционные агенты способны проникать через плацентарный барьер. В результате повышается риск развития не только миоклонической эпилепсии, но и психических расстройств, дефектов развития. Миоклоническая эпилепсия развивается в конце 2-3 триместра.
- Заболевания в период беременности не инфекционного характера. К данной группе болезней относится сахарный диабет, патология щитовидной железы, почечная, печеночная, сердечная недостаточность.
- Бесконтрольный прием препаратов во время беременности. Некоторые лекарственные средства обладают выраженными тератогенными свойствами. Поэтому их прием негативно сказывается на развитии плода. Доктора советуют во время беременности избегать приема лекарств. При возникновении необходимости все назначения должны быть выполнены врачом.
- Спонтанные мутации. Причины подобных изменений до сих по не изучены. Выделяют провоцирующие факторы, наличие которых способствует мутационным процессам. Среди них стресс, резкие перепады температуры, чрезмерная физическая нагрузка.
Общие положения
Эпидемиология
Согласно немногочисленным имеющимся в наличии эпидемиологическим данным, СДМЭД составляет менее 1% всех эпилепсий (Центр Св. Павла, 1997), 1,3% и 1,72% эпилепсий, которые начинаются в первый год жизни (Далла Бернардина и др., 1983), и 0,39% эпилепсий, начинающихся в первые 6 лет жизни (Охтсука и др., 1993).
Пол
Распределение по полу: 52 мальчика и 27 девочек.
Генетика
Генетика СДМЭД неизвестна. Больных мало, а случаи семейного СДМЭД описаны не были. В семейном анамнезе эпилепсия или фебрильные припадки (ФП) присутствуют у 39% из 80 больных. У 70 больных заболеваемость ФП в семье составляла 17%, а заболеваемость эпилепсией — 24%. Трудно оценить тип эпилепсии, обнаруживаемый у родственников. В 10 случаях это, вероятно, была идиопатическая эпилепсия. В случае, описанном Арзиманоглоу и др. (1996), пробандом был 2-й из 2 братьев, а старший страдал типичной эпилепсией с миоклонически-астатическими припадками (ЭМАП, синдром Дуза).
Анамнез жизни
В анамнезе большинства больных патологии до начала МП не было. Только у двух (1,9%) были сопутствующие заболевания: синдром Дуза (Драве и др., 1992) и гиперинсулиновый диабет (Коламария и др., 1987).
Однако случаи ФП не являются редкими: 19 больных из 64 (30%). ФП были всегда простыми, однако редкими (1-2) и наблюдались до наступления миоклоний и до начала лечения (15 случаев).
Симптомы миоклонической эпилепсии
Клиническая картина миоклонической эпилепсии зависит от вида заболевания. Среди основных патологических симптомов выделяют:
- Судороги. Заболевание характеризуется миоклоническими приступами. Они не сопровождаются выраженным болевым синдромом. Судороги чаще всего затрагивают конечности, реже лицо и туловище. В среднем продолжительность припадка составляет 10-20 минут. Сознание при этом сохраняется.
- Потеря сознания. Возникает крайне редко. Характерна для юношеской формы.
- Тонико-клонические судороги. Данная форма припадка сопровождается потерей сознания, болезненным сокращением мышц.
- Олигофрения. Умственная отсталость встречается в различных вариантах. Чаще всего это расстройство творческого мышления, интеллекта.
- Психические расстройства. Выражаются галлюцинациями, неврозами и пограничными состояниями.
Определение клинической симптоматики необходимо для подбора корректной терапии. Врачи Юсуповской больницы разрабатывают индивидуальный план лечения для каждого пациента.
Течение и лечение
У детей с СДМЭД не наблюдаются припадки какого-либо другого типа, даже если они остаются без лечения (до 8,5 лет у одного нашего больного), особенно это касается малых эпилептических или тонических припадков. Результаты клинического обследования нормальные. Интериктальный миоклонус был описан только Джиованарди-Росси и др. (1997) у 6 больных. Анализируя состояние наших больных, мы обнаружили легкий интериктальный миоклонус у 2 по записям ЭЭГ. Многие больные не были обследованы, но когда КТ и МРТ были выполнены, результаты оказались нормальными (33 больных).
Исход, вероятно, зависит от раннего диагноза и лечения. Миоклонии легко поддаются монотерапии вальпроатом, развитие ребенка при этом соответствует возрасту. При отсутствии лечения у больного продолжаются миоклонические припадки, что может привести к нарушению психомоторного развития и поведенческим отклонениям.
Более или менее досконально способы лечения апробированы на 74 больных. У 65 больных проводилась монотерапия, у 6 — политерапия, у 3 лечение не проводилось. Монотерапия включала вальпроат (ВПА), фенобарбитал (ФБ), нитразепам (НТЗ). 6 больных получали терапию примидоном (ПРМ) и этосуксимидом (ЭСМ). В результате лечения припадки исчезли у 69 больных (93%).
Эти данные подтверждают, что при СДМЭД ВПА является препаратом первого выбора. Однако лечение должно проходить под контролем концентрации препарата в плазме, т.к. неправильный прием может привести к рецидиву или вызвать резистентную к препаратам эпилепсию.
Диагностика миоклонической эпилепсии
Миоклоническая эпилепсия требует проведения комплексной диагностики. Обследование включает в себя:
- Сбор жалоб и анамнеза заболевания. На первичном осмотре невролог опрашивает пациента об имеющихся жалобах, времени их появления, выраженности симптоматики. Помимо этого, уточняется продолжительность приступов, состояние после них.
- Неврологический осмотр. Врач оценивает рефлексы, проводит тестирование для оценки состояния нервной деятельности.
- ЭЭГ. Благодаря исследованию получается установить патологическую активность различных структур головного мозга. Подобным образом определяется очаг поражения.
- МРТ. Для усиления эффекта обследование проводится с использованием контраста. Миоклоническая эпилепсия не характеризуется наличием структурных изменений в головном мозге. Однако, бывают исключения.
В Юсуповской больнице для диагностики миоклонической эпилепсии используется современное медицинское оборудование. Оно позволяет быстро и эффективно установить наличие заболевания. На основании полученных данных назначается корректная терапия.
Отдаленные результаты и прогноз
Длительность наблюдения за 63 больными составила от 9 мес. до 27 лет, из них за 45 пациентами наблюдали около 5 лет. Возраст больных в период наблюдения — от младше 5 до старше 15 лет.
Во всех случаях МП купировались. Длительность заболевания известна у 52 больных: у большинства из них МП длились менее одного года, у 7 — от 1 до 2 лет, только у 5 — более двух лет.
О возникновении генерализованных эпилептических припадков (ГЭП) после прекращения МП сообщалось в случае 10 больных без сопутствующих МП.
Было доложено о результатах наблюдения 74 больных.
Приступы прекратились у 28 больных в возрасте старше 6 лет. У 6 детей этого же возраста приступы сохраняются: при фотостимуляции — у 2 (Драве и др., 1992), по неизвестной причине — у 3 (Джиованарди-Росси и др., 1997). Также приступы сохраняются у 13 больных младше 6 лет. 3 больных младше 6 лет остались без лечения (Риччи и др., 1995). О 24 больных информации нет.
Картина ЭЭГ известна для 55 больных. Она быстро нормализовалась у 23. Редкие спонтанные генерализованные СВ сохранялись у 13. Фотосенситивные изменения наблюдались у 6. Интересно, что фотосенситивность может появиться после исчезновения МП и персистировать долгие годы после прекращения МП вплоть до взрослого возраста. Были также представлены фокальные нарушения. Они были записаны у 5 больных во время пробуждения как СВ в двух лобно-центральных и теменных областях, иногда в лобно-теменной и лобно-височной. Они исчезали с течением времени. Напротив, у других больных они появлялись только во время сна. Они еще сохранялись в конце периода наблюдения у 5 наших больных, и только во время сна.
В целом психологический исход благоприятный, и большинство больных выздоровели. Это точно известно в 69 случаях. 57 (83%) были здоровыми, из них 38 в возрасте 5 лет и старше. У 10 (14%) была легкая заторможенность, они посещали специализированную школу, но никто из них не был помещен в больницу. У 2 больных (3%) была нарушена познавательная способность и выявлены отклонения в формировании личности: у одного пациента был синдром Дауна и сильная чувствительность, у другого до 5 лет были МП с чувствительностью к ИРС и к закрытию глаза. Это психотическое нарушение появилось у него в возрасте 10 лет и прогрессировало.
Этот психологический исход частично зависит от ранней диагностики, позволяющей провести соответствующее лечение и убедить семью в хорошем будущем.
Эти данные подтверждают обычно хороший прогноз СДМЭД. Приступы, вызванные шумом или разговором, было легче контролировать, чем спонтанные. Фотосенситивность же было труднее контролировать, она сохранялась на протяжении нескольких лет после прекращения припадков.
Виды миоклонической эпилепсии
Миоклоническая эпилепсия делится на несколько видов. Рассмотрим основные из них.
Младенческая миоклоническая эпилепсия
Диагностируется в 30-40% случаев. Характеризуется симптомами по типу гиперкинезов или тиков. Слабая степень развития заболевания может протекать незаметно на протяжении многих лет. На фоне младенческой миоклонической эпилепсии не страдает интеллектуальное развитие. Заболевание может проявиться у ребенка с 2 месяцев до 3 лет.
Синдром Драве
Выявляется на первом году жизни. Симптоматически напоминает младенческую миоклоническую эпилепсию. Синдром Драве вызывает выраженные психические расстройства. Они проявляются олигофренией, умственной отсталостью. Без корректного лечения количество приступов увеличивается до нескольких раз в неделю.
Болезнь Унферрихт — Лундборга
Считается генетическим заболеванием. Характеризуется тяжелой неврологической симптоматикой. Болезнь Унферрихт — Лундборга также сопровождается психическими нарушениями. Первый приступ чаще всего проявляется в период полового созревания. Болезнь диагностируется в 10-20% случаев.
MERRF эпилепсия
Чаще диагностируется у взрослых. Миоклоническая эпилепсия юношеского возраста характеризуется тонико-клоническими пароксизмами. Болезнь не сопровождается неврологическими расстройствами, психическими нарушениями. Сознание на фоне приступа остается ясным.
Абсансы — разновидность эпилептического приступа. Считаются одним из симптомов миоклонической эпилепсии.
В зависимости от прогрессирования эпилепсии выделяют следующие формы болезни:
- Прогрессирующая. Клиническая картина эпилепсии постепенно нарастает. По мере прогрессирования заболевания увеличивается риск летальных исходов. В некоторых случаях болезнь плохо поддается лечению.
- Стабильная. Симптоматика остается на примерно одном уровне.
- Ремитирующая. Признаки эпилепсии могут медленно развиваться, а затем затухать на продолжительное время. Со временем возможно полное исчезновение патологических признаков.
ТИПЫ ПРИСТУПОВ ПРИ ИДИОПАТИЧЕСКИХ ГЕНЕРАЛИЗОВАННЫХ ЭПИЛЕПСИЯХ
Абсансы — генерализованные приступы, сопровождающиеся кратковременной утратой сознания, остановкой взора и наличием на ЭЭГ специфических паттернов в виде генерализованных синхронных регулярных комплексов «пик-волна» частотой 3-3,5 Гц. Такие абсансы называются типичными.
Впервые описаны Poupart в 1705 году, и позже Tissot в 1770 году, который использовал тер-мин «petitaccess.» Термин «абсанс» впервые использовал Calmeil в 1824 году.
Связь между утратой сознания и комплексами пик-волна 3 Гц на ЭЭГ была выявлена и описана Gibbs, Davis, и Lennox в 1935 году.
Распространенность этого типа приступов- 1,9-8 на 100,000. Типичные абсансы встречаются чаще у девочек — 2:1. Абсансы с миоклонусами чаще встречаются у мальчиков.
У 90,6% больных приступы сопровождаются вариабельными двигательными компонентами (сложные абсансы): автоматизмы — 63%, миоклонический компонент -45,5%,снижение постурального тонуса — 22,5%, повышение постурального тонуса — 4,5%. В одном приступе обычно имеют место два или три двигательных компонента, но три и более встречаются редко. При наличии двигательных компонентов в структуре приступа абсанс обозначается как сложный, в их отсутствие – как простой.
Классическим ЭЭГ-паттерном абсансов являются генерализованные билатерально-синхронные комплексы пик-волна частотой 3 Гц (Рис. 1). Комплексы пик-волна быстрее в начале разряда (в основном около 4 Гц), затем замедляются до 3,5-3 Гц в основной порции и к концу приступа замедляются до 2,5 Гц. Если пик-волновой разряд длительный, то частота может снижаться до 2 Гц. Если пик-волновой разряд развился до начала записи, то дифференциация комплексов «пик-волна» и «острая-медленная волна» может быть затруднительной.
Максимум пик-волновой активности почти всегда находится над лобными отделами по срединной линии, а минимум находят в височных и затылочных отведениях.
Начало пик-волновой активности в срединных отведениях лобной области на означает, что источником активности являются отделы лобной доли в непосредственной близости от межполушарной борозды, что характерно для всех первично-генерализованных эпилепсий.
Хотя классические пик-волновые комплексы билатерально синхронные и симметричные, и асинхрония обычно не превышает 20 мсек, они могут начинаться на 100-200 мсек раньше или быть более выраженными над одним из полушарий. Однако такое преобладание может менять свою сторонность в течение одной или нескольких записей. Редко классические пик-волновые разряды регистрируются над одним полушарием.
По крайней мере, у 40% пациентов с идиопатическими генерализованными эпилепсиями регистрируются очаговые эпилептические разряды на межприступной ЭЭГ.
Клинические проявления абсанса обычно выражены, когда длительность разряда превышает 5 секунд. Более короткие вспышки обычно протекают без очевидных проявлений.
Абсансы не являются обязательным и единственным видом приступов, которые сопровождаются разрядами комплексов пик-волна на ЭЭГ — частота клинически явных абсансов колеблется от 26% до 70%; частота grandmal — 37-86%; частота миоклоний — 14-27%.В небольшом числе случаев имеют место тонические, атонические приступы или только фебрильные судороги.
Дифференциальная диагностика абсансов наиболее часто проводится с атипичными абсансами, сложными фокальными приступами лобного и височного происхождения, неэпилептическими «замираниями».
Атипичные абсансы встречаются главным образом у детей с тяжелыми симптоматическими или криптогенными эпилептическими синдромами, которые представлены сочетанием атипичных абсансов, атонических, тонических, миоклонических и генерализованных судорожных приступов. Клинически начало и окончание атипичного абсанса более постепенные, изменения мышечного тонуса более выражены, может быть послеприступная спутанность сознания. На ЭЭГ — нерегулярные пик-волны частотой менее 2,5 Гц или другие варианты эпилептической активности (Рис. 2). Фоновая биоэлектрическая активность, как правило, изменена.
Замирание с утратой реактивности могут входить и в структуру сложных фокальных приступов при височной или лобной эпилепсиях. «Лобные» абсансы (очаг в области полюса лобной доли) клинически могут не отличаться от типичных абсансов, дифференциальная диагностика основывается на данных ЭЭГ.
Клинические отличия сложных фокальных приступов при височной эпилепсии и типичных абсансов при ИГЭ представлены в таблице 3.
Таблица 3
Дифференциальная диагностика типичных абсансов и сложных фокальных приступов при височной эпилепсии.
| Признак | Сложные фокальные приступы (височная эпилепсия) | Типичные абсансы |
| Аура | Часто | Никогда |
| Длительность | как правило более 1 минуты | Обычно несколько десятков секунд |
| Провокация гипервентиляцией | Редко | Как правило |
| Фотосенситивность | Редко | Часто (зависит от синдрома) |
| Утрата сознания | Обычно глубокая | Вариабельная (зависит от синдрома) |
| Автоматизмы | Практически всегда; часто вовлекаются туловище и ноги ипсилатерально. Дистоническая установка контралатеральных конечностей в 40% случаев. | До 2/3 случаев. Минимальная выраженность. Туловище и ноги вовлекаются редко. |
| Амбулаторные автоматизмы | Часто | Только при статусе абсансов |
| Клонические судороги | Редко; односторонние в конце приступа | Часто; двусторонние, обычно в области рта и/или век |
| Бессудорожный статус | Как исключение | Может встречаться |
| Послеприступные симптомы | Практически всегда спутанность сознания, часто амнезия и дисфазия | Никогда |
В отличие от типичных абсансов, которые прерывают текущую деятельность, неэпилептические замирания, как правило, возникают в периоды отсутствия деятельности, могут быть прерваны внешними стимулами и не сопровождаются моторными компонентами и разрядами на ЭЭГ.
Миоклонус характеризуется быстрыми непроизвольными мышечными сокращениями,как правило, с движением в суставах, генерализованными или ограниченными отдельной группой мышц, преимущественно во флексорах. Эпилептический миоклонус сопровождается эпилептическими разрядами на ЭЭГ.
Если эпилептический разряд приводит к «выключению» мышечного тонуса, то может возникать короткое движение под влиянием гравитации. Такой вариант называется «негативным» миоклонусом.
Генерализованный тонико-клонический приступ – вариант приступа, представленный последовательными фазами непрерывного сокращения мышц (тоническая фаза) и прерывистых сокращений (клоническая фаза) с утратой сознания. Приступ начинается с утраты сознания и резкого тонического напряжения всех мышц длительностью 30-40 секунд. В этой фазе появляется резкий цианоз. Далее появляются ритмичные судороги мышц с постепенным увеличением интервалов между отдельными сокращениями длительностью до нескольких минут. После сокращения наступает полное расслабление и кратковременное коматозное состояние, которое переходит в сон.
Лечение миоклонической эпилепсии
Для терапии миоклонической эпилепсии применяются медикаментозные средства. Врачи Юсуповской больницы применяют следующие группы препаратов:
- противоэпилептические;
- барбитураты;
- транквилизаторы;
- ноотропы.
Каждому пациенту разрабатывается индивидуальный план лечения. Он учитывает форму миоклонической эпилепсии, стадию развития, возраст больного и наличие сопутствующих заболеваний. Такой подход позволяет быстро и эффективно подобрать терапию. В Юсуповской больнице прием ведут опытные неврологи, эпилептологи, психиатры. Реабилитацию проводят квалифицированные массажисты, инструкторы ЛФК. Для того чтобы записаться на прием, необходимо позвонить по телефону или оставить заявку на официальном сайте больницы.
СПИСОК ЛИТЕРАТУРЫ:
- Диагностика и лечение эпилепсий у детей. Под ред. Темина П.А., Никаноровой М.Ю. // М.: Можайск-Терра. – 1997. – 656 с.
- Евтушенко С.К., Омельяненко А.А. Клиническая электроэнцефалография у детей // До-нецк. – 2005. – с. 539-546, 585-594
- Мартинюк В.Ю. Протокол лікування епілепсії, епілептичних синдромів. Протокол лікування епілептичного статусу у дітей.–Київ,2005.
- Мухин К.Ю., Петрухин А.С. Идиопатические формы эпилепсии: систематика, диагности-ка, терапия — М.: Арт-Бизнес-Центр, 2000 – 319 с.
- Эпилептология детского возраста: Руководство для врачей / Под ред. А.С. Петрухина. — М.: «Медицина», 2000. — 620 с.
Юношеская миоклоническая эпилепсия (ЮМЭ) как отдельная форма идиопатической генерализованной эпилепсии с возрастозависимым началом была выделена в 1969 г. D. Janz [1], хотя имеются данные и в более ранней работе этого автора, совместной с W. Christian, в которой она была названа «импульсивной petit mal» [2]. Кроме того, имеется первое описание больного, которое датируется 1867 г. [3]. Тем не менее, несмотря на длительный период изучения ЮМЭ, в настоящее время остаются вопросы и нерешенные проблемы в отношении ее диагностики и лечения.
В статье проведен сравнительный анализ результатов наших исследований в соответствии с работами других авторов. Сравнивались результаты исследования В.А. Карлова и Н.В. Фрейдковой [4] 72 больных ЮМЭ, а также новой выборки больных за последние 5 лет (20 человек) с материалами исследований отечественных и зарубежных авторов, относящихся к тому же временному периоду. Рассмотрена эволюция проблемы в аспектах клинической диагностики, терапии, прогноза заболевания и социальной адаптации больных ЮМЭ.
Возраст дебюта данной формы эпилепсии в литературе указан с большим разбросом, что связано с нефиксированной точкой начала заболевания. Это объясняется тем, что дебютом заболевания, как правило, являются миоклонии, которым больные, а зачастую и врачи не придают должного значения. Если в предыдущих наших исследованиях ранний дебют отмечен в 10 лет, а поздний в 26, то сейчас зафиксирован случай более раннего дебюта, а именно — в 9-летнем возрасте.
Что касается генетического аспекта ЮМЭ, то еще в работах F. Elmslic и соавт. [5] и позднее другими авторами [6—8] были идентифицированы патологические гены — BRD2
и
EFHCI
с локусом на хромосомах 6p21, 6p12—p11 (
EJM1
) и 5q14 (
EJM2
) с дефектом одного из генов — миоклонином. Кроме того, подтверждено наличие распространенных нарушений на микроструктурном уровне в белом веществе головного мозга — в лобной доле и мозолистом теле. Наличие этих изменений связывается с лобной когнитивной дисфункцией, на что обратил внимание еще D. Janz [1], который первым описал эту форму заболевания. Он же подчеркивал, что, хотя большинство случаев ЮМЭ и являются изолированными (единичными), примерно у 1/3 пациентов имеется заболевание эпилепсией в семье. Данные P. Thomas и соавт. [9] указывают, что в семьях больных ЮМЭ наблюдается сегрегация больных с идиопатической генерализованной эпилепсией, и примерно около 5% родственников I степени больны эпилепсией.
По данным наших последних наблюдений, эпилепсия в семье отмечалась у 1 родственника I степени и у 5 родственников I степени по данным опубликованных ранее исследований. В 2014 г. было проведено исследование [10] клинико-генеалогических данных у пробандов с ЮМЭ и членов их семей. Изучены 13 неродственных семей, в которых как минимум 2 члена страдали эпилептическими приступами. Не был обнаружен ни материнский, ни какой-либо другой тип наследования. Найден гетерогенный фенотип у лиц II и III степени родства: в семьях с ЮМЭ обнаруживаются другие формы эпилепсии, в частности с генерализованными тонико-клоническими приступами (ГТКП) у лиц с поздним началом ЮМЭ.
Приводим соответствующее собственное наблюдение.
Больная 18 лет обратилась с жалобами на приступы с 11-летнего возраста — «такие же, как у матери», при пробуждении, и единичный генерализованный судорожный приступ (ГСП) в 13-летнем возрасте. Последние два года принимает конвулекс по 750 мг 2 раза в сутки, приступов не было. Срыв клинической ремиссии наступил с возникновения приступа «вокруг сна» (при засыпании).
Рождена от 23-летней матери, роды в срок, стимулированные. Мать больной ранее лечилась с диагнозом ЮМЭ: роняла предметы из рук, были утренние подергивания в руках. По назначению невролога принимала в течение года люминал, а затем три года фенитоин (дифенин), что, естественно, усилило приступы. В 20-летнем возрасте самостоятельно прекратила принимать назначенные противоэпилептические препараты (ПЭП), в это же время приступы практически прекратились: остались только подергивания, провоцируемые психоэмоциональным стрессом.
При обследовании самой больной в неврологическом статусе выявлена легкая асинергия Бабинского. МРТ головного мозга показала обширную субарахноидальную кисту в левой лобно-теменной области, несомненно врожденную. На предыдущей ЭЭГ имели место мягкая дезорганизация фона, отсутствие фотосенсетивности и эпилептиформного ответа на гипервентиляцию. В то же время в фазе медленноволнового сна были зарегистрированы эпилептиформные разряды по типу острой-медленной волны и спайк-волны, в основном возникающие в лобных отведениях, локальные или иногда генерализующиеся. Последняя ЭЭГ показывает значительную их редукцию.
В приведенном наблюдении имеется ряд особенностей. Во-первых, у матери больной с клинической картиной ЮМЭ в 20-летнем возрасте на фоне самоотмены ПЭП (которые, кстати, ей были противопоказаны) сохранилась только редкая психоэмоциональная провокация миоклоний. Во-вторых, у дочери сочетание утренних миоклоний с единичными генерализованными судорожными приступами (ГСП), связанными со сном, дает известное основание для диагноза ЮМЭ. В то же время можно, как мы полагаем, квалифицировать данный случай как «стертую» форму ЮМЭ, поскольку отсутствовали характерные вздрагивания и падения предметов из рук. Можно полагать, что у матери имелась «стертая» форма ЮМЭ. В принципе, эти наблюдения подтверждают существование проблемы миоклоний, связанных со сном, возможно, за пределами эпилепсии.
Как известно, ЮМЭ имеет характерный клинический паттерн: билатеральные, чаще асимметричные нерегулярные аритмичные толчкообразные миоклонические подергивания мышц плечевого пояса и самих рук различной амплитуды. При этом миоклонические подергивания в значительной степени игнорируются больными, в связи с чем пациенты, как правило, не обращаются с этими жалобами к врачам. Однако вряд ли их можно назвать неосознаваемыми, поскольку на наводящие вопросы врача следует описание больным этих приступов. Скорее, данный феномен можно объяснить характерными особенностями психики больных (анозогнозия) [1].
Другим характерным клиническим проявлением этой формы эпилепсии является генерализованный миоклонический феномен — вздрагивание. В отличие от физиологических вздрагиваний данное проявление заболевания при ЮМЭ возникает не столько во сне, сколько в период пробуждения. У одной из наблюдаемых нами пациенток вздрагивания преобладали при отходе ко сну. Это сближает ЮМЭ с эпилепсией с ГТКП пробуждения, при которой припадки могут проявляться «вокруг сна».
Подтверждается сочетание миоклоний в большинстве случаев с редкими ГТКП (60%). По нашим последним наблюдениям, среднее время возникновения ГТКП после появления миоклоний составило около 4 лет. Сочетание миоклонии только с абсансами остается довольно редким явлением: ранее мы наблюдали всего один случай, за последние 5 лет подобных случаев в наших наблюдениях не было.
Сочетание миоклоний, ГТКП, атипичного абсанса и ауры, что вызывает некоторые диагностические трудности, нашло отражение в следующем клиническом наблюдении.
Больная Х.
, 29 лет, обратилась в июле 2013 г. Она по профессии психолог, но не работает.
Пренатальный и постнатальный анамнез без особенностей, наследственность не отягощена, со слов матери, «выдавливали» во время родов. На фоне видимого здоровья, но при этом хронического недосыпания, в апреле 2012 г. во время поездки на работу в поезде случился первый и единственный ГТКП с предшествующим ощущением нереальности происходящего (более точно его описать пациентка не смогла). Ко времени обращения к нам уже была назначена терапия — топамакс 50 мг в сутки, ламиктал 100 мг 2 раза в сутки. Это вызвало ухудшение — появление вздрагиваний, чаще связанных со сном.
При МРТ на одном из аксиальных базальных срезов в режиме Т2 обнаружено усиление сигнала от полюса левой височной доли. ЭЭГ сна представлена эпизодами генерализованных спайков и полиспайк-волн единичных и/или продленных до нескольких секунд (в этих случаях напоминающих атипичный абсанс).
Учитывая, что в анамнезе у больной была операция по поводу двустороннего поликистоза яичников (менструальный цикл не нарушен), а средством первой линии выбора при доминирующем клиническом проявлении миоклоний может быть леветирацетам, было принято решение отменить ламиктал и добавить кеппру 500 мг 2 раза в сутки. В сентябре 2013 г. был второй ГТКП, который пациентка амнезировала, но при этом, видимо, чувствовала его начало (ушла из кухни и легла в постель). Кроме того, бывает изолированное трудноидентифицируемое состояние дереализации. Подергивания при этом уменьшились. Доза кеппры была увеличина до 750 мг 2 раза в сутки и присоединен топамакс по 50 мг 2 раза в сутки (с учетом избыточной массы тела пациентки). Последовало учащение приступов до одного в неделю в состоянии бодрствования, пациентка самостоятельно отменила ПЭП. После чего ГТКП не было, однако в ночное время во сне случались общие вздрагивания. При проведении 12-часового ЭЭГ-мониторинга зарегистрированы в периоды бодрствования и сна билатерально-синхронные пик-волновые и полипик-волновые разряды частотой 3,5—4, длительностью 3—5 с.
Этот случай вначале представлял диагностические трудности: дифференциальный диагноз проводился между ЮМЭ и фенокопией ЮМЭ. Не характерным, хотя и возможным для ЮМЭ было начало заболевания с ГСП, учащение судорожных приступов в ходе заболевания и картина ЭЭГ, в значительной степени представленная коррелятом атипичного абсанса. Другой особенностью, которая и послужила вначале поводом для обсуждения диагноза ЮМЭ, было появление миоклоний, как правило, связанных со сном, в связи с их появлением после назначения комбинации топамакса (прописанного в связи с избыточной массой пациентки) с ламотриджином. Поскольку оба этих препарата, хотя и редко, могут провоцировать появление миоклоний, сам по себе факт возникновения миоклоний не после пробуждения, а во время сна не отрицал диагноза ЮМЭ. Наконец, существенно еще одно обстоятельство: самоотмена препаратов совпала со спонтанной ремиссией ГСП, хотя вздрагивания сохранялись. Таким образом, данный случай демонстрирует, что миоклонии являются сущностью заболевания. Что касается ГСП, очевидно, что первый из них был спровоцирован недосыпанием, а последующее появление и учащение приступов приходится расценивать как результат неэффективного или даже парадоксального эффекта ПЭП.
Вернемся к диагнозу. Дебют заболевания с 10-летнего возраста, когда отмечались кратковременные эпизоды «замирания» и вздрагиваний; первый приступ, возникший в поезде, видимо, связанный с дефицитом сна, и генерализованные изменения, выявленные при ЭЭГ, могли бы свидетельствовать об идиопатической природе заболевания: ЮМЭ относится к идиопатической эпилепсии с варьирующим фенотипом. В то же время у пациентки с ГСП имеет место трудноидентифицируемая аура, которая также бывает в виде изолированного проявления; трансформация судорожных приступов из асинхронных в приступы бодрствования — признаки, характерные для симптоматической и в значительной степени — криптогенной эпилепсии. Уже в классификации 1989 г. была выделена форма эпилепсии с синдромами, имеющими признаки как фокальных, так и генерализованных. В предложенной позже и до сих пор не принятой классификации в разделе «Эпилептические синдромы и родственные состояния» вышеуказанная рубрика удалена [11, 12]. Однако новый состав Комиссии Международной противоэпилептической лиги (МПЭЛ) по классификации и терминологии эпилепсии, возглавляемый I. Scheffer [13], недавно предложил ввести раздел «Неклассифицированные эпилепсии», в который относятся случаи, не распознающиеся как известные электроклинические синдромы, или неизвестной этиологии. Таким образом, данный случай не относится к конкретным электроклиническим синдромам и может быть причислен к неклассифицируемым формам эпилепсии.
Так как ЮМЭ может изначально длительно проявляться только миоклониями, особая ценность принадлежит ЭЭГ. ЭЭГ при ЮМЭ характеризуется такими особенностями, как наличие коротких вспышек полиспайк- и спайк-волн 3—6 в с (рис. 1); разряды генерализованных симметричных спайк-волн 3 в с и редко 1—2 в с; эпилептические разряды, отличающиеся высокой, иногда гигантской амплитудой. Чаще выявляется лобно-долевая активность (рис. 2 и 3), сон резко активизирует эпилептиформную активность, при этом акцент также может обнаруживаться и в некоторых других отведениях. Хотя клинически абсансы наблюдались в единичных случаях, во время записи ЭЭГ коррелят абсанса зарегистрирован в 18,1% в ранних исследованиях и в 15% более поздних, в то время как ЭЭГ-коррелят миоклоний — у половины пациентов.
Рис. 1. ЭЭГ больной Х., 29 лет, с ЮМЭ.
Рис. 2. ЭЭГ больной Х., 29 лет. Лобно-долевая активность.
Рис. 3. Локализация эпилептического очага по данным отведений для ЭЭГ (объяснение в тексте).
У больных с ЮМЭ широко распространены фокальные ЭЭГ-проявления [14]. Так, в исследованиях E. Montalenti и соавт. [15], К.Ю. Мухина и соавт. [16] выявлены высокая частота региональных изменений и асимметрия диффузных пик-волновых разрядов. По мнению указанных авторов, эти «нетипичные» изменения на ЭЭГ нередко являются причиной ошибочного диагноза фокальной эпилепсии с феноменом вторичной билатеральной синхронизации. В связи с этим уместно упомянуть, что отечественные авторы подчеркивают: классическая клиническая картина является основополагающей в постановке диагноза, а ЭЭГ является всего лишь вспомогательным дополнительным методом исследования.
К сожалению, несмотря на характерную клиническую картину заболевания и прогресс в методиках исследования, в настоящее время все еще остается открытой проблема диагностики и назначения корректной терапии, хотя и наблюдаются положительные тенденции. Если ранее ставился правильный диагноз и адекватная терапия назначалась только 34,8% больных, то по данным последних исследований, стартовая терапия была корректно подобрана для 50%. Отметим, кстати, что все еще иногда назначается фенитоин.
Проблема диагностики подтверждается и некоторыми зарубежными работами. Так, ретроспективное наблюдение 200 пациентов с ЮМЭ, проходивших амбулаторно-поликлиническое обследование за 2014—2015 гг. [17], обнаружило некорректно поставленный диагноз в 49 случаях с дебютом заболевания с ГТКП и регистрацией на ЭЭГ в 56% случаев генерализованных спайк-волновых или полиспайк-волновых разрядов. В случаях начала заболевания с миоклонических приступов диагноз не вызывал трудностей. Почти половине пациентов были назначены неадекватные ПЭП, остальным рекомендовано наблюдение. По сравнению с данными исследований 1998 г. частота ошибочного диагноза стала меньшей, а время постановки корректного диагноза короче. Тем не менее диагностика «с первого взгляда» все еще остается проблемой среди неврологов, даже если имеют место типичные изменения в ЭЭГ.
Обоснованный диагноз ЮМЭ, однако, еще не гарантирует оптимального ответа на терапию. Этот факт нашел свое отражение в работе [18] по исследованию 116 пациентов с ЮМЭ, наблюдаемых по меньшей мере 18 мес каждый. У 68 пациентов за последние 12 мес приступов не было, а у 48 был зарегистрирован хотя бы один приступ разного типа. Наиболее частыми негативными факторами, обнаруженными в последней группе, были: короткий период наблюдения, лекарственное средство, отличное от вальпроевой кислоты (ВК), плохая приверженность к терапии. В частности, в связи с этим авторы рекомендуют шире использовать вальпроаты. Другими исследователями [19] отмечено, что у 19% из 201 пациента с ЮМЭ с отсутствием реакции на ВК обнаружены существенные корреляции и ассоциации с психическими расстройствами. Это, а также другие проблемы терапии и причины возникновения рецидива рассматриваются в этой статье.
Одной из проблем в терапии ЮМЭ, как и при других формах эпилепсии, являются побочные реакции.
Больная З.
, заболела в 11—12 лет, когда появились подергивания по утрам после сна, роняла из рук предметы. Были проведены МРТ- и ЭЭГ-исследования, после чего нарушения были расценены как функциональные тики. В 15-летнем возрасте перенесла сальмонеллез, на фоне которого развилась резкая головная боль, сопровождающаяся рвотой, усиливающаяся при вертикализации. Прошла курс лечения в инфекционном отделении, однако головная боль не была купирована, заподозрен объемный процесс в головном мозге. В мае того же года обследована в Научном центре неврологии, был поставлен диагноз «миоклонии» и назначены клоназепам и финлепсин. Отмечался положительный эффект стартовой терапии, но на контрольных ЭЭГ сохранялась эпилептиформная активность. Спустя год на фоне вынужденной самоотмены препаратов (закончились ПЭП на отдыхе) утром развился ГТКП. Была увеличена дозировка клоназепама. Четырьмя годами позже во время утреннего туалета в ванной комнате был эпизод кратковременной потери сознания, послеприступного сна не было.
В это время больная впервые обратилась к авторам статьи, и было изменено лечение: назначен депакин энтерик по 300 мг 3 раза в день. Состояние пациентки значительно улучшилось: подергиваний не наблюдалось, а все последующие ЭЭГ были с положительной динамикой. Однако появились побочные реакции: увеличение массы тела, нарушение менструального цикла, гирсутизм. Было решено назначить кеппру по 750 мг 2 раза в день и уменьшить дозировку депакина. Так как побочные эффекты депакина сохранялись, пришлось в течение года полностью снять депакин, но через 3 мес продолжалось ухудшение ЭЭГ. При увеличении дозировки кеппры до 2000 мг в день состояние оставалось прежним. Во время одного из приступов пациентка чуть не упала на лестнице, вновь в терапию ввели депакин 300 мг/сут. Спустя год на ЭЭГ зарегистрировано выраженное ухудшение, по согласованию с больной было решено перейти на комбинированную терапию топамаксом по 100 мг 2 раза в день и депакином энтерик по 300 мг 2 раза в день. На ЭЭГ стала отмечаться положительная динамика. Позже была проведена попытка снять депакин, однако усилилась слабость в руках, появилась неуверенность по утрам, закатывание глаз, на ЭЭГ регистрировалась отрицательная динамика. Было решено вернуться к дозировке депакина по 300 мг 2 раза в день.
Данный случай мы приводим не для иллюстрации побочных эффектов ВК, они общеизвестны, а для того чтобы показать, какие трудности могут возникнуть при ее непереносимости. Возможно, надо было попытаться применить другие формы ВК.
Известно, что чаще ЮМЭ встречается у лиц женского пола в соотношении 2:1. Это отражает другую сторону проблемы — гендерный аспект. Несмотря на то что вальпроаты по эффективности действия являются препаратами первой линии при ЮМЭ, они во многих случаях не могут быть использованы в эффективной дозе у лиц женского пола репродуктивного возраста из-за выраженных побочных явлений, как это было проиллюстрировано выше. Эта проблема обсуждалась Европейской академией неврологов, и была принята рекомендация ограничения применения вальпроатов у этой категории больных [20].
V. Puri и соавт. [21] попытались найти нейрофизиологический механизм преобладания заболеваемости у женщин с использованием метода транскортикальной магнитной стимуляции у ранее не лечившихся больных. Найдена повышенная активность в корковой ингибиторной нервной сети, «очевидно вследствие длительного кортикального периода молчания». Это явление было обнаружено только у пациентов женского пола, чем авторы объясняют повышенную чувствительность к данному заболеванию в когорте у женщин и соответственно возможное значение гормонального фактора (эстроген).
В связи со сказанным является актуальным дальнейший поиск альтернативного препарата ВК для терапии ЮМЭ у женщин.
Заменой вальпроатов при лечении ЮМЭ может являться леветирацетам, высокоэффективный в отношении как миоклоний [22, 23], так и в блокировании интериктальных эпилептиформных разрядов и фотопароксизмального ответа на ЭЭГ [24].
В 2007 г. было проведено исследование [25] 30 пациентов, лечившихся леветирацетамом, из которых 80% достигли полной ремиссии при монотерапии леветирацетамом. При этом финальные терапевтические дозировки колебались от 12 до 50 мг/кг в сутки. Данное исследование подтвердило вероятность рассмотрения леветирацетама в качестве препарата первой линии при ЮМЭ.
Одним из авторов данной статьи совместно с Н.В. Фрейдковой [26] было проведено исследование, в котором оценивалась эффективность применения невысоких доз вальпроатов и леветирацетама в лечении идиопатических форм эпилепсии, у 13 из 23 пациентов была ЮМЭ. При этом группа пациентов с ЮМЭ (как в сочетании с ГТКП, так и без них) была наиболее репрезентативна в достижении наилучшего терапевтического эффекта. Так, комплексная терапия упомянутыми ПЭП привела к медикаментозной ремиссии у 6 из 8 больных; в 1 наблюдении частота приступов снизилась более чем на 75%, и еще в 1 — более чем на 50%.
В другом исследовании [27] эффективности леветирацетама в монотерапии у 4 пациентов с ЮМЭ (2 пациенткам из которых препарат был назначен впервые в связи с планированием беременности, остальные были переведены на терапию карбамазепином в связи с уточнением диагноза) применение ПЭП позволило достичь ремиссии приступов в течение 6 мес.
В то же время, по некоторым данным литературы [28], леветирацетам не уступает по эффективности вальпроатам. Отечественными авторами проведено обширное ретроспективное исследование базы данных 1159 пациентов Волгоградской области, из которых 78 страдали ЮМЭ. Срок наблюдения составил от 1 года до 6 лет. В 56% случаев пациенты с диагнозом ЮМЭ находились на монотерапии вальпроатами, в 17% случаев применялся леветирацетам. Частота достижения медикаментозной ремиссии составила 83%, при этом при применении монотерапии вальпроатами — 92%, леветирацетамом — 87%. Полная клинико-ЭЭГ-ремиссия достигнута в 41% случаев, преимущественно при применении вальпроатов.
Также наряду с изучением вальпроата проведено проспективное рандомизированное исследование [29] по применению ламотриджина у пациентов с дебютом ЮМЭ во взрослом возрасте, в котором сравнивали его эффективность и переносимость относительно В.К. Получены данные, свидетельствующие об эффективности и лучшей переносимости ламотриджина именно у взрослых пациентов с ЮМЭ, хотя распространенность идиосинкразических реакций может быть причиной беспокойства.
Следует отметить, что в современной научной литературе не поднимается вопрос о состоянии детей, рожденных от больных ЮМЭ матерей, а также роли мужской наследственности. Приведем несколько примеров из нашей практики, в частности в таких случаях, как описываемый далее.
Больная Л.
, 37 лет, впервые обратилась в 18-летнем возрасте после ГСП, в связи с тем, что у нее прекратился менструальный цикл (приступ был накануне начала менструации). Второй ГСП сна случился через неделю уже на фоне менструации. В дальнейшем был лишь единичный ГСП. Что касается миоклоний, то они периодически повторялись. Пациентка жаловалась на частые тревожные сны, в связи с чем был назначен феназепам. В первый раз при обследовании больной на ЭЭГ обнаружены комплексы острая—медленная волна лобно-височной локализации по альтернирующему типу, последней ЭЭГ в состоянии бодрствования был отмечен эпизод генерализованных высокоамплитудных спайк-волн с максимальной выраженностью в передних отделах головного мозга. За все это время пациентка была три раза беременна, две беременности прерваны по социальным показаниям, одна состоялась. На январь 2015 г. ребенку 15 лет. Он отличался девиантностью поведения, снижением уровня интеллекта; до 13 лет у него был ночной и дневной энурез, учится в коррекционной школе.
С момента возникновения заболевания пациентка постоянно принимает депакин хроно по 300 мг 2 раза в сутки и ламотриджин (ламолеп) по 100 мг 2 раза в сутки. Судорожных приступов нет, сохранились вздрагивания по утрам.
Следует отметить, что результаты исследования K. Meador и соавт. [30] продемонстрировали снижение IQ (коэффициент интеллекта) у детей школьного возраста, матери которых применяли ВК во время беременности, на 7—10 пунктов по сравнению с другими ПЭП.
На сегодняшний день проведен ряд исследований отдаленных исходов использования ВК во время беременности, результаты которых свидетельствуют о 3-кратном увеличении частоты расстройств аутистического круга и 4-кратном — аутизма у детей наряду с популяционными показателями. Часть работ дает основание полагать, что у таких детей развивается синдром дефицита внимания и гиперактивности [31—33].
Влияние ВК на умственное и физическое развитие детей при ее применении в период беременности зависит от дозировки, хотя порог доз не определен. Данная проблема и ряд вопросов беременности при ЮМЭ на фоне монотерапии ВК подробно рассмотрены в статье П.Н. Власова [34].
Наличие перечисленных проблем подтверждается существованием таких случаев, как приводимый ниже.
Судорожные приступы возникли у 6-летнего ребенка, рожденного от отца с ЮМЭ. Дебют заболевания у отца начался со сложного парциального приступа во сне (автоматизм). Ему была назначена стартовая терапия карбамазепином (финлепсин) по 200 мг 2 раза в сутки. На этом фоне у пациента наряду с повторяющимися сложными парциальными приступами появились приступы «вздрагивания». На ЭЭГ была обнаружена региональная и генерализованная спайк- и полиспайк-волновая активность. Затем постепенно карбамазепин был заменен на депакин по 500 мг 2 раза в сутки. Эпилептическая активность на ЭЭГ регрессировала, подергивания прекратились. Спустя два года с учетом клинико-ЭЭГ-ремиссии была проведена попытка снижения дозы депакина до 600 мг в сутки при концентрации препарата в крови 48,3—50,8 мкг/мл, однако на ЭЭГ появилась абсансная активность в периоде ночного сна. При повышении дозы до 300 мг утром и 500 мг вечером произошло возобновление вздрагиваний в руках. Полная ремиссия была достигнута при дозе препарата 1000 мг в сутки (по 500 мг на 2-кратный прием). Что касается ребенка, то перинатальный анамнез, со слов родителей, не отягощен, но он наблюдается у невролога с диагнозом «детский церебральный паралич, симптоматическая эпилепсия с редкими судорожными приступами на фоне противоэпилептической терапии».
К сожалению, генетический анализ в описанном случае не проводился, поэтому возможный вклад генетического фактора остается недоказанным. Другим немаловажным, но нерешенным как для самого пациента, так и для членов его семьи остается вопрос дальнейшего прогноза болезни.
В работе J. Gaithner и соавт. [35] на основании анализа больных, наблюдавшихся не менее 25 лет, выделены факторы неблагоприятного прогноза: начало с ГСП, предшествующих миоклониям, безуспешность терапии и политерапии. В разрез общепринятому мнению, длительное лечение не обязательно, кроме тех пациентов, у которых имеются указанные факторы неблагоприятного прогноза. В то же время в наших исследованиях у 30 больных отмена ПЭП после 5-летней медикаментозной ремиссии оказалась возможной лишь у 9, в остальных случаях наступал рецидив. Не исключено, что данное явление в какой-то степени связано с поздним началом адекватно подобранной терапии. По нашим наблюдениям, за последние 5 лет отмечено 3 случая из 20 с полной клинико-медикаментозной и ЭЭГ-ремиссией на фоне лечения ВК и/или леветирацетамом.
В исследовании К.Ю. Мухина и соавт. [16] у 106 пациентов с ЮМЭ клиническая ремиссия была достигнута в большинстве случаев (89,6%), а клинико-ЭЭГ — в 22%. У большинства пациентов (79%) применяли монотерапию, наиболее часто использовали ВК (56%), реже — леветирацетам (13%). К сожалению, несмотря на высокую эффективность лечения, авторы отмечают высокий процент (92%) возникновения рецидивов, наиболее часто — на этапе снижения дозы более чем на 50% и в течение первого года после отмены. Авторы связывают это с такими достоверными факторами, как недосыпание (23,5%), самостоятельная отмена, снижение дозы или пропуск приема ПЭП, замена на дженерики (21%).
О затруднениях в социальной адаптации, необычном стиле жизни и плохом сотрудничестве с врачом у пациентов с ЮМЭ впервые упомянули D. Janz и W. Cristian [2]. Подобные изменения, достигающие степени психических нарушений, зарегистрированы в 25,6% [36, 37].
Поскольку своеобразные психические нарушения у больных с ЮМЭ связываются с когнитивными нарушениями за счет лобных долей [20, 38], бразильские авторы предприняли специальное исследование в этом направлении на контингенте из 42 пациентов с несомненным диагнозом ЮМЭ и 42 лиц контрольной группы с применением батареи тестов. Полученные данные показали, что пациенты с ЮМЭ имеют худшую адаптацию в 2 значимых аспектах жизни — работе и семейных отношениях, однако этот фактор коррелирован не с когнитивными нарушениями, а с высокой частотой приступов и импульсивностью [39].
Значимым фактором для больного и его родственников является ранний прогноз заболевания. Авторы одной из работ [40] изучали чувствительность к закрыванию глаз при ЮМЭ и эффективность прогноза у 76 пациентов с минимальным сроком наблюдения в течение года. У 15,8% был плохой прогноз в связи с резистентностью к адекватным ПЭП, 19,7% были псевдорезистентны (т.е. их неправильно лечили) и 64,5% имели хороший прогноз. Они также изучали чувствительность к закрыванию глаз. Она была обнаружена только у 4 (5,3%) больных и только тех, у которых был плохой прогноз. Таким образом, фотосенситивность, вероятно, относится к факторам, ухудшающим прогноз.
В литературе имеются данные [41], касающиеся связи фотопароксизмального ответа на ЭЭГ и данных оптической когерентной томографии. У группы пациентов с наличием фотопароксизмального ответа на ЭЭГ было обнаружено увеличение толщины retina nerve fiber layer
обоих глаз и сосудистой оболочки правого глаза. Толщина сетчатки обоих глаз была существенно меньше. Авторы считают, что данные микроструктурные особенности могут быть связаны с фотосенситивностью у пациентов с ЮМЭ. В других исследованиях [40] было показано, что eye closure sensitivity (ECS) у пациентов с ЮМЭ является редкой ЭЭГ-находкой и не может быть достоверным маркером плохого прогноза.
Известно, что одну из главных ролей в патогенезе ЮМЭ играет нарушение корковой пластичности. Группа итальянских ученых [42] изучали синаптическую пластичность моторной коры посредством метода парной ассоциативной стимуляции у пациентов с ЮМЭ и выявили соответствующие изменения.
Приведенные данные свидетельствуют о положительных сдвигах в диагностике и лечении ЮМЭ. Тем не менее, несмотря на характерную клиническую картину заболевания и прогресс современных методов исследования, а также большой клинический опыт, вопрос диагностики этой формы эпилепсии остается проблемой для неврологов. Определены факторы, отягощающие прогнозирование: сочетание миоклоний с ГТКП, наличие психических нарушений, фотосенситивность, отсутствие должного ответа на адекватные ПЭП. Открытым в настоящий момент все еще остается гендерный аспект заболевания, особенно в отношении терапии. Необходимо также накопление научной информации о детях, рожденных от матерей с ЮМЭ, и роли отцовской наследственности.
Авторы заявляют об отсутствии конфликта интересов.
Дифференциальный диагноз
Если миоклонии начинаются в первый год жизни, их надо дифференцировать с криптогенными детскими судорогами (ДС). ДС клинически отличаются от доброкачественных миоклоний: они более тяжело протекают, включают в себя тонические судороги во всем теле, что никогда не наблюдается при СДМЭД; единичные судороги всегда сочетаются с серийными приступами у данного ребенка; возникновение долгих серийных спазмов происходит после пробуждения. Затем СД на ЭЭГ демонстрируют типичную картину коротких тонических сокращений, которую хорошо описали Руско и Вигевано (1993); редко имеют место длительные миоклонии. Иктальная ЭЭГ переменная: внезапные прерывистые гипсаритмии выравниваются наложенными быстрыми ритмами, большой медленной волной, за которой следует выравнивание или отсутствие видимых изменений. Наступление ДС связано с поведенческими изменениями, затруднением речевого контакта, замедлением психомоторных достижений.
На интериктальной ЭЭГ всегда есть патологические признаки: истинная гипсаритмия, или видоизмененная гипсаритмия, или фокальные нарушения, на них не определяются отдельные или короткие всплески билатеральных синхронных СВ или СДМЭД.
Если психомоторное развитие и ЭЭГ в пределах нормы по результатам нескольких обследований, выполненных во время бодрствования и сна, припадки, похожие на ДС, должны навести на мысль о диагнозе доброкачественного неэпилептического миоклонуса, описанного Ломброзо и Фейерманом (1977). У этих больных даже иктальная ЭЭГ без патологических изменений (Драве и др., 1986; Пашатс и др., 1999).
На первом году жизни может развиваться миоклоническая эпилепсия младенчества, она всегда начинается с длительных и частых фебрильных судорожных припадков, а не с отдельных миоклонических приступов. На втором году психомоторное развитие замедляется.
Если миоклонии начинаются после первого года жизни, можно заподозрить криптогенный синдром Леннокса — Гасто (СЛГ). При СЛГ (Бюмане и Драве, 1992) приступы в основном не миоклонические, а миоклонико-атонические, а чаще тонические, приводящие к внезапным падениям и травмам. Их ЭЭГ картина неоднородна, а в иктальном периоде высокоамплитудная или выравнивается, или определяется высокая медленноволновая активность, за которой следуют низкоамплитудные волны. В самом начале интериктальные ЭЭГ могут быть нормальными, в дальнейшем могут появиться типичные диффузные разряды медленной СВ. Типичные электроклинические признаки во время сна могут быть отложенными по времени. Диагноз основывается на быстрой связи припадков разного типа, таких как атипичные абсансы и аксиальные тонические судороги, на постоянных поведенческих нарушениях поведения и появлении новых навыков и неэффективности антиэпилептических препаратов.
Если миоклонические приступы изолированные или связаны с БЭП, необходимо рассмотреть диагноз миоклонической астазической эпилепсии раннего детского возраста (ЭМАП), хотя при этом синдроме миоклонические астанические припадки редко начинаются до возраста 3 лет (Дуз, 1992). Есть два существенных различия: 1) клинический аспект припадков со ступором, которые не наблюдаются при СДМЭД (Гуеррини и др., 1994); 2) ЭЭГ признаки тоже разные: СВ и ПСВ более многочисленные, сгруппированы в долгие вспышки, связанные типичным тета-ритмом над центро-теменными зонами. Но некоторых больных, вероятно, следовало бы классифицировать как СДМЭД. Подобным образом Дельгадо-Эскуэта и др. (1990) в группу обследованных или больных включили, вероятно, под названием миоклонической эпилепсии детского возраста (МЭРД) случаи как ЭМАП, так и СДМЭД.
Наконец, следует учитывать и другие эпилепсии, начинающиеся в первые три года жизни, при которых миоклонии являются основным типом приступов и которые имеют изменчивый прогноз. Они неоднородны: сочетание приступов других типов, постоянные фокальные нарушения на ЭЭГ, замедленное психомоторное развитие в прошлом, плохая реакция на лечение, неясный прогноз (Драве и др., 1992).
Клиническое обследование больного с целью постановки диагноза.
Это обследование — достаточно простое. Для него необходим тщательный сбор анамнеза и повторные видео-ЭЭГ записи, чтобы продемонстрировать наличие МП с генерализованными СВ разрядами, спонтанными или такими, которым способствуют сонливость, шум, контакт или ИРС. Записи сна позволяют показать слабую активацию разрядов и фокальных нарушений. Полезно использовать нейровизуализацию для подтверждения отсутствия поражения мозга, но она не является обязательной при наличии типичной симптоматики. Более полезно психоневрологическое обследование для проверки психомоторного развития и прослеживания течения заболевания.