Разрушение клеток и их связей с полной дисфункцией называется атрофией головного мозга. Субатрофией головного мозга именуется частичная местная утрата функций мозга. При таком заболевании, как церебральная атрофия головного мозга продолжительность жизни не изменяется, так как нейроны отмирают постепенно и, согласно статистике, в большинстве случаев смерть наступает от других болезней. Однако данный недуг характеризуется прогрессированием, подводящим пациента к деменции (приобретенному слабоумию).
Атрофия головного мозга: причины, симптомы, диагностика
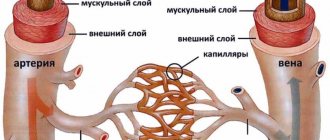
Атрофические изменения коры головного мозга приводят к разрушению нейронных связей, снижению активности функциональных центров. Состояние приводит к нарушению внутримозгового метаболизма, слабоумию, формированию ряда психических заболеваний (Альцгеймера, боковой амиотрофический склероз, деменция).
Клинические симптомы зависят от вида, стадии, степени заболевания. Мультисистемная форма сопровождается диффузной гибелью нейронов, постепенной утратой функций организма.
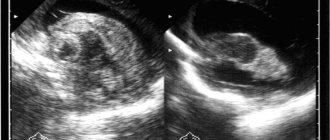
Атрофия мозга на МРТ
Симптоматика
Атрофические повреждения головного мозга сначала проявляются в едва заметных переменах: человек предается апатии и равнодушию, у него исчезают стремления и появляется вялость, ухудшается память. Утрачиваются прежние навыки и с трудом приобретаются новые. Часто происходит сильное отступление от нравственных норм, повышается раздражительность и конфликтность, происходят резкие перепады настроения, депрессии.
Наблюдаются и такие симптомы:
- оскудение лексикона – затяжной подбор нужных слов для выражения обыкновенных реалий;
- снижение мозговой активности;
- исчезновение самокритики, способности к осмыслению;
- расстройства чувствительности, эректильная дисфункция;
- ухудшения моторики;
- паркинсонизм.
Мыслительные функции продолжают ухудшаться вместе с самочувствием. Снижается способность различать объекты и пользоваться ими. Обнаруживается синдром «зеркала», при котором больной непроизвольно повторяет чужие поведенческие привычки. Постепенно почти прекращается психическая деятельность и наступает полная недееспособность (стадия маразма), личность распадается.
Специфическая симптоматика при церебральной атрофии мозга головы зависит от вовлечения различных участков. Например, нарушения функций лобных долей негативно влияют на поведение и возможности интеллекта, а повреждения мозжечка влияют на моторику, походку, речь и почерк. При повреждении нервных соединительных путей могут возникнуть вегетативные нарушения.
Причины возникновения атрофии мозга
После 50 лет увеличивается риск нейродегенеративных состояний. Повышают вероятность появления нозологической формы провоцирующие факторы:
- Снижение функции почек (недостаточность);
- Длительное увеличение внутричерепного давления (гидроцефалия);
- Частое употребление алкоголя, наркотические средства;
- Инфекционное поражение коры мозга (ретровирусы, полиомиелит, энцефалит);
- Черепно-мозговая травма;
- Сосудистые заболевания (тромбоз, атеросклероз, аневризма);
- Метаболические состояния;
- Психические болезни – Альцгеймера, синдрома Иценко-Кушинга, Паркинсона, Уиппла, Геллервордена-Шпатца.
Увеличивает вероятность нозологии – метаболические расстройства, родовые травмы, половые инфекции, недостаток витаминов группы B, фолиевой кислоты.
Основные причины возникновения атрофии коры мозга
Научные исследования показывают высокую вероятность поражения кортикальных и субкортикальных структур у людей 50-55 лет из-за генетической предрасположенности. Кортикальная атрофия развивается у пациентов, страдающих наследственной хореей Хантингтона.
Другие причины:
- Черепно-мозговые травмы, сопровождающиеся гематомой, гибелью нейронов, формированием кист;
- Хронический алкоголизм, наркомания, прием некоторых медикаментов обеспечивает уменьшение толщины полушарий мозга, подкоркового шара. Длительная спиртовая интоксикация нарушает внутриклеточный метаболизм, обеспечивает постепенное отмирание нейронов;
- Хроническую церебральную (мозговая) ишемию формируют сосудистые заболевания (атеросклероз, гипертоническая болезнь). Недостаток поступления кислорода способствует необратимой гибели тканей;
- Врожденная гидроцефалия у новорожденных приводит к повышению внутричерепного давления, атрофии мозгового вещества;
- Более семидесяти процентов случаев заболевания у людей старше 55 лет приходится на долю нейродегенеративных заболеваний – Пика, Леви, Альцгеймера, Паркинсона. Нозологии формируют старческое слабоумие.
Менее частые этиологические факторы нозологии – гипоксия новорожденных, гидроцефалия, множественные врожденные кисты у ребенка.
Причины церебральной атрофии новорожденных
Основным этиологическим фактором уменьшения толщины полушарий новорожденных является внутриутробная гипоксия, проблемы во время родов. Повреждения головы малыша при прохождении по родовым путям провоцируют черепно-мозговую травму, способствуют появлению гидроцефалии (водянки).
Причины атрофических церебральных изменений новорожденных:
- Повреждение костей черепа;
- Увеличение количества спинномозговой жидкости (гидроцефалия);
- Внутриутробные инфекции (цитомегалия, герпес, менингит).
Не существует эффективных методов лечения атрофии новорожденных. Своевременное выявление с помощью МРТ позволяет назначить поддерживающую терапию, уменьшить прогрессирование заболевания. Умеренные изменения коррелируются медикаментозной терапией. Ребенок сможет посещать детский сад, учиться в специальной школе.
Аутоиммунные энцефалиты
После разговора об особом иммунном статусе мозга мы перейдем к теме аутоиммунных энцефалитов — группе заболеваний, которые связаны с поражением мембранных и внутриклеточных структур нейронов собственным иммунитетом организма. В современной практике аутоиммунные энцефалиты диагностируются редко. Это объясняется тем, что первые случаи подробно описали только в 2005 году [10]. Можно предположить, что на самом деле случаев этого заболевания больше, чем регистрируется специалистами. Некоторым пациентам с аутоиммунным энцефалитом могут устанавливать диагноз других расстройств, например, шизофрении или инфекционного энцефалита. Это связано с тем, что врачи мало осведомлены об этом заболевании. Врачи диагностируют только те болезни, которые им известны. Чем больше арсенал диагнозов в запасе у врача, тем точнее диагностика и правильнее лечение.
Аутоиммунные энцефалиты можно разделить на две группы:
- заболевания, вызванные активированными T-клетками (нечто похожее происходит при рассеянном склерозе [11]);
- заболевания, которые возникают при воздействии антител на внутри- и внеклеточные компоненты нейрона, например, ионные каналы.
Для первой группы аутоиммунных энцефалитов характерно повреждение клеток антителами и активированными Т-лимфоцитами [12]. Эти энцефалиты носят более тяжелый характер и требуют интенсивных лечебных вмешательств в отличие от представителей второй группы.
Во второй группе энцефалитов поражение нейронов носит только «поверхностный» характер. Воздействие специфических антител на поверхностно расположенные структуры приводит к тому, что происходит «стягивание» рецепторов (по-английски это называется capping — «сшивание») и их последующая интернализация (захват) в цитоплазму (рис. 3) [13]. Кроме этого аутоантитела могут сами соединяться с рецепторами, блокируя их работу [14].
Рисунок 3. Изменения, которые происходят с рецепторами при аутоиммунных энцефалитах, схожи с изменениями в синапсах при миастении. В норме (левая часть рисунка) рецепторы свободны и легко взаимодействуют с нейромедиатором ацетилхолином. В случае болезни на рецепторы начинают воздействовать антитела, и нарушается их способность связываться с нейромедиатором. «Слипшиеся» рецепторы к ацетилхолину постепенно втягиваются в цитоплазму, где разрушаются.
сайт memorangapp.com
Антитела проникают снаружи, из-за пределов ГЭБ, или производятся проникшими в головной мозг и активированными B-лимфоцитами [15]. В тех случаях, когда антитела направлены против внутриклеточных структур, атаку на нейроны возглавляют цитотоксические T-лимфоциты. При помощи перфорина и гранзима B они повреждают мембрану нейронов, что приводит к их гибели [16], [17]. ГЭБ, о котором мы говорили выше, в этом свете представляется надежной крепостной стеной, защищающей тихий город, который отвык воевать. Если в стене возникнет брешь, то город быстро падет: нервные клетки окажутся слишком чувствительны к воздействию иммунных факторов.
В поисках флагов
Признаки аутоиммунных энцефалитов очень разнообразны, но можно выделить три типа симптомов.
- Психиатрические симптомы: психозы, агрессивные действия, сексуальная расторможенность, панические атаки, навязчивые действия, чувство эйфории или страха.
- Двигательные симптомы: повышение тонуса мышц и его неравномерность, мышечные подергивания и повторяющиеся движения конечностей.
- Припадки: генерализованные эпилептические припадки, эпилептический статус.
Начальными проявлениями аутоиммунного энцефалита могут быть симптомы психического расстройства: нарушение памяти, галлюцинации или появление бредовых идей. Например, при аутоиммунном поражении глутаматных NMDA-рецепторов у 80% пациентов были выявлены симптомы психических заболеваний, а больше 60% первоначально были госпитализированы в психиатрические отделения [18], [19]. Врачи-психиатры должны уметь выявлять пациентов с аутоиммунными энцефалитами или хотя бы заподозрить это заболевание, чтобы вовремя отправить пациента на соответствующие обследования и консультации к другим врачам.
Среди многообразия симптомов, которые могут быть вызваны разными причинами, легко потеряться. Врачу требуются хотя бы приблизительные ориентиры, чтобы заподозрить диагноз аутоиммунного энцефалита. В результате анализа множества случаев заболевания выявили признаки, которые с большой вероятностью указывают на этот диагноз — так называемые «красные флаги» аутоиммунного энцефалита [20]. К ним относятся:
- Лимфоцитарный плейоцитоз или появление олигоклональных полос при электрофорезе ЦСЖ.
- Эпилептические припадки.
- Фациобрахиальные дистонические припадки.
- Подозрение на злокачественный нейролептический синдром.
- Отклонения на МРТ.
- Отклонения на ЭЭГ.
Кроме того, исследователи определили и «желтые флаги» — признаки, которые должны насторожить врача и заставить его задуматься о возможном диагнозе аутоиммунного энцефалита [20]. «Желтыми флагами» аутоиммунного энцефалита являются:
- Сниженный уровень сознания.
- Нарушение позы и движений.
- Нестабильность вегетативной нервной системы.
- Очаговая неврологическая симптоматика.
- Нарушения речи (афазия и дизартрия).
- Быстрое, несмотря на лечение, прогрессирование психоза.
- Гипонатриемия.
- Кататония.
- Головные боли.
- Наличие других аутоиммунных заболеваний, в том числе тиреоидитов.
Если врач видит симптомы из группы «красных флагов» у пациента, то авторы исследования рекомендуют проведение анализов на специфические аутоантитела для своевременной диагностики аутоиммунного энцефалита. При наличии у пациента симптомов из списка «желтых флагов» врачу следует заподозрить возможность такого диагноза и более тщательно обследовать пациента для поиска более достоверных признаков аутоиммунного энцефалита.
Дополнительные аргументы
Кроме совокупности ранее описанных симптомов, диагноз аутоиммунного энцефалита должен быть подтвержден лабораторными исследованиями и другими диагностическими процедурами [21]. Например, можно выполнить анализ на антитела к конкретным рецепторам. При аутоиммунном энцефалите, поражающем глутаматные NMDA-рецепторы, можно обнаружить повышение титра антител к ним. Интересно, что при энцефалите увеличивается количество иммуноглобулинов класса G, а при шизофрении — классов А и М [22]. В настоящее время установлено соответствие между антителами, поражающими конкретные структуры нейрона, и симптоматикой энцефалита (табл. 1). При проведении магнитно-резонансной томографии (МРТ) могут быть обнаружены изменения в структуре головного мозга, а электроэнцефалографическое исследование (ЭЭГ) в случае аутоиммунного энцефалита может показать нарушение функционирования головного мозга.
Таблица 1. Соответствие симптомов и аутоантител при аутоиммунных энцефалитах[20]
| Структура, к которой вырабатывается антитело | Психиатрические симптомы | Другие симптомы | Типичный пациент |
| NMDA-рецептор | Психоз, шизофреноподобные расстройства, кататония, агрессия | Эпилептические припадки, дискинезия, вегетативная нестабильность, нарушение речи и сознания | Молодые женщины, частая связь с тератомой яичника |
| Caspr2 | Бессонница, панические атаки, депрессия, шизофреноподобные расстройства | Синдром Морвана, нейромиотония, мышечные спазмы, фасцикуляции | Пациенты среднего и старшего возраста, возможна связь с тимомой |
| LGI1 | Амнезия и другие нарушения памяти, спутанность, депрессия | Лимбический энцефалит, фациобрахиальные дистонические припадки, гипонатриемия | Пациенты среднего и старшего возраста, соотношение мужчин и женщин 2:1, возможна связь с тимомой |
| Глициновый рецептор | Поведенческие изменения, шизофреноподобный синдром | Синдром мышечной скованности, прогрессирующий энцефаломиелит с ригидностью, миоклонус, гиперэкплексия | Пациенты среднего и старшего возраста, возможна связь с тимомой и лимфомой |
| Синаптические антигены (GAD) | Шизофреноподобный синдром, аутизм, синдром дефицита внимания и гиперактивности | Лимбический энцефалит, синдром мышечной скованности, припадки, стволовая дисфункция, атаксия | Пациенты среднего и старшего возраста, возможна связь с мелкоклеточным раком легких |
| Онконевральные антигены (Yo, Hu, CV2, Ri, Ma2) | Поведенческие нарушения | Лимбический энцефалит, мозжечковая дегенерация, сенсорная нейропатия | Пожилые пациенты, часто со злокачественными опухолями |
В некоторых случаях аутоиммунное поражение центральной нервной системы вызвано развитием паранеопластического синдрома, который может сопровождать появление в организме злокачественной опухоли. При паранеопластическом синдроме опухоль может начать самостоятельно вырабатывать гормоны и гормоноподобные вещества, нарушая регуляцию различных процессов в организме. Кроме этого паранеопластический синдром может проявляться в виде аутоиммунного заболевания, например, аутоиммунного энцефалита.
Патогенез аутоиммунного энцефалита в рамках паранеопластического синдрома заключается в следующем. В злокачественной опухоли определенной ткани экспрессируются гены, типичные для нее, а также гены, которые обычно «молчат» в ней. Среди «молчащих» генов могут оказаться и те, которые в норме экспрессируются только в мозге, под защитой ГЭБ. Поэтому получающиеся белки носят название раково-нейрональных антигенов. За время созревания иммунной системы она знакомится почти со всеми белками организма, однако эти белки оказываются скрыты от нее и, соответственно, воспринимаются как чуждые. С точки зрения нашего иммунитета между ними и бактериальными антигенами нет никакой разницы. Опухоль начинает производить раково-нейрональные антигены, а иммунная система распознает их и вырабатывает специфичные к ним аутоантитела. Через минимальные бреши в ГЭБ аутоантитела проникают в центральную нервную систему и начинают атаковать нейроны [14].
По этой причине при диагностике аутоиммунных энцефалитов отдельное внимание уделяется поиску опухоли в организме пациента. Удаление опухоли в случаях паранеопластического генеза аутоиммунного энцефалита приведет к значительному улучшению состояния пациента. Пока же опухоль находится в организме человека, антитела продолжают вырабатываться, а состояние пациента ухудшаться.
Удар по иммунитету
В качестве препаратов первой линии лечения аутоиммунных энцефалитов используют стероиды и иммуноглобулины, вводимые внутривенно. Стероиды обладают мощным противовоспалительным эффектом. Они способны подавить иммунные реакции на самых разных уровнях. Применение стероидов приводит к уменьшению синтеза медиаторов воспаления, стабилизации мембран лизосом, выделяющих воспалительные факторы. Кроме этого под воздействием стероидных гормонов снижается миграция моноцитов. Также может помочь и плазмаферез, очищающий кровь от «лишних» антител.
Если терапия первой линии не работает, то переходят к использованию ритуксимаба и циклофосфамида. Ритуксимаб — это моноклональные антитела к рецептору CD20, который обнаруживается на поверхности B-лимфоцитов [23]. В-лимфоциты производят самые разные антитела, в том числе и аутоантитела против нервных клеток, и их уничтожение может привести к улучшению состояния. Рецептор CD20 появляется на поверхности нормальных B-лимфоцитов и B-лимфоцитов, которые прошли процесс малигнизации (озлокачествления). Благодаря этому свойству ритуксимаб эффективен при аутоиммунных заболеваниях и B-клеточных лимфомах. Лекарство присоединяется к рецептору CD20 на поверхности лимфоцита и дает возможность другим компонентам иммунной системы уничтожить клетку.
Циклофосфамид обладает иммуносупрессивным действием и способен подавить избыточный иммунный ответ организма. После прохождения через печень циклофосфамид превращается в несколько активных метаболитов, которые проникают в клетку и плотно соединяют между собой две нити ДНК. Это препятствует делению опухолевых или других быстро делящихся клеток (например, B- и Т-лимфоцитов). По этой причине циклофосфамид входит в схему лечения некоторых аутоиммунных заболеваний. Тонкость использования стероидов, циклофосфамида и ритуксимаба при аутоиммунных энцефалитах заключается в том, что эти препараты могут осложнить диагностику тех опухолей, которые связаны с появлением аутоантител. При лимфоме назначение этих лекарств способно временно улучшить состояние, но при отмене опухоль снова «возьмется за старое» и будет производить аутоантитела. Хотя лимфома не так часто осложняется аутоиммунным энцефалитом, эту особенность надо учитывать при терапии.
На примере аутоиммунных энцефалитов можно рассмотреть два важнейших тренда в современной медицине. Первый тренд — изучение влияния иммунных процессов на функционирование нервной системы человека и попытки вмешаться в этот процесс при лечении неврологических и психических заболеваний. Сейчас мы близки к пониманию того, что мозг — это не просто электрохимическая лаборатория под черепной коробкой, но и особый иммунный мир со своими правилами. В наших интересах изучить эти правила и начать играть по ним в свою пользу. Второй же тренд — это биологизация психиатрии, поиск конкретных биологических изменений в организме, которые приводят к нарушению психического здоровья. Психиатрия — это часть медицины, большой отрасли, где соединяются теоретические знания и их практическое применение. Без биологической основы медицина перестанет быть научной. Если игнорировать биологические законы и знания внутри одной из медицинских специальностей, то с ней произойдет то же самое. Психиатрия должна становиться биологической, чтобы оставаться научной и выполнять свои медицинские задачи.
Новые горизонты
В последнее время исследователи и врачи все больше внимания уделяют реакциям врожденного иммунитета при развитии нейродегенеративных заболеваний (болезни Альцгеймера [24], болезни Паркинсона [25], хореи Гентингтона [26]) и психических расстройств [27]. Накопление бета-амилоида, который сам, вероятнее всего, вовлечен в иммунные реакции центральной нервной системы [28], связано с нарушением баланса между его накоплением и элиминацией (удалением). Последний процесс отчасти зависит от того, как экспрессируется толл-подобный рецептор 2 (TLR2) [29]. На мышиных моделях показано: чем ниже уровень экспрессии TLR2, тем хуже удаляется бета-амилоид [30]. Снижение элиминации бета-амилоида приводит к его накоплению в нервных клетках и последующему нарушению их функции и гибели. Изучение внутренних иммунных процессов мозга может стать основой для поиска новых препаратов при нейродегенеративных заболеваниях. Сейчас фармацевтические компании тестируют моноклональные антитела для терапии болезни Альцгеймера, но успехи остаются скромными.
Субатрофия мозга – первая стадия старческого слабоумия
До возникновения клинических симптомов развиваются субатрофические изменения. Внешние симптомы отсутствуют. Состояние сопровождается частичным снижением функции сегмента полушарий.
Морфологические виды субатрофии:
- Лобная;
- Лобно-височная;
- Теменно-затылочная.
Первая разновидность характеризуется снижением умственной активности, потерей речевых и двигательных функций.
Повреждение лобно-височных областей приводит к снижению слуховой способности человека, утрачиваются коммуникативные функции (сложности общения с другими людьми), нарушается функционирование сердечнососудистой системы.
Субатрофия уменьшает объем серого и белого вещества. Возникают нарушения проводниковой, двигательной функции, мелкой моторной активности.
Литература
- Craig L Hyde, Michael W Nagle, Chao Tian, Xing Chen, Sara A Paciga, Jens R Wendland, et al.. (2016). Identification of 15 genetic loci associated with risk of major depression in individuals of European descent. Nat Genet
.
48, 1031-1036; - Novel study method identifies 15 genomic regions associated with depression. (2016). Science Daily;
- Код жизни: прочесть не значит понять;
- Генетика псориаза: иммунитет, барьерная функция кожи и GWAS;
- GWAS и психогенетика: консорциумы в поисках ассоциаций;
- Загадочная генетика «загадочной болезни кожи» — витилиго;
- Wei Cheng, Edmund T. Rolls, Jiang Qiu, Wei Liu, Yanqing Tang, Chu-Chung Huang, et al.. (2016). Medial reward and lateral non-reward orbitofrontal cortex circuits change in opposite directions in depression. Brain
.
139, 3296-3309; - Depression’s physical source discovered. (2016). Science Daily..
Особенности кортикальной атрофии
Отмирание корковых клеток начинается с лобных долей, где располагаются функциональные центры контроля движения, речи. Постепенно атрофия распространяется на окружающие структуры. У пожилых людей патология приводит к старческому слабоумию.
Диффузные кортикальные изменения сопровождаются расстройством микроциркуляции, прогрессирующими клиническими симптомами. Нарушается мелкая моторика верхних конечностей, координация движений. Патологический комплекс приводит к болезни Альцгеймера, старческому слабоумию.
МРТ при кортикальной атрофии показывает уменьшение размеров лобных долей. Если изменения с обеих сторон, нарушается работа внутренних органов, контролируемых лобными долями.
Врожденная корковая атрофия новорожденных локализуется с одной стороны. Симптоматика выражена слабо. С помощью реабилитационных процедур удается социализировать ребенка.
Что делать чтобы остановить отмирание
Если отмирание клеток уже началось, то его следует затормаживать и останавливать. Сделать это можно при помощи лекарственной терапии. Группы средств, которые используют в медицине:
- Антиоксиданты.
- Нейропептиды.
- Нейрометалолиты.
- Витамины и минералы.
Внутри каждый клетки мозга имеются радикалы. Когда их становится слишком много — они просто убивают эту клетку. С таким процессом прекрасно справляются антидепрессанты. К сожалению, к ним быстро привыкают и они имеют выраженные побочные действия.
Нейропептиды, в свою очередь, замедляют процесс гибели и управляют здоровыми клетками, а также строят новые.
Многие чувствуют эффект после начала приема данных групп препаратов, ведь это своего рода профилактика от нежелательных осложнений, когда болезнь заходит далеко и уже вряд ли чем можно спасти ситуацию.
Клинические симптомы мультисистемной атрофии
Диффузная нейродегенерация сопровождается проблемами со стороны половой, мочевыводящей сферы. Некроз многих отделов мозга одновременно сопровождается разнообразными клиническими симптомами:
- Мышечный тремор при Паркинсонизме;
- Нарушение походки, координации подвижности;
- Потеря эрекции;
- Вегето-сосудистые расстройства.
До появления магнитно-резонансной томографии ранняя диагностика заболевания проблематична. Только ядерно-магнитный резонанс верифицирует уменьшение толщины мозговой паренхимы.
Клинические симптомы мозговой атрофии
Проявления патологии во многом определяются причинами и провоцирующими факторами. У большинства пожилых людей присутствует деменция, синдром лобной доли, внутренняя полиорганная патология.
Чем проявляется синдром лобной доли:
- Отсутствие аппетита;
- Потеря памяти, интеллектуальной активности;
- Частые эмоциональные срывы;
- Отсутствие коммуникации с окружающими людьми;
- Раздражительность;
- Отсутствие самокритики.
Психоорганический синдром сопровождается цереброастеническими расстройствами, аффективными нарушениями, амнезией.
Адекватная оценка окружающих событий, самокритика у пациента отсутствует. Появляется примитивность мышления, одностороннее представление сути детали. Речевой запас уменьшается, появляется парамнезия.
Сопутствующие аффективные расстройства приводят к депрессивному синдрому, неадекватному психическому состоянию. Плаксивость, обидчивость, раздражительность, необоснованная агрессия – типичные проявления патологии.
Виды и классификация атрофии головного мозга
По степени опасности разделяют два вида атрофических изменений мозга:
- Физиологическая;
- Патологическая.
Первый вид является естественным. На протяжении развития человека сопровождает вначале гибель пупочных артерий, артериального протока (новорожденных). После полового созревания утрачиваются ткани вилочковой железы.
В пожилом возрасте возникают дегенеративные изменения половой сферы. У людей преклонного возраста появляется кортикальная деструкция, инволюция лобной части. Состояния является физиологическими.
Виды патологической атрофии:
- Дисфункциональная – развивается при снижении функциональной активности мозга;
- Компрессионная – провоцируется повышенным давлением на мозговые ткани (гидроцефалия, гематома, обильное скопление крови);
- Ишемическая (дисциркуляторная) возникает по причине сужения просвета артерий атеросклерозом, сгустками крови, повышенной неврогенной активностью. Генерализованная церебральная гипоксия сопровождается не только умственным слабоумием, склеротическими внутримозговыми изменениями;
- Нейротическая (неврогенная) формируется из-за снижения поступления нервных импульсов к внутреннему органу. Состояние формируется из-за постепенных кровоизлияний, присутствия внутримозговых опухолей, атрофии зрительного или тройничного нерва. Возникает при хронической интоксикации, воздействии физических факторов, лучевой терапии, длительном лечении нестероидными противовоспалительными препаратами;
- Дисгормональная – возникает на фоне эндокринного дисбаланса со стороны яичников, семенников, щитовидной железы, молочных желез.
Морфологические виды атрофии мозга:
- Гладкая – поверхность мозга сглаживается;
- Бугристая – неравномерное распределение участков некроза формирует особую структуру;
- Смешанная.
Классификация по распространенности повреждения:
- Очаговая – прослеживаются лишь отдельные участки атрофического повреждения мозговой коры;
- Диффузная – распространяется по всей поверхности паренхимы;
- Частичная – некроз ограниченной части мозга;
- Полная – атрофические изменения белого и серого вещества, дегенерация тройничного и зрительного нерва.
Характер морфологических изменений мозга выявляет магнитно-резонансное сканирование. Проводить сканирование следует после появления первых клинических симптомов.
Как сохранить нейроны
Нервные клетки восстанавливаются — миф или реальность? В процессе эмбриогенеза внутри организма закладываются и формируются все клетки, ткани и органы, именно в таком порядке. Огромное количество клеток головного мозга образуется еще до рождения ребенка — часть он теряет при рождении еще часть в процессе первых лет жизни и так на протяжении всего жизненного пути. Восстановление нервных клеток — это миф, который можно превратить в реальность приложив немого усилий. Усилия эти заключаются не только в тренировки памяти и внимания различными упражнениями, чтение книг, просмотр фильмов, интеллектуальные игры, но и правильное питание — оно является залогом здоровья всего тела.
Следующие факторы способны сохранить, продлить жизнь и восстановить нейроны:
- Достаточное количество кислорода. Ни для кого не секрет, что мозг питается кислородом, а значит для его правильного и нормального функционирования этого элемента должно быть много. Чистая вода, продукты, которые стимулируют выработку гемоглобина и головной мозг будет питаться в нужном количестве.
- Сосудистое равновесие. Бляшки из холестерина, которые прикрепляются к сосудам, нарушают ток крови, а значит и кислорода, а значит и питания головного мозга
- Витаминные и минеральные комплексы. Помимо витаминов и минералов, которые поступают в организм с пищей, необходимо курсами употреблять калий, кальций, магний, фосфор и йод.
- Эмоциональный комфорт. Конечно же, благоприятный психоэмоциональный фон для человека — это важный аспект в данном процессе.
Формы мультисистемной атрофии
Опасность множественных поражений мозговых структур определяется комплексом патологических повреждений со стороны полушарий, подкорковых образований, мозжечка, спинномозгового ствола, белого вещества. Сопутствующие изменения зрительного нерва приводит к слепоте, тройничного нерва – нарушению иннервации лица.
Формы мультисистемной атрофии:
- Оливопонтоцеребеллярная – повреждения мозжечка с нарушением подвижности;
- Стриатонигральная дегенерация – мышечный тремор с проявления Паркинсонизма;
- Синдром Шая-Дрейджера – вегето-сосудистая дистония, снижение артериального давления;
- Амиотрофия Кугельберга-Веландера – атрофия мозга с гипотрофией мышц, гиперплазией соединительнотканных волокон.
Симптоматика определяется преимущественной формой поражения.
Основные стадии атрофических мозговых изменений
Заболевание имеет пять степеней течения. По клиническим симптомам удается верифицировать нозологии, начиная с второй-третьей стадии.
Степени кортикальной атрофии:
- Клинически симптомы отсутствуют, но патология быстро прогрессирует;
- 2 степень – характеризуется снижением коммуникабельности, отсутствием адекватной реакции на критические замечания, увеличивается число конфликтов с окружающими людьми;
- Отсутствие контроля поведения, беспричинный гнев;
- Потеря адекватного восприятия ситуации;
- Исключение психоэмоцинальной составляющей поведенческих реакций.
Выявления любого симптома требует дополнительного изучения структуры мозга.
Принципы диагностики атрофии
Первоначальный этап предполагает сбор анамнеза, осмотр, физикальное обследование. Второй этап – клинико-инструментальные методы (УЗИ, КТ, МРТ головного мозга, сцинтиграфия, ПЭТ/КТ). Повреждение зрительного нерва подтверждается офтальмоскопией, тонометрией, контрастной КТ или МРТ-ангиографией.
Лучшим способом выявления патологии мягких тканей головного мозга является МРТ. Процедуру нужно выполнять несколько раз (с разницей через месяц), чтобы выявить атрофию разной глубины, распространенности.
Магнитно-резонасное обследование выявляет самые мелкие локальные очаги, помогает правильно установить степень прогрессирования болезни.
Причины гибели нейронов
Отмирание клеток головного мозга — это процесс, который происходит на протяжении всей жизни человека. Врачи говорят, что в молодом возрасте это не страшно, так как организм молодой — роль играет в этом случае наследственный фактор. Люди пожилого возраста, особенно после 55 лет, с таким явлением сталкиваются намного чаще и диагностируют его в несколько раз больше. Виной этому могут стать следующие причины:
- Инфаркт — процесс нарушения тока крови к главной сердечной мышце.
- Инсульт — процесс нарушения тока крови в головной мозг (нарушение мозгового кровообращения).
- Промышленные выбросы, условия рабочего труда, экология.
- Ранее полученные травмы.
- Наследственность и генетическая предрасположенность.
- Период беременности (употребление матерью наркотических препаратов, сигарет, алкоголя), непрофессионализм врачей — гинекологов и акушеров.
Причин распространения такого явления достаточно много. В настоящее время показатели МРТ и КТ все чаще и чаще диагностируют серьезные изменения в нейронах головного мозга.